2. 芜湖市眼科医院一病区,芜湖 241001
2. Primary Disease Area, Wuhu City Eye Hospital, Wuhu 241001, China
失能是指由于机体衰老、伤残、疾病或心理等问题造成活动能力的散失或躯体限制[1],全球糖尿病患者中糖尿病视网膜病变(Diabetic Retinopathy,DR)患病率约为22.27%[2]。中国约为18.45%[3],DR是导致全球糖尿病患者失明和失能的最主要原因[4],失能不仅增加家庭照护负担和社会疾病负担,还会严重影响患者生活质量,并增加患者后续多病症、心血管疾病及死亡风险[5-6]。目前,关于DR患者失能相关研究较少,临床中缺乏有效的风险筛查工具。因此,本研究调查并分析DR患者失能现状及影响因素,构建失能风险预测模型,为医护人员尽早识别失能DR患者提供依据。
1 对象与方法 1.1 调查对象便利选取2022年6月至2023年3月安徽省某三级眼科医院收治的476例DR患者作为研究对象,按7∶3比例随机分为训练集和验证集,训练集用于构建DR患者失能风险预测模型,验证集则用于验证预测模型。纳入标准:1)符合指南中DR的诊断标准[7];2)意识清楚,能正常沟通,并独立或协助完成问卷调查。排除标准:1)存在精神障碍疾病或严重躯体障碍。2)无法配合完成问卷调查者。本研究已获得医院伦理委员会批准(LLSP-202206),研究对象均知情同意并自愿参与本研究。
本研究预测模型最终纳入了8个预测因子,根据样本量计算要求[8],所需阳性失能DR患者数量应为预测因子数量的5~10倍。所需样本量至少为267例,最终纳入476例,其中,训练集333例,验证集143例。
1.2 调查工具 1.2.1 一般资料调查表参考国内外相关文献,经专家咨询及讨论后自行设计,包括以下2个部分。1)一般人口学资料。性别、年龄、婚姻状况、居住地、宗教信仰、居住方式、文化程度、个人月收入等。2)疾病相关资料。DR分期、糖尿病病程、病变眼、合并症情况、疾病检查治疗情况等。
1.2.2 症状与视功能调查问卷采用于强等[9]编制的视功能损害眼病患者生存质量量表中的症状与视功能维度(8个条目),构成DR患者症状与视功能调查问卷,各条目采用0~10级评分,其中1~4条目为反向计分,其余条目均为正向计分,总分范围为0~80分,得分越高,说明患者症状与视功能越好。该研究问卷Cronbach′s α为0.798。
1.2.3 疾病感知问卷简化量表采用Broadbent等[10]编制的疾病感知问卷简化量表(brief illness perception questionnaire,BIPQ)进行评估,该量表共包括3个维度,8个条目,分别为疾病认知(5个条目)、情绪(2个条目)、疾病了解(1个条目),前8个条目采用0~10级评分,其中3、4、7条目为反向计分,其余条目均为正向计分,总分范围为0~80分,得分越高,说明自觉疾病威胁程度越大。该研究量表Cronbach′s α为0.959。
1.2.4 焦虑和抑郁自评量表采用汪向东等[11]编制的焦虑自评量表(Self-Rating Anxiety Scale, SAS)及抑郁自评量表(Self-Rating Depression Scale, SDS)评估DR患者的焦虑和抑郁情况,各量表均包括20个条目,采用Likert 4级评分,“没有或偶尔”为1分,“有时”为2分,“经常”为3分,“总是如此”为4分,其中SAS量表(条目5、9、13、17、19)和SDS量表(条目2、5、6、11、12、14、16、17、18、20)的部分条目为反向计分,剩余条目均为正向计分,各量表20个条目总分相加乘以1.25后为最终得分,得分越高,说明患者焦虑、抑郁程度越高。该研究两个量表Cronbach′s α分别为0.789、0.804。
1.2.5 中文版健康促进生活方式量表-Ⅱ采用Chen[12]汉化修订的中文版健康促进生活方式量表-Ⅱ (Health-Promoting Lifestyle-Ⅱ Chinese,HPLP-ⅡC),该量表包括6个维度40个条目,分别为营养行为(5个条目)、健康责任行为(8个条目)、自我实现行为(8个条目)、社会支持行为(6个条目)、运动行为(6个条目)及压力处理行为(7个条目),各条目采用Likert 4级评分,“从不”为1分至“总是”为4分,总分范围为40~160分,得分越高,说明DR患者生活方式越健康。该研究该量表Cronbach′s α为0.961。
1.2.6 日常生活能力量表采用Zhang等[13]编制的日常生活能力量表(Activity of Daily Living Scale,ADL),该量表包括2个分量表共14个条目,分别是躯体生活自理量表(6个条目)和工具性日常生活活动量表(8个条目),各条目采用Likert 4级评分,“自己完全可以做”为1分至“完全不可以”为4分,总分范围为14~56分,14分表示未失能,>14分则表示失能,得分越高,说明DR患者功能受损越严重。该研究该量表Cronbach′s α为0.946。
1.3 资料收集开始调查前对6名调查员(4名护士和2名医生)进行统一培训,医生负责疾病评估(如DR分期),剩余其他资料由护士采集。问卷调查均采用纸质问卷进行一对一、面对面调查,调查前用统一指导语进行解释,并由调查人员根据问卷内容逐条提问代填。
1.4 统计学方法利用SPSS 27.0软件进行描述性统计分析,计数资料采用频数、百分比描述,非正态分布的计量资料采用中位数、四分位数描述,单因素分析采用χ2检验或Mann-Whitney U检验,将单因素分析中有统计学意义的变量进行二元logistic回归分析,构建风险模型并进行评价和验证,利用R软件绘制列线图。P<0.05差异具有统计学意义。
2 结果 2.1 调查对象的一般资料及失能发生情况训练集中,发放问卷350份,回收有效问卷333份,有效问卷回收率为95.14%。患者年龄为60(54,71)岁,其他一般资料见表 1。验证集中,共发放问卷150份,回收有效问卷143份,有效问卷回收率为95.33%。患者年龄为56(52,66)岁;男68例(47.55%),女75例(52.45%);在婚122例(85.31%),未婚/离婚/丧偶21例(14.69%);居住地农村65例(45.45%),非农村78例(54.55%);病程以0.5~10年居多,有72例(50.35%);中学或中专学历居多,有59例(41.26%);非独居者居多,有105例(73.43%);增殖期DR患者居多,有107例(74.83%);未合并其他眼症者居多,有83例(58.04%);合并其他慢性病者居多,有108例(75.52%)。训练集和验证集中失能发生率分别为33.33%(111/333),29.37%(42/143)。
| 表 1 训练集DR患者一般资料及失能风险的单因素分析(n/%) |
训练集中,两组间年龄、婚姻状况、居住地、个人月收入、糖尿病病程、是否手术治疗、定期眼年检、DR分期、症状与视功能、疾病感知、焦虑、抑郁、健康促进行为比较,差异有统计学意义(P<0.05)。见表 1。
2.3 DR患者失能风险的logistics回归分析与模型构建将单因素分析中有统计学意义的变量作为自变量,以是否失能为因变量(0=未失能,1=失能),进行二元logistic回归分析。DR分期、定期眼年检、疾病感知、抑郁、健康促进行为、症状与视功能、婚姻状况、年龄是DR患者失能风险的影响因素(P<0.05),见表 3。最终构建的DR患者失能风险预测模型:P=1/[1+exp(2.619-2.056×DR分期+1.028×定期眼年检-0.060×疾病感知-0.083×抑郁+0.024×健康促进行为+0.052×症状与视功能+1.152×婚姻状况-0.741×年龄)]。
| 表 2 自变量赋值表 |
| 表 3 DR患者失能风险的logistics回归分析 |
训练集中,Hosmer-Lemeshow检验中χ2=9.563,P=0.297,ROC曲线下面积为0.845,95%CI为0.804~0.886,约登指数最大值为0.554,灵敏度为0.910,特异度为0.644;验证集中,Hosmer-Lemeshow检验中χ2=5.575,P=0.695,ROC曲线下面积为0.877,95%CI为0.819~0.935,约登指数最大值为0.589,灵敏度为0.738,特异度为0.851,详见图 2。143名患者中,本风险预测模型判断45名DR患者会发生失能、98名不会发生,实际42名发生失能、101名未发生,本模型误判6例,总正确率为95.80%。
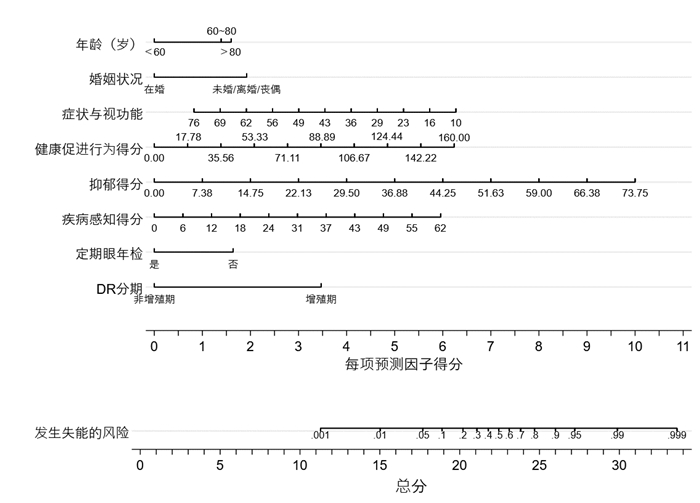
|
图 1 DR患者失能风险列线图 |
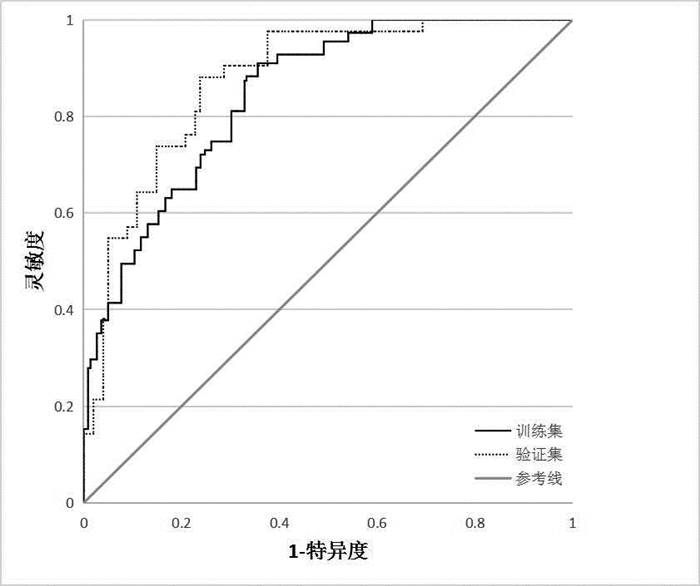
|
图 2 DR患者失能风险筛查模型的受试者操作特征曲线 |
本研究DR患者失能发生率为33.33%,高于糖尿病群体失能率的13.00%[14]、社区60岁以上老年群体失能率的11.40%[15],说明DR患者更易导致失能。早期识别失能高危DR患者,采取有针对性的措施干预,对促进患者功能恢复、提高生活质量具有重要作用。
3.2 DR患者失能影响因素分析 3.2.1 增殖期DR患者易发生失能本研究结果显示,增殖期DR是DR患者失能的危险因素。非增殖期DR患者通常无症状,而增殖期DR患者则由于视网膜或视盘上新生血管的形成常导致患者玻璃体积血而失明或因视网膜脱离而丧失视力[16],这一时期患者通过玻璃体切割术虽可以有效改善视力,但仍有超过1/4患者术后会发生视力残疾[17]。DR严重程度与糖尿病肾病和糖尿病神经病变的严重程度成正相关[18],这些原因均可能导致患者不同程度的生活能力下降。故临床医护人员因应注意关注患者病情发展进程及治疗效果,避免DR患者失能发生风险。
3.2.2 未定期眼年检的DR患者易发生失能本文结果显示,未定期进行眼年检是DR患者失能的危险因素。定期眼年检是预防DR进展的重要手段,通过早期正确的预防和治疗可使DR患者严重视力损伤风险降低94%[2]。农村患者、疾病认知、机构未定期提醒等因素是影响DR眼年检情况不佳的主要因素[19]。因此,临床医护人员应该加强DR患者健康教育,扩大医疗服务范围,并设置定期提醒等手段鼓励DR患者定期进行眼年检,避免患者失能风险。
3.2.3 疾病感知程度越高的DR患者易发生失能本研究结果显示,疾病感知程度越高的DR患者发生失能的风险越高,疾病感知是影响半失能患者社会疏离、疾病复发恐惧等的重要因素[20]。因此,临床医护人员采取有针对性措施,降低患者疾病感知程度,预防失能。
3.2.4 抑郁程度越重的DR患者易发生失能本研究结果显示,抑郁程度越重的DR患者发生失能的风险越高,这与尹振华[21]的研究结果相似。抑郁症与慢病共存的患者会导致更为严重的功能障碍和躯体障碍,不良情绪会进一步影响患者躯体功能、认知功能,导致活动的减少、社会功能的弱化[22]。因此,临床医护人员应鼓励DR患者发泄不良情绪,进行心理干预,对预防失能有积极地影响。
3.2.5 不良生活方式的DR患者易发生失能本研究结果显示,不良生活方式的DR患者发生失能的风险越高,这与王秀芳[23]的研究结果相似。生活方式干预包括合理饮食、适量运动、规律睡眠等,是延缓DR发展进程,有效改善患者视力并降低并发症的重要控制手段。因此,临床医护人员可通过全科治疗、延续护理等方式有效干预DR患者生活方式,积极避免患者失能的发生。
3.2.6 症状与视功能越差的DR患者易发生失能本研究结果显示,DR患者的症状与视功能越差,其发生失能的风险越高,视力状况是影响视力障碍老年人社会功能的主要影响因素[24],包括认知功能、自理能力、社会参与等方面。因此,早发现早治疗,注重低视力DR患者视力保护,通过有效手段预防视力进一步恶化。
3.2.7 未婚、离婚和丧偶的DR患者易发生失能本研究结果显示,未婚、离婚和丧偶的DR患者易发生失能。配偶是DR患者社会支持的重要来源,婚姻状况是影响失能老年人家庭代际团结的主要影响因素[25]。配偶的照顾对保护患者自理能力起到重要促进作用[26]。由此,临床医护人员应注意关注不再婚DR患者的心理情况,鼓励子女、朋友及社会团体关心及照护,加强其社会支持水平,避免失能风险的发生。
3.2.8 年龄越大的DR患者易发生失能本研究结果显示,DR患者年龄越大,其发生失能的风险越高,这与张妍等[15]结果相似。增殖期DR患者,年龄越大,治疗后视力预后效果越差[27]。且随着年龄的增长,患者认知功能及生理功能均发生不同程度的退化,导致失能。因此,临床上应将老年DR患者作为失能防治的重点对象,社会上应加大老年DR患者照护投入水平。
4 小结本研究显示,年龄、婚姻状况、DR分期、定期眼年检、症状与视功能、疾病感知、抑郁、健康促进行为是DR患者失能发生的预测因素,通过列线图预测模型可有效筛查DR失能高危患者。本文研究对象均来源于同一家医院,样本量相对较少,且纳入模型的影响因素有限。因此,还需通过多中心、大样本的研究对该模型进行进一步的验证与完善,为临床筛查DR失能高危患者并采取针对性干预提供有效依据。
利益冲突:所有作者均申明不存在利益冲突。
| [1] |
Leonardi M, Lee H, Kostanjsek N, et al. 20 years of ICF-International Classification of Functioning, disability and dealth: Uses and applications around the world[J]. Int J Environ Res Public Health, 2022, 19(18): 11321. DOI:10.3390/ijerph191811321 |
| [2] |
Teo ZL, Tham YC, Yu M, et al. Global prevalence of diabetic retinopathy and projection of burden through 2045: Systematic review and meta-analysis[J]. Ophthalmology, 2021, 128(11): 1580-1591. DOI:10.1016/j.ophtha.2021.04.027 |
| [3] |
Song P, Yu J, Chan KY, et al. Prevalence, risk factors and burden of diabetic retinopathy in China: A systematic review and meta-analysis[J]. J Glob Health, 2018, 8(1): 010803. DOI:10.1097/MD.0000000000013678 |
| [4] |
Mohammadi M, Raiegani A, Jalali R, et al. The prevalence of retinopathy among type 2 diabetic patients in Iran: A systematic review and meta-analysis[J]. Rev Endocr Metab Disord, 2019, 20(1): 79-88. DOI:10.1007/s11154-019-09490-3 |
| [5] |
Qiao Y, Liu S, Li G, et al. Longitudinal follow-up studies on the bidirectional Association between ADL/IADL disability and multimorbidity: Results from two national sample cohorts of middle-aged and elderly adults[J]. Gerontology, 2021, 67(5): 563-571. DOI:10.1159/000513930 |
| [6] |
Son KY, Kim SH, Sunwoo S, et al. Association between disability and cardiovascular event and mortality: A nationwide representative longitudinal study in Korea[J]. PLoS One, 2020, 15(7): e0236665. DOI:10.1371/journal.pone.0236665 |
| [7] |
中华医学会眼科学会眼底病学组. 我国糖尿病视网膜病变临床诊疗指南(2014年)[J]. 中华眼科杂志, 2014, 50(11): 851-865. DOI:10.3760/cma.j.issn.0412-4081.2014.11.014 |
| [8] |
高永祥, 张晋昕. Logistic回归分析的样本量确定[J]. 循证医学, 2018, 18(2): 122-124. DOI:10.12019/j.issn.1671-5144.2018.02.015 |
| [9] |
于强, 李绍珍, 陈和年, 等. 视功能损害眼病患者生存质量量表的研究[J]. 中华眼科杂志, 1997, 33(4): 307-310. |
| [10] |
Broadbent E, Petrie KJ, Main J, et al. The brief illness perception questionnaire[J]. J Psychosom Res, 2006, 60(6): 631-637. DOI:10.1016/j.jpsychores.2005.10.020 |
| [11] |
汪向东. 心理卫生评定量表手册[M]. 增订版. 北京: 中国心理卫生杂志社, 1999: 160-161, 202-203.
|
| [12] |
Chen MY. The effectiveness of health promotion counseling to family caregivers[J]. Public Health Nurs, 1999, 16(2): 125-32. DOI:10.1046/j.1525-1446.1999.00125.x |
| [13] |
Zhang L, Du H, Song J. Effect of holistic nursing intervention combined with humanized nursing intervention on activities of daily living and limb movement ability of elderly patients with cerebral hemorrhage after surgery[J]. Evid Based Complement Alternat Med, 2021, 2021: 2480551. DOI:10.1155/2021/2480551 |
| [14] |
Gregg EW, Menke A. Diabetes and Disability[M]. 3rd ed, Bethesda (MD): National Institute of Diabetes and Digestive and Kidney Diseases(US), 2018: 33651544.
|
| [15] |
张妍, 袁红, 金亚清, 等. 上海市嘉定区社区老年人的失能现状及其影响因素[J]. 中华疾病控制杂志, 2022, 26(7): 784-789. DOI:10.16462/j.cnki.zhjbkz.2022.07.007 |
| [16] |
刘涵, 方晏红, 陈健. 糖尿病视网膜病变的全科医学管理[J]. 眼科学报, 2023, 38(4): 350-359. DOI:10.12419/j.issn.1000-4432.2023.04.07 |
| [17] |
王爽, 李晓鹏. 房水中内皮素-1、超氧化物歧化酶与糖尿病视网膜病变患者术后视力残疾的关系[J]. 眼科新进展, 2023, 43(3): 203-207. DOI:10.13389/j.cnki.rao.2023.0041.DOI:10.13389/j.cnki.rao.2023.0041 |
| [18] |
Saini DC, Kochar A, Poonia R. Clinical correlation of diabetic retinopathy with nephropathy and neuropathy[J]. Indian J Ophthalmol, 2021, 69(11): 3364-3368. DOI:10.4103/ijo.IJO_1237_21 |
| [19] |
师铖, 秦光浩, 林铁柱. 糖尿病视网膜病变眼年检障碍因素分析[J]. 国际眼科杂志, 2023, 23(4): 677-681. DOI:10.3980/j.issn.1672-5123.2023.4.29 |
| [20] |
鲍金雷, 杨庆爱, 张俊, 等. 脑卒中半失能老年患者复发恐惧的调查研究[J]. 中华护理杂志, 2021, 56(11): 1661-1666. DOI:10.3761/j.issn.0254-1769.2021.11.010 |
| [21] |
尹振华. 中老年人失能发生风险的列线图预测模型研究[D]. 青岛: 青岛大学, 2021.
|
| [22] |
Jiang C, Yin H, Liu A, et al. Dietary inflammatory index and depression risk in patients with chronic diseases and comorbidity[J]. J Affect Disord, 2022, 301: 307-314. DOI:10.1016/j.jad.2022.01.008 |
| [23] |
王秀芳. 老年人认知衰弱、焦虑抑郁与失能的相关性研究[D]. 延吉: 延边大学, 2022.
|
| [24] |
踪玮. 视力障碍老年人社会功能现况及影响因素分析[D]. 沈阳: 中国医科大学, 2022.
|
| [25] |
赵秋平, 张晓阳, 崔玉, 等. 社区中高龄失能老年人家庭代际团结现状及其影响因素[J]. 护理研究, 2023, 37(7): 1301-1304. DOI:10.12102/j.issn.1009-6493.2023.07.033 |
| [26] |
闫伟, 何梦娇, 路云, 等. 基于CLHLS的我国老年人失能现状及其影响因素研究[J]. 护理研究, 2021, 35(10): 1807-1811. DOI:10.12102/j.issn.1009-6493.2021.10.021 |
| [27] |
许领先. 不同年龄增殖性糖尿病性视网膜病变患者临床观察[D]. 长春: 吉林大学, 2021.
|

