1900年,Comberg提出了“有机自由基”的概念[1]。此后,大量关于自由基的科学研究迅速开展起来。20世纪50年代,Harman提出了“自由基学说”,自由基与放射线诱导突变和诱发肿瘤的机理有关[2]。
1968年,McCord报道超氧化物歧化酶(SOD)在抗氧化方面的生物学作用,开创了自由基生物的新篇章[3]。自由基在平衡状态下,其在消炎、抗菌及抑制肿瘤等方面具有重要作用和意义;一旦平衡被打破,如机体受疾病或某些外源性药物和毒物的影响,自由基便会产生巨大的伤害作用,导致生物膜的脂质过氧化损伤,引起生命大分子(蛋白质、酶及氨基酸)的氧化破坏,导致对内脏器官、免疫系统的功能等产生影响,从而引起机体产生疾病,甚至死亡[4-6]。
许多疾病的发生、发展都与自由基有关[7]。动脉粥样硬化症、老年痴呆症、帕金森综合征、癌症等,以及胃肠消化、内分泌、新陈代谢、衰老等慢性疾病,都与氧自由基积累过多,以及过多自由基攻击生命大分子所造成的组织损伤有关。如何有效地清除体内过多自由基,减小其对人体的伤害成为研究热点之一[8-10]。
中药具有千百年的应用经验,对其性味、副作用及毒性有较为深刻的认识,因此,从中药中寻找具有抗氧自由基的活性成分是一条相对安全的途径。香豆素类化合物、桂皮醛及有机酸成分的肉桂酸,具有抗肿瘤、抗菌、抗炎等多种生物学活性,并表现出显著的抗氧化能力,但尚未见桂枝配方颗粒的抗氧化活性方面的研究[11-12]。本实验测定了不同批次桂枝配方颗粒的DPPH自由基清除能力、ABTS自由基清除能力和铁离子还原能力,综合评价不同批次桂枝配方颗粒的抗氧化活性,从而为药物药效物质基础的研究提供参考,可以更科学、合理地进行桂枝配方颗粒的质量控制及评价。
1 仪器与试剂 1.1 仪器十万分之一电子天平(梅特勒-托利多国际贸易(上海)有限公司,XS205DU); 紫外可见分光光度计(日本shimadzu公司,UV-2450);纯水/超纯水一体化系统(德国默克密理博公司,Milli-Q Integral 10);Eppendorf移液器,规格: 1000μl,200μl,20μl(Eppendorf公司,德国)。
1.2 试剂DPPH(1,1-二苯基-2-三硝基苯肼)、ABTS-(NH4)2(2,2’-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐)、过硫酸钾、盐酸、2,4,6-三吡啶基三嗪(TPTZ)(上海麦克林生化科技有限公司);三氯化铁(FeCl3)(天津市大茂化学试剂厂);硫酸亚铁(天津市大茂化学试剂厂);甲醇(分析纯,天津市致远化学试剂有限公司);醋酸钠(分析纯,天津市致远化学试剂有限公司);乙醇(分析纯,天津富宇);纯净水(杭州娃哈哈集团有限公司)。
2 方法 2.1 DPPH法测定抗氧化活性精密称取DPPH5.0000mg,置于烧杯中,加适量无水乙醇,避光超声使其充分溶解,再用无水醇定容至100mL,摇匀,配制成50mg/mL的DPPH溶液,避光保存。
精密称取0.5000g桂枝配方颗粒,精准加入20mL甲醇,超声(功率250W,频率35kHz)30min,过滤即得。
取3支试管并编号,在1号试管中加入1.5mL DPPH溶液和0.5mL供试品溶液,作为试验组(AS);在2号试管中加入0.5mL供试品溶液和1.5mL无水乙醇溶液,作为对照组(AC); 在3号试管中加入1.5mLDPPH溶液和0.5mL甲醇溶液,作为空白组(Ab)分别充分混合均匀后,室温避光反应30min,于波长517nm条件下,用紫外分光光度计测定其吸光度值(甲醇调零校准)。用以下公式计算其清除率:
| $ {\rm{DPPH}}清除率{\rm{=[1-(AS-AC)/Ab]×100\%}} $ |
其中,AS为待测溶液与DPPH溶液混合液的吸光度; AC为待测溶液与无乙醇溶液混合液的吸光度; Ab为DPPH溶液与样品溶剂溶液混合液的吸光度。
2.2 ABTS法测定抗氧化活性精密称取ABTS200.0000mg,过硫酸钾34.4000mg;溶于50mL蒸馏水,摇匀,室温避光放置24h后,作为ABTS母液。取适量ABTS母液,用95%乙醇稀释至吸光度值在0.70±0.02内(OD734)作为ABTS测定溶液,避光保存。
精密称取166.0000mg桂枝配方颗粒,精准加入20mL甲醇,超声(功率250W,频率35kHz)30min,过滤即得。
取2支试管并编号,在1号试管中加入3.6mLABTS溶液和0.4mL供试品溶液作为试验组(AS)。在2号试管中加人3.6mL ABTS溶液和0.4mL样品溶剂溶液(甲醇)作为空白组(Ab)分别充分混合均后,室温避光反应5min,于波长734nm条件下,用紫外分光光度计测定其吸光度值(样品溶剂调零校准)。用以下公式计算其清除率:
| $ {\rm{ABTS清除率=(Ab-AS)/Ab×100\%}} $ |
其中,Ab是ABTS溶液与样品溶剂溶液混合液的吸光度; AS是待测溶液与ABTS溶液混合液的吸光度。
2.3 FRAP法测定抗氧化活性精密称取2.5500g无水醋酸钠,加入10ml冰醋酸中,然后加水至125mL,混匀。
精密称取0.0278g FeSO4·7H2O,置于烧杯中,加入适量蒸馏水溶解,待溶解后,转移至100mL容量瓶中,定容,混匀,备用。
精密称取0.0808g TPTZ,溶解在25mL、40mmol/L的HCl溶液中。
精密称取0.1351g FeCl3·6H2O,溶于适量蒸馏水中,转移至25mL容量瓶中,定容,混匀。
按10mmol/L TPTZ溶液、20mmol/L FeCl3溶液、醋酸-醋酸钠缓冲液(pH 3.6)三者容积比为1∶1∶10。分别精密量取10mL TPTZ溶液和FeCl3溶液及100mL醋酸-醋酸钠缓冲液,混匀,备用。
精密称取0.5000g桂枝配方颗粒,精准加入20mL甲醇,超声(功率250W,频率35kHz)30min,过滤即得。
分别精密吸取0.1、0.2、0.4、0.6、0.8mmol/L的FeSO4标准液,加入1ml FRAP工作液,混匀,准确反应5min,于594nm处测定其吸光度,用超纯水调零,以Fe2+浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
样品的抗氧化活性(FRAP值)以达到相同吸光度所需FeSO4的mmol/L表示。精密吸取系列浓度供试液1mL及3 mL FRAP工作液摇匀后静置10min作为样品溶液; 用蒸馏水代替FeCl3溶液,同上述步骤操作配制空白溶液,在594nm处测定吸光度值,代入吸光度对Fe2+浓度的标准曲线得出FRAP值。
2.4 光谱预处理方法及校正模型的构建测量样品的近红外光谱时,由于光的散射和基线漂移等因素原始光谱会产生噪声信号,所以需要使用光谱预处理方法进行改善,从而有效提取样品的特征信息。本实验采用了8种预处理方法,分别为1st,SG,2nd,MSC,SNV及相结合的方法,之后各自建立PLS和SVR模型,得到相应模型参数。
3 结果 3.1 DPPH法测定抗氧化活性 3.1.1 DPPH清除能力不同批次桂枝配方颗粒对DPPH自由基的清除率为55.88%~91.39%,平均清除率为78.1%,标准偏差为7.08%。不同批次桂枝配方颗粒对DPPH自由基清除率均大于50%,说明桂枝配方颗粒具有较强的抗氧化性能。
3.1.2 不同预处理方法对DPPH清除率定量模型的影响为了更好地将原始光谱的模型结果和使用多种预处理方法得到的光谱定量模型结果进行对比,使用表格的形式将各种预处理之后的光谱定量模型预测结果呈现出来。预测能力是由校正相关系数(Rc)和预测相关系数(Rp)值检验的。SG+SNV方法得到的Rp值比其他方法均较高,Rc值高于或不明显低于其他方法,所以SG+SNV方法为PLS模型的最佳预处理方法,见表 1。SG+SNV方法得到的Rp值比其他方法均较高,Rc值高于或不明显低于其他方法,所以SG+SNV方法为SVR模型的最佳预处理方法,见表 2。
| 表 1 不同预处理方法对DPPH清除率定量PLS模型的影响 |
| 表 2 不同预处理方法对DPPH清除率定量SVR模型的影响 |
根据2表的结果可以看出,抗DPPH活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rp值为0.621,小于抗DPPH活性与近红外光谱建立的PLS模型中最佳预处理方法下的Rp值为0.769,Rc值为0.795。综合上述结果使用DPPH方法测定抗氧化活性时用PLS校正模型预测能力更好。
3.2 ABTS法测定抗氧化活性 3.2.1 ABTS清除能力不同批次桂枝配方颗粒对ABTS自由基的清除率为47.33%~85.45%,平均清除率为65.68%,标准偏差为9.38%。由此可得,不同批次桂枝配方颗粒对ABTS自由基清除率小于对DPPH自由基的清除率,说明桂枝配方颗粒对DPPH自由基的清除能力更强。
3.2.2 不同预处理方法对ABTS清除率定量模型的影响无预处理方法、SG+SNV、SG+SNV+一阶导数方法得到的Rp值比其他方法均较高,而无预处理方法和SG+SNV方法的Rc值明显低于其他方法,SG+SNV+一阶导数方法的Rc值高于或不明显低于其他方法,所以SG+SNV+一阶导数方法为PLS模型的最佳预处理方法,见表 3。SG+MSC+二阶导数方法得到的Rp值比其他方法均较高,Rc值高于或不明显低于其他方法,所以SG+MSC+二阶导数方法为SVR模型的最佳预处理方法,见表 4。
| 表 3 不同预处理方法对ABTS清除率定量PLS模型的影响 |
| 表 4 不同预处理方法对ABTS清除率定量SVR模型的影响 |
根据两表的结果可以看出,抗ABTS活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rp值为0.928,大于抗ABTS活性与近红外光谱建立的PLS模型中最佳预处理方法下的Rp值0.922。综合上述结果使用ABTS方法测定抗氧化活性时用SVR校正模型预测能力更好。
3.3 FRAP法测定抗氧化活性 3.3.1 FRAP值的表示方法样品的抗氧化能力以FRAP值表示:1FRAP单位=1mmol/L FeSO4,即样品的抗氧化能力相当于FeSO4的mmol/L数。
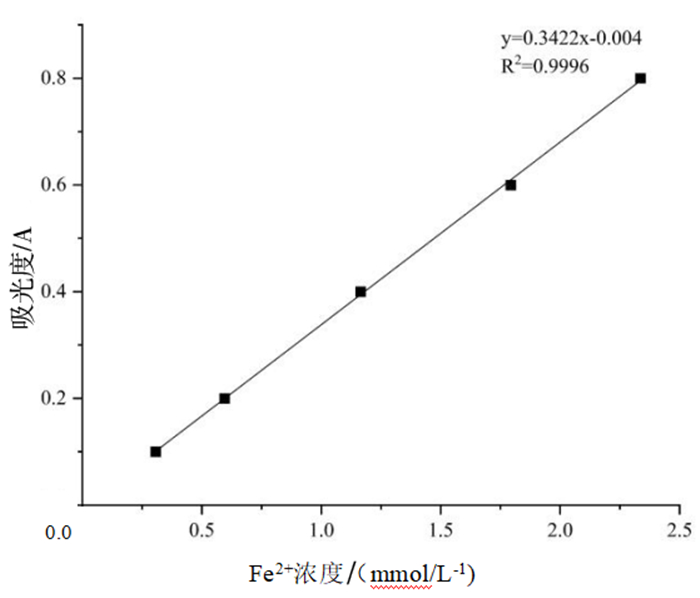
3.3.2 标准曲线标准曲线的回归方程为y=0.3422x-0.004,R2=0.9996,FeSO4在0.0~2.5mmol/L范围内与吸光度呈良好的线性关系,符合定量要求。见图 1。
|
图 1 FRAP标准曲线 |
取各批次样品,按“2.3”项下方法制备溶液并进行操作,测定吸光度,计算样品还原能力,以FRAP值表示,不同批次桂枝配方颗粒的FRAP值范围在0.18~0.37mmol,平均FRAP值为0.27mmol,标准偏差为0.04mmol。由此可知,FRAP(Ferric ion reducing antioxidant power),即“铁离子抗氧化能力法”。在低pH条件下,Fe3+-TPTZ复合物可被抗氧化物还原成Fe2+-TPTZ。Fe2+-TPTZ呈蓝紫色,在594nm下有强吸收,利用紫外分光光度法对其进行定量测定,25mg/mL的样品溶液FRAP值范围为:0.18~0.37,平均FRAP值为0.27,不同批次桂枝配方颗粒在FRAP抗氧化活性测定中均具有良好的抗氧化活性。
3.3.4 不同预处理方法对FRAP值定量模型的影响无预处理方法和SG+SNV方法得到的Rp值比其他方法均较高,但无预处理方法和SG+SNV方法的Rc值明显低于其他方法,所以即便使用预处理方法也不能提升PLS模型的预测能力,见表 5。SG+MSC方法得到的Rp值比其他方法均较高,Rc值高于或不明显低于其他方法,所以SG+MSC方法为SVR模型的最佳预处理方法,见表 6。
| 表 5 不同预处理方法对FRAP值定量PLS模型的影响 |
| 表 6 不同预处理方法对FRAP值定量SVR模型的影响 |
根据2表的结果可以看出,抗FARP活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rp值为0.573,Rc值为0.926,而抗FRAP活性与近红外光谱建立的PLS模型无预测能力。综合上述结果,使用FRAP方法测定抗氧化活性时用SVR校正模型预测能力更好。
4 讨论天然抗氧化剂来源于植物等天然产物,清除自由基的机理可以分为3种,一是自由基清除,二是抑制自由基生成,三是增强自身抗氧化体系。其中,自由基清除是最直接的抗氧化方式,应用较广泛。评价天然抗氧化剂清除自由基能力的方法有很多,包括DPPH法、ABTS法、FRAP法等。
ABTS法这种体外测定抗氧化能力的方法花费的时间短,经费少,所需仪器设备简单。其所测的值为被测物质总抗氧化能力,与其他一些总抗氧化能力体外测定法相比,ABTS法快速简便、与抗氧化剂的生物活性相关性强,因而较为广泛地应用于包括血清在内的生物样品、果蔬类和一些纯物质的抗氧化能力的测定。DPPH法快速、简单,但其检测波长与部分抗氧化物质本身的吸收波段重叠(如类胡萝卜素)。因此,在检测该类物质时,结果会有一定偏差。
ABTS和DPPH是测定抗氧化活性使用最广的两种人工生成的自由基,但是它们对抗氧化剂的响应以及它们的操作也有几个重要的不同: 1)DPPH不需制备可直接得到,而ABTS必须由酶或化学反应生成。2)ABTS可溶于水,也可溶于有机溶剂,所以既可测量水溶性化合物也可测量脂溶性化合物。而DPPH只能溶于有机溶剂,特别是乙醇,不溶于水,在评价水溶性抗氧化剂的作用时,有一定的局限。3)在与供氢体的反应上,DPPH比ABTS的选择性强。例如,DPPH不能与只含有一个羟基的芳香酸反应,也不能与苯环上没有羟基的类黄酮反应。而ABTS可与任何羟基化的芳香族化合物反应。因而,ABTS法比DPPH法更适合于提取物总抗氧化能力。
目前大多数测定抗氧化活性的方法是针对某一种自由基而言,如国外应用较多的氧自由基清除力法,该法需要昂贵的全自动生化分析仪,手工操作费时费力,国内一般实验室很难推广应用。和建立的法原理明确,操作简便,不需特殊仪器,易于标准化,已用于测定不同抗氧化物质、食物与生物样品的抗氧化活性。它反映的不是样品针对某一种自由基的清除活性,而是样品的总还原能力,一些学者因此认为该法测定结果可用来反映样品总抗氧化活性的强弱。此法真正测量的是被测物将还原成的能力。FRAP法操作简单快速,重复性好,易于标准化,最初用于测量血浆的活性,后来也用于测定其他生物体液、食品、植物提取物、果汁等的抗氧化活性。
根据3.1、3.2和3.3的结果可以看出,抗ABTS活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rp值为0.928,大于抗DPPH活性与近红外光谱建立的PLS模型中最佳预处理方法下的Rp值0.769,大于抗FARP活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rp值0.573。抗ABTS活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rc值为0.992,大于抗DPPH活性与近红外光谱建立的PLS模型中最佳预处理方法下的Rc值0.795,大于抗FARP活性与近红外光谱建立的SVR模型中最佳预处理方法的参数Rc值0.926,综合上述结果用近红外光谱法快速测定不同批次桂枝配方颗粒的抗氧化活性时采取ABTS方法测定抗氧化活性并用SVR校正模型可使预测能力更好。
桂枝配方颗粒具有高效的抗炎,抗氧化,抗癌等多方面的药理作用,本文论证了使用近红外光谱技术检测不同批次桂枝配方颗粒抗氧化活性的可行性。实验数据表明,近红外光谱法可有效预测不同批次桂枝配方颗粒的抗氧化活性。和FARP抗氧化活性之间有相关性。其中DPPH方法对应PLS模型的Rp值为0.769,Rc值为0.795;ABTS方法对应SVR模型的Rp值为0.928,Rc值为0.992;FARP方法对应SVR模型的Rp值为0.573,Rc值为0.926。结果表明近红外光谱可以应用于不同批次桂枝配方颗粒抗氧化活性的快速预测,对其他中药配方颗粒生物学活性的快速评价具有一定的参考意义。
利益冲突:所有作者均申明不存在利益冲突。
| [1] |
莫简. 自由基生物学导论[M]. 人民卫生出版社, 1998: 77.
|
| [2] |
赵保路, 黄可秦. 自由基与皮肤老化[J]. 生命的化学, 1991, 11(5): 32-34. |
| [3] |
闫道广, 周玫, 陈缓. 芦丁和槲皮素对低密度脂蛋白氧化修饰的抑制作用[J]. 生物物理学报, 1995, 11(1): 105-109. |
| [4] |
李勇, 孔令青, 高洪, 等. 自由基与疾病研究进展[J]. 动物医学进展, 2008, 29(4): 85-87. |
| [5] |
李涛, 余旭亚, 陈朝银, 等. 抗氧化剂的研究与应用现状[J]. 食品研究与开发, 2003, 24(2): 23-26. DOI:10.3969/j.issn.1005-6521.2003.02.009 |
| [6] |
彭长连, 陈少薇, 林植芳, 等. 用清除有机自由基DPPH法评价植物抗氧化能力[J]. 生物化学与生物物理进展, 2000, 27(6): 658-661. DOI:10.3321/j.issn:1000-3282.2000.06.022 |
| [7] |
柳爱莲, 刘绣华. 天然产物抗氧DPPH自由基活性研究[J]. 周口师范学院学报, 2007, 24(5): 80-82. |
| [8] |
Daud M, Wibowo A, Abdullah N, et al. Bioassay-guided fractionation of Artocarpus heterophyllus L.J33 variety fruit waste extract and identification of its antioxidant constituents by TOF-LCMS[J]. Food Chem, 2018, 266: 200-214. DOI:10.1016/j.foodchem.2018.05.120 |
| [9] |
Liu J, Zhang Q, Li RL, et al. The traditional uses, phytochemistry, pharmacology and toxicology of Cinnamomi Ramulus: a review[J]. J Pharm Pharmacol, 2020, 72(3): 319-342. DOI:10.1111/jphp.13189 |
| [10] |
Shin SH, Lee SR, Lee E, et al. Caffeic acid phenethyl ester from the twigs of cinnamomum cassia inhibits malignant cell transformation by inducing c-fos degradation[J]. J Nat Prod, 2017, 80(7): 2124-2130. DOI:10.1021/acs.jnatprod.7b00433 |
| [11] |
夏天卫, 周国威, 姚晨, 等. 桂枝及肉桂治痹的中医认识与现代药学研究进展[J]. 中国实验方剂学杂志, 2019, 25(6): 218-226. DOI:10.13422/j.cnki.syfjx.20190607 |
| [12] |
徐锋, 王德健, 王凤, 等. 桂枝挥发油的药理作用研究进展[J]. 中华中医药杂志, 2016, 31(11): 4653-4657. |



