2. 山东第一医科大学附属省立医院超声科, 济南 250021;
3. 济宁医学院附属医院超声科, 济宁 272029;
4. 济宁医学院附属医院病理科, 济宁 272029
2. Department of Ultrasound, Shandong Provincial Hospital Affiliated to Shandong First Medical University, Jinan 250021, China;
3. Deparment of Ultrasound, Affiliated Hospital of Jining Medical University, Jining 272029, China;
4. Department of Pathology, Affiliated Hospital of Jining Medical University, Jining 272029, China
透明细胞汗腺瘤(clear cell hidradenoma, CCH)[1]是一种起源于汗腺的良性肿瘤,该病较为罕见,常为单发,生长缓慢。好发年龄40~80岁,好发于头颈部,躯干和四肢次之。临床表现为局部皮肤出现表面光滑、质地较韧的结节,少数伴有压痛,可出现色素沉着,部分伴有溃疡或浆液性渗出以致误诊为湿疹或过敏性皮炎,该病首选手术治疗。本研究回顾性分析CCH的高频彩色多普勒超声表现,并结合病理进行分析,寻找有助于临床诊断的超声特征。
1 资料及方法 1.1 临床资料选取2012年4月至2022年10月济宁医学院附属医院经病理证实的CCH患者31例,男14例,女17例,年龄7~69岁,平均(42.9±16.2)岁,病程1个月~8年,平均(4.1±2.9)年。临床均表现为皮肤出现圆形或椭圆形肿物,多突出于皮肤表面,瘤体大小不一,可呈肤色、红色、棕色或蓝色。本研究已通过济宁医学院附属医院伦理委员会审批(2019JYFY-科伦审第17号)。
1.2 仪器与方法采用Siemens S3000(德国SIEMENS公司)、GE Logiq E9(美国GE公司)超声诊断系统,选用高频线阵探头,频率为12~18MHz。患者取合适体位,充分暴露患处后全面扫查,先用二维超声观察肿物边界、形态、内部回声、与周围组织的关系等,测量其大小并记录;然后用彩色多普勒观察血流情况,再根据Adler血流分级标准进行分级[2]。由3名超声浅表专科副主任医师共同分析声像图特征,2名病理学副主任医师进行组织病理学检查。
2 结果 2.1 超声检查结果31例病例所有肿物均为单一病变,肿物位于头面部15例,下肢6例,颈部5例,手掌2例,腰部1例,胸壁2例。31例肿物大小7mm×4mm×3mm~32mm×26mm×21mm,均为边界清晰、形态规则的囊实性结节,其中13例有包膜,18例未见明显包膜;21例以实性为主,10例以囊性为主,13例表现为后方回声增强;其中13例囊性部分透声好,18例囊性部分透声差,8例内见分隔;31例肿物实性部分均可探及血流信号,Adler血流分级为1级6例、2级10例、3级15例,其中19例病变血流频谱为低速高阻、12例为低速低阻(血流峰值流速:10.9~40.3cm/s,血流阻力指数:0.31~0.77);所有肿物周围及区域淋巴结未见肿大。见表 1、图 1。
| 表 1 31例CCH临床与超声图像特征 |
|
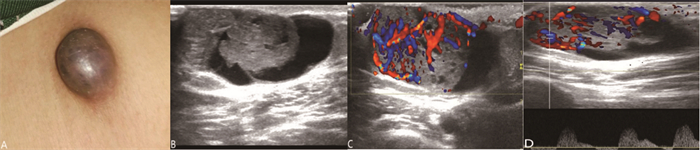
图 1 胸壁CCH临床及超声表现 注:A图示胸壁见一孤立圆形红棕色肿物,突出体表;B图示二维超声显示皮下囊实性回声结节,界清,实性部分呈附壁乳头状,乳头状组织内含有大小不一的囊性回声,呈“囊中有实、实中有囊”声像图表现;C图示超声彩色多普勒显示实性部分及分隔可及丰富血流信号,血流Adler分级3级;D图示超声频谱多普勒显示其动脉呈低速高阻血流频谱。 |
31例肿物术后病理镜下表现:真皮内界限清楚的囊实性结节,实性区呈巢状排列,由位于中央的圆形空泡状透明细胞和位于周边的嗜碱性细胞两种肿瘤细胞构成,两型细胞比例不一。囊性区衬覆立方和柱状细胞,囊腔内可见嗜酸性无定形物质。见图 2。
|
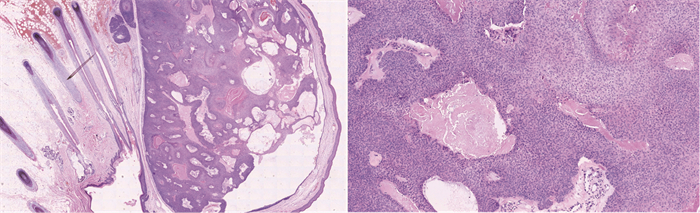
图 2 胸壁CCH病理表现 注:(左)低倍镜下真皮内见界限清楚的囊实性结节(HE,×40);(右)高倍镜下见肿瘤主要由两种细胞组成,位于中央的圆形空泡状透明细胞和位于周边的嗜碱性细胞(HE,×100)。 |
CCH是一种罕见的良性皮肤肿瘤,传统上认为起源于汗腺,又称结节性汗腺瘤、实性囊性汗腺瘤、汗腺顶瘤,仅少数可发生恶变[3]。CCH可发生于任何皮肤部位,多见于头颈部,成年人好发,女性发病率是男性的1.7~2倍。CCH常为单发,生长缓慢,病变皮肤可呈肤色、红色、棕色或蓝色外观,偶见溃疡或浆液性分泌物。其不同的临床表现可能与肿瘤的生长速度、血管分布程度、黏液性物质或内出血充填液体腔的大小和比例有关[4],典型的组织学位置为皮肤真皮层和皮下脂肪层,肿瘤通常被正常的表皮所覆盖[5]。
目前一些检查方法可为CCH的临床诊断提供参考,如皮肤镜检查,CCH表现为淡黄色背景,中央呈黄色无结构区,周围可见点状、线状血管或腔隙样结构,但皮肤镜仅能显示病变表层信息,不能明确显示病变的厚度及边缘[6];MRI对病变穿透能力也是有限的,尤其是较薄的病变无显著优势,且其价格昂贵,更不能提供实时检测。随着超声高频甚至超高频技术的发展,超声检查逐渐应用于皮肤疾病的诊断,高频超声分辨率高,探查范围广,可实时、清晰的显示病变区域累及范围并可重复观察。因CCH临床表现缺乏特异性,目前影像学检查方法难以直接做出明确诊断,仍需通过切除皮损组织病理学检查明确诊断。
CCH病变处表皮正常,肿瘤位于真皮内,可突入皮下脂肪组织,有或无包膜,大体呈囊实性,囊腔内有深红色的浓稠液体;组织病理表现为2种类型比例不定的细胞:其一为嗜碱性多角形小细胞,位于外围,呈嗜碱性;另一为较大的透明或浅染细胞,位于中央,胞浆透明空泡状,故称“透明细胞”[7]。上述两种类型的细胞为其特征性病理表现,两种细胞在肿瘤中比例不一的沿管状囊腔混杂排列,管状囊腔内见无定形蛋白性物质及嗜伊红性物质并充以黏液,肿瘤周围见纤维结缔组织包绕。本研究所有31例肿瘤均见上述2种类型的细胞,2种细胞混杂排列,成分比例不一且有移行区,多以透明细胞为主,另均可见扩张的囊腔结构及其内充填的黏液。免疫组化染色显示肿瘤细胞主要表达上皮源性标记,特别是CK系列包括CK、CK7、CK8、CK14、CK18、CK19等,但CCH的免疫组化缺乏特异性,多数病例仍以HE染色为基础进行病理诊断;另外其PAS染色呈阳性,提示细胞浆淡染的透明细胞富含糖原,可辅助诊断[8]。
本研究31例病例均为单发肿物,平均年龄(42.9±16.2)岁,肿物主要位于头颈部(64.5%,20/31),与文献报道的好发部位一致[8]。本组病例CCH均表现为囊实性结节,边界清晰,形态规则,其边界与形态符合良性肿瘤的超声表现;其中13例有包膜,此超声表现符合病理检查中部分肿瘤可见包膜,或者是肿瘤周边有结缔组织包绕。也有文献报道肿瘤呈实性[9],但本组病例超声表现均呈囊实性,考虑可能与本组检查所采用的探头频率相对较高(12~18MHz),分辨率高,能够检出较细微的囊性成分有关;我们发现本组肿物均为囊实性结节,具有一较大囊腔,实性部分呈附壁乳头状位于囊腔中,同时实性乳头状组织内含有数量众多、大小不一的囊性回声,形成了“囊中有实、实中有囊”的特征性声像图表现,这与其病理学特征相符合;不同肿物囊实性比例不一,本研究中实性为主/囊性为主:21/10,经与病理对比,发现其囊实性成分比例与肿瘤组织中囊腔数量、囊腔扩张程度及黏液含量相关,但与患者年龄、病程及皮损部位无明显相关性。13例表现为后方回声增强,这可能是由于肿物内囊性部分的声束相对于邻近软组织的衰减较低,导致肿物深部软组织出现高回声[4]。13例囊性部分透声好,18例囊性部分透声差,囊性部分的回声可能由于肿瘤中管状囊腔排列不一及出血成分比例差异而不同,而本研究囊性部分透声差者,其病理检查所见囊液中含有陈旧性血液成分较多。彩色多普勒检查所有病例均检出血流,且多数血流丰富,可能是由于肿瘤组织中存在多个血管通道[1],本研究肿瘤可见血流Adler血流分级多为2~3级(80.6%,25/31),考虑肿瘤中的实性附壁结节通常是高血管性的,故多表现为血流丰富;因其血流来自皮肤真皮层动脉(属肢体末端小动脉),因此表现为低速动脉血流。
CCH尽管具有一定特征性高频超声表现,仍需与以下疾病相鉴别:1)表皮样囊肿。该囊肿分布位置广泛,超声显示病变边界清晰,形态规则,内部呈囊性回声,多数透声较差,后方回声增强,内无血流,囊壁可及少量血流。病理显示囊壁由复层鳞状上皮组织构成,可及纤维结缔组织包绕,囊内为无结构红染物[10];2)毛根鞘囊肿。好发于毛发茂盛的区域,超声表现为皮下低回声结节,形态规则,内可及液性暗区及斑块状钙化,多无血流信号。病理下为真皮内囊肿样结构,囊壁由多层鳞状上皮细胞组成,囊腔内容物为角化物[11];3)皮脂腺囊肿。常表现为头面部、臀部、背部结节,超声表现为边界清晰的囊性回声,囊壁较厚,内充满细密点状回声,合并感染时囊腔顶端局部呈蒂状向皮肤表面突出,囊腔内无明显血流信号[12];4)皮肤血管瘤。多见于婴幼儿,皮肤表面可见鲜红色微隆起,高频超声下可及低回声或不均质回声高血管性实性病变,内血流信号丰富[13];5)基底细胞癌。好发于头面部,常为褐灰色质硬结节,多为形状不规则的低回声区,在超声上可见特征性高回声斑点[14]。6)恶性CCH。可原发为恶性,也可从良性CCH恶变而来[15],瘤体以实体生长,体积较大,坚硬而固定,无包膜,与周围组织分界不清。超声显示其呈实性,边界不清,与良性CCH呈囊实性不同。病理显示以透明细胞为主,常无腺腔形成,浸润表皮及其他组织,常见坏死,可见细胞异型性和核分裂象[8]。
CCH的治疗首选手术切除,重点是实现肿瘤的完全切除,当肿瘤累及深层脂肪组织或切除不完整时,易复发。本研究所有病例术后随访至今均未发生局部复发。
利益冲突:所有作者均申明不存在利益冲突。
| [1] |
Lee JY, Kang BS, Shim HS, et al. Clear cell hidradenoma: characteristic imaging features on ultrasonography, computed tomography, and magnetic resonance imaging[J]. J Ultrasound Med, 2018, 37(8): 1993-2001. DOI:10.1002/jum.14552 |
| [2] |
Adler DD, Carson PL, Rubin JM, et al. Doppler ultrasound color flow imaging in the study of breast cancer: preliminary findings[J]. Ultrasound Med Biol, 1990, 16(6): 553-559. DOI:10.1016/0301-5629(90)90020-d |
| [3] |
Demirci GT, Atis G, Altunay IK, et al. A giant benign clear cell hidradenoma on the anterior trunk[J]. Dermatol Reports, 2011, 3(3): e45. DOI:10.4081/dr.2011.e45 |
| [4] |
Wortsman X, Reyes C, Ferreira-Wortsman C, et al. Sonographic characteristics of apocrine nodular hidradenoma of the skin[J]. J Ultrasound Med, 2018, 37(3): 793-801. DOI:10.1002/jum.14379 |
| [5] |
Jin W, Kim GY, Lew BL, et al. Sonographic findings of an eccrine spiradenoma: case report and literature review[J]. J Ultrasound Med, 2008, 27(5): 813-818. DOI:10.7863/jum.2008.27.5.813 |
| [6] |
Yoshida Y, Nakashima K, Yamamoto O. Dermoscopic features of clear cell hidradenoma[J]. Dermatology, 2008, 217(3): 250-251. DOI:10.1159/000148253 |
| [7] |
童咏花, 谢蒙, 孙艳虹, 等. 透明细胞汗腺瘤[J]. 临床皮肤科杂志, 2021, 50(2): 85-86. DOI:10.16761/j.cnki.1000-4963.2021.02.006 |
| [8] |
薛霜, 史立纲, 张梦阳, 等. 透明细胞汗腺瘤3例临床病理分析[J]. 肿瘤基础与临床, 2015(4): 335-336. DOI:10.3969/j.issn.1673-5412.2015.04.022 |
| [9] |
郑庆虎, 于蕊, 周欣, 等. 透明细胞汗腺瘤[J]. 临床皮肤科杂志, 2012, 41(9): 545-546. DOI:10.3969/j.issn.1000-4963.2012.09.013 |
| [10] |
王子, 王曦曦, 朱强, 等. 超声影像在皮肤病变诊断中的应用研究[J]. 中华医学超声杂志(电子版), 2019, 16(6): 407-418. DOI:10.3877/cma.j.issn.1672-6448.2019.06.002 |
| [11] |
刘佩佩, 张翠平, 何萍, 等. 高频超声在外毛根鞘囊肿诊断中的价值[J]. 中国超声医学杂志, 2019, 35(3): 266-268. DOI:10.3969/j.issn.1002-0101.2019.03.023 |
| [12] |
轩维锋, 张红环, 陈祎. 皮脂腺囊肿的超声诊断[J]. 临床超声医学杂志, 2007, 100(8): 498-500. DOI:10.16245/j.cnki.issn1008-6978.2007.08.013 |
| [13] |
Wortsman X. Common applications of dermatologic sonography[J]. J Ultrasound Med, 2012, 31(1): 97-111. DOI:10.7863/jum.2012.31.1.97 |
| [14] |
王诗琪, 刘洁, 朱庆莉, 等. 皮肤高频超声和皮肤镜在基底细胞癌术前精确评估中的应用[J]. 中华皮肤科杂志, 2020, 53(1): 51-55. DOI:10.35541/cjd.20190243 |
| [15] |
惠海英, 吴娜, 孙晶莹, 等. 恶性透明细胞汗腺瘤一例[J]. 中华皮肤科杂志, 2017, 50(2): 90. DOI:10.3760/cma.j.issn.0412-4030.2017.02.004 |



