光致变色化合物在特定光照的条件下,其颜色、光化学和光物理性质(吸收光谱、荧光光谱、折射指数等)均会发生显著变化,且这种变化一般是可逆的[1-2]。上述独特性能,使光致变色化合物在有机光储存、分子开关、逻辑门、生物医学等领域具有广泛的应用前景[3]。
目前,已发现的光致变色化合物种类繁多,然而研究较为广泛的光致变色化合物有10种左右,具体有二芳基乙烯类光致变色化合物[4-5]、偶氮苯类光致变色化合物[6]、螺吡喃类光致变色化合物[7]、供体-受体斯坦豪斯加合物[8]、六芳基二咪唑基化合物[9-10]等。
其中,二芳基乙烯类光致变色化合物作为典型的T-型光致变色化合物[4-5],具有合成方法简单、光致异构化反应抗疲劳性强、开闭环异构体热稳定性好等显著特点而引起科学家的广泛关注[11-13]。
二芳基乙烯是指1, 1-二芳基取代的乙烯衍生物。因此,可以将其拆分成两个相对独立的结构单元:中心的乙烯桥结构和两侧的芳香杂环[14]。同时,根据乙烯桥两侧芳香杂环的异同,可将二芳基乙烯类光致变色化合物分为对称型二芳基乙烯类光致变色化合物和不对称型二芳基乙烯类光致变色化合物[15]。显而易见,无论从化合物分子结构设计还是有机化学合成方面,不对称型二芳基乙烯类光致变色化合物要比对称型二芳基乙烯类光致变色化合物略显复杂。相反,不对称型二芳基乙烯类光致变色化合物却在光致异构化反应、光化学性质等方面展现出独特的性能优势。因此,不对称型二芳基乙烯类光致变色化合物的研发具有重要的意义。
基于此,本研究以苯并噻吩为烯桥,以2-苯基噻唑和萘为侧链,设计并合成出两个新型不对称型二芳基乙烯类光致变色化合物,通过光化学性质测试和分析,探究其光致异构化性能和应用前景。
1 材料与方法 1.1 试剂四氢呋喃99.50%(批号:MDHR4DAE)购自萨恩化学技术(上海)有限公司;四(三苯基膦)钯99%(批号:M9PNRV8Q)购自萨恩化学技术(上海)有限公司;碳酸钠(批号:MYDR2EZK)购自萨恩化学技术(上海)有限公司;色谱正己烷(批号:M8EDRH6X)购自萨恩化学技术(上海)有限公司;色谱乙腈(批号:1MRCRRKE)购自萨恩化学技术(上海)有限公司;色谱甲醇(批号:F3EQRRUG)购自萨恩化学技术(上海)有限公司。
1.2 仪器旋转蒸发仪(上海爱朗仪器有限公司,OSB-2100);磁力搅拌器(上海梅颖浦仪器仪表制造有限公司,MYP13-2s);油浴锅(郑州长城科工贸有限公司,HWCL-1);低温冷却液循环泵(郑州长城科工贸有限公司,DLSB-10/30);紫外-可见分光光度计(岛津企业管理(中国)有限公司,UV-2450)等。
1.3 方法具体合成方法如图 1所示。

|
图 1 目标化合物的合成路线 |
化合物4、化合物6、化合物7和化合物9的合成可参考已发表文献进行合成[16-19]。
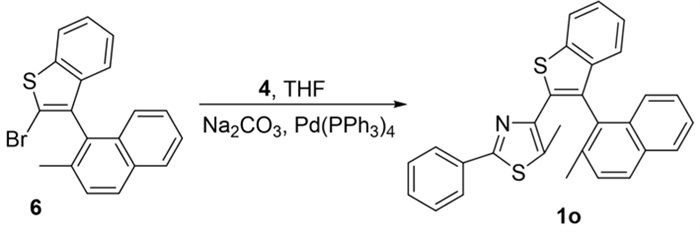
1) 化合物1o的合成
|
图 2 化合物1o的合成 |
在氮气保护下,将化合物4(0.11g,0.31 mmol),四三苯基膦钯(0.028g,0.024mmol)加入反应瓶中。加入Na2CO3水溶液(2mol/L),化合物6(0.10g,0.34mmol),和四氢呋喃(3mL)后,将上述体系置于68℃油浴中加热反应24h。待反应完全后,将体系冷却至室温。体系中加入适量蒸馏水后,并用乙酸乙酯萃取3次,合并有机相,减压旋蒸。通过柱层析对所得粗品进行分离提纯(展开剂:石油醚∶乙酸乙酯=200 ∶1),得到淡紫色固体0.059g,收率为46.46%。
1H NMR (400MHz, CDCl3), δ: 2.45(s, 3H), 2.78(s, 3H), 7.33(m, 1H), 7.52(m, 7H), 8.01(m, 5H), 8.56(m, 2H)。
2) 化合物2o的制备

|
图 3 化合物2o的合成 |
在氮气保护下,将化合物7(0.090g,0.28 mmol),四(三苯基膦)钯(0.026g,0.022mmol)加入反应瓶中。加入Na2CO3水溶液(2mol/L),化合物9(0.11g,0.34mmol)和四氢呋喃(3mL)后,将上述反应体系置于68℃油浴中加热反应24h。待反应完全后,将体系冷却至室温。体系中加入适量蒸馏水后,用乙酸乙酯萃取3次,合并有机相,减压旋蒸。通过柱层析对所得粗品进行分离提纯(展开剂:石油醚∶乙酸乙酯=300 ∶1),得到淡黄色固体0.082g,收率为64.57%。
1H NMR (400MHz, CDCl3), δ: 2.40(s, 3H), 2.76(s, 3H), 7.29(m, 1H), 7.54(m, 7H), 8.03(m, 5H), 8.43(m, 1H), 8.92(m, 1H).
1.4 目标产物光化学性质测定用不同极性的色谱纯溶剂(色谱甲醇、色谱乙腈、色谱正己烷),将目标光致变色化合物1o和2o配成相应浓度的样品溶液,采用紫外-可见分光光度计对目标光致变色化合物进行光化学性质测试。测定目标光致变色化合物的摩尔吸光系数及其在光照条件下的紫外可见吸收光谱图变化。
2 结果与讨论 2.1 目标光致变色化合物的紫外可见吸收光谱图利用紫外-可见分光光度计对目标变色化合物1o和2o进行紫外可见吸收光谱测定。
由图 4所示,光致变色化合物1o在色谱甲醇、色谱乙腈和色谱正己烷溶液中的最大吸收波长分别为293nm、300nm和293nm。同时,光致变色化合物2o在色谱甲醇、色谱乙腈和色谱正己烷溶液中的最大吸收波长分别为294nm、293nm、296nm。由此可知,具有不对称结构的两个二芳基乙烯类光致变色化合物1o和2o,虽然其侧链的两个官能团与苯并噻吩烯桥的连接位点不同,但是其相似的π共轭体系,使上述两个光致变色化合物在不同极性溶剂中具有相似的最大吸收波长。此外,两个目标光致变色化合物分别在不同极性溶剂中显示出的相似的最大吸收波长证实其紫外-可见吸收光谱受溶剂极性影响较小,因此, 其在不同极性溶剂中展现出相似的光谱性质。

|
图 4 化合物1o(上)和2o(下)的紫外可见吸收光谱图 注:a.色谱甲醇;b.色谱乙腈;c.色谱正己烷 |
在同一波长处,随着化合物1o和2o在溶液中浓度的升高,化合物的吸光度也呈线性增长趋势。根据朗伯-比尔定律计算可知,光致变色化合物1o和2o在不同极性溶剂中的摩尔吸光系数〔1o: ε=21000L/(mol·cm); 2o: ε=20000L/(mol·cm)〕并无显著差别,由此进一步证实两个化合物的光谱性质受溶剂影响较小。
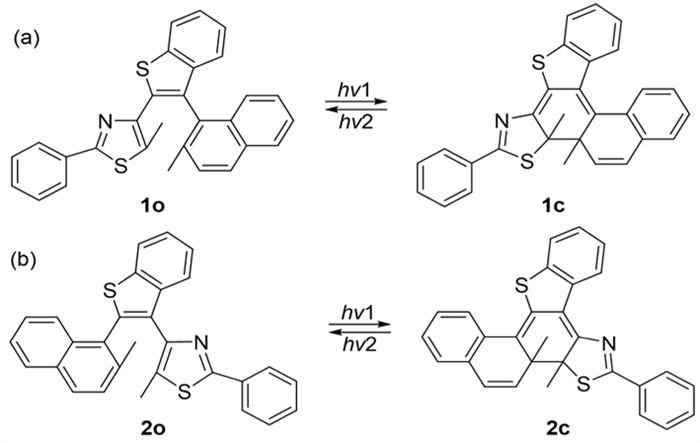
2.2 目标光致变色化合物的光致异构化反应光致变色化合物1o和2o在特定光照条件下的光致异构化反应如图 5所示。
|
图 5 化合物1o和2o的光致异构化反应示意图 |
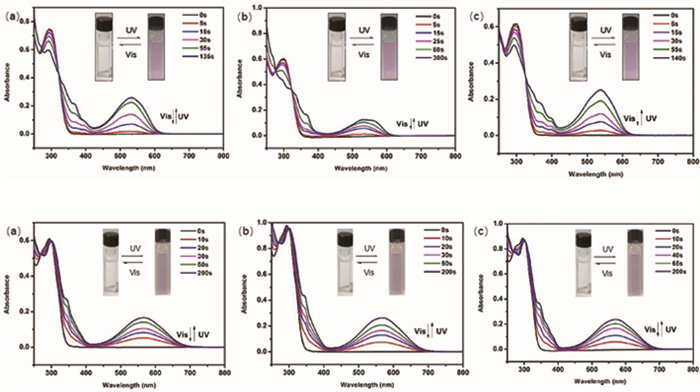
在特定光照的条件下(λ = 254 nm),光致变色化合物1o和2o的紫外-可见吸收光谱图均发生了显著变化(图 6),由此证明在光照条件下,化合物1o和2o均发生了如图 5所示的光致异构化反应,也进一步证实通过图 1所示的合成路线得到了目标光致变色化合物。
|
图 6 化合物1o(上)和2o(下)在光照条件下的紫外可见吸收光谱图 注:a.色谱甲醇;b.色谱乙腈;c.色谱正己烷 |
在紫外光照下,化合物1o的溶液颜色由无色变为粉红色,紫外-可见光谱在可见光区出现新的吸收峰,并且其最大吸收波长为532 nm,而其在紫外光区(< 250 nm)的吸收强度出现一定程度的下降,并在327 nm处出现一个等色点,说明上述体系存在开闭环两种异构体。在可见光的照射下,溶液颜色又变为无色,同时其吸收光谱也变为初始的状态。
光致变色化合物2o在光照条件下显示出和化合物1o类似的光化学性质。即在紫外光(λ = 254 nm)照射下,化合物溶液由无色变为紫红色,紫外-可见吸收光谱变化与化合物1o相似,其在可见光区的最大吸收波长为566 nm,等色点位于275 nm处。在可见光的照射下,化合物的溶剂颜色也同样变为无色,吸收光谱也变为初始的状态。
紫外光照后,目标化合物在可见光区有显著吸收的原因是,经紫外光照后,化合物均由开环异构体1o和2o分别变为闭环异构体1c和2c。随着其开闭环异构体的变化,化合物的π共轭长度也发生了显著的变化,从而导致其溶液颜色和吸收光谱的显著变化。相似的光谱性质变化则是源于两个化合物在光照前后相似的化学结构变化。
2.3 目标光致变色化合物的抗疲劳性测试一般来说,二芳基乙烯类光致变色化合物具有很强的抗疲劳性,即通过反复光致异构化反应或长时间光照后,其吸收光谱不会发生显著变化,也就是说体系中不会产生其他副产物。
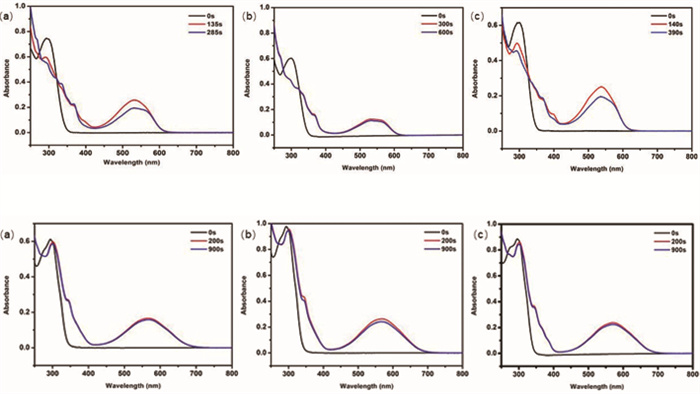
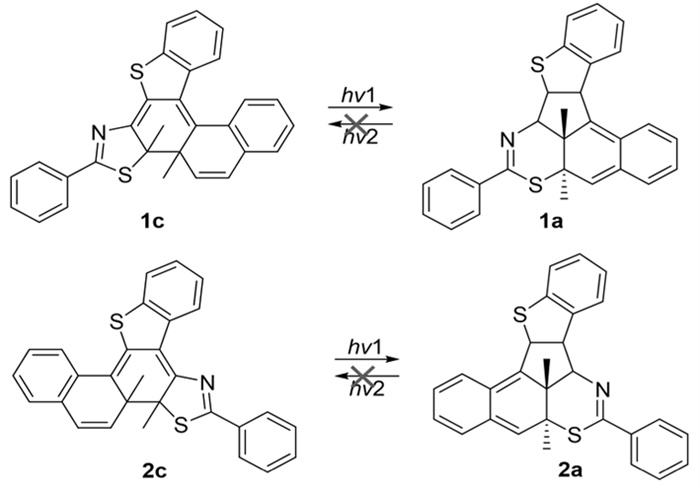
然而,化合物1o和2o在长时间的光照条件下,其闭环异构体1c和2c在可见光区的吸收强度在不同溶剂中均出现不同程度的下降(图 7)。产生该现象的主要原因是长时间的光照,会使其闭环异构体分别生成一个含有五元环的副产物1a和2a(图 8),该含有五元环的副产物因分子内没有显著的长π共轭体系,因此其在可见光区没有显著吸收,这也是通过长时间光照后,两个化合物在可见光区的吸收强度呈现不同程度的下降的原因。该副产物在光照条件下不能发生光致异构化反应,即在光照条件下既不能生成闭环异构体,也不能生成开环异构体。
|
图 7 化合物1c(上)和2c(下)长时间(t=900s)光照后的紫外可见吸收光谱图 注:a.色谱甲醇;b.色谱乙腈;c.色谱正己烷 |
|
图 8 化合物1c和2c经长时间光照后的副反应示意图 |
虽然目标光致变色化合物的抗疲劳性较差,进而使其在诸如光学分子开关等特定领域的应用受到一定的局限性,但是其副产物1a和2a的稳定性和反应的不可逆性也使其在不可擦除的光记录材料和光储存器件等领域具有广泛的应用前景。
3 结论本文以二芳基乙烯结构为骨架,设计了以苯并噻吩为烯桥,以萘和噻唑为侧链的不对称型二芳基乙烯类光致变色化合物1o和2o。通过光化学性质测试可知,上述两个目标光致变色化合物均具有良好的光致变色性能。同时,目标光致变色化合物较弱的抗疲劳性,使其在不可擦除的光记录和光储存器件领域具有广泛的应用前景。
利益冲突:所有作者均申明不存在利益冲突。
| [1] |
郭洁芬, 赵喜玲, 曹喜云, 等. 光致变色材料的制备、性能及变色机理[J]. 化学工程师, 2021, 35: 57-60. DOI:10.16247/j.cnki.23-1171/tq.20210957 |
| [2] |
Feringa BL, Browne WR. Molecular switches[M]. Second Edition. Wiley-VCH, Weinheim, Germany, 2011.
|
| [3] |
Tian H, Zhang J. Photochromic materials: preparation, properties and applications[M]. Wiley-VCH, Weinheim, Germany, 2016: 36.
|
| [4] |
Irie M. Diarylethenes for memories and swithches[J]. Chem Rev, 2000, 100(5): 1685-1716. DOI:10.1021/cr980069d |
| [5] |
Irie M, Fukaminato T, Matsuda K, et al. Photochromism of diarylethene molecules and crystals: memories, switches, and actuators[J]. Chem Rev, 2014, 114(24): 12174-12277. DOI:10.1021/cr500249p |
| [6] |
Dong L, Feng Y, Wang L, et al. Azobenzene-based solar thermal fuels: design, properties, and applications[J]. Chem Soc Rev, 2018, 47: 7339-7368. DOI:10.1039/C8CS00470F |
| [7] |
Berkovic G, Krongauz V, Weiss V. Spiropyrans and spirooxazines for memories and switches[J]. Chem Rev, 2000, 100: 1741-1754. |
| [8] |
Lerch MM, Szymański W, Feringa BL. The (photo)chemistry of stenhouse photoswitches: guiding principles and system design[J]. Chem Soc Rev, 2018, 47(6): 1910-1937. DOI:10.1039/c7cs00772h |
| [9] |
Hayashi T, Maeda K. Preparation of a new phototropic substance[J]. Bull Chem Soc Jpn, 1960, 33(4): 565-566. DOI:10.1246/bcsj.33.565 |
| [10] |
Hayashi T, Maeda K. Mechanism of chemiluminescence of 2, 4, 5-triphenyl-imidazole[J]. Bull Chem Soc Jpn, 1962, 35(12): 2057-2058. DOI:10.1246/bcsj.35.2057 |
| [11] |
肖建森, 徐汤泽钰, 邓霏. 二芳基乙烯的发展和应用[J]. 广东化工, 2021, 48(13): 90-91. DOI:10.3969/j.issn.1007-1865.2021.13.040 |
| [12] |
朱世琴, 李萌祺, 朱为宏. 有机光致变色二芳基乙烯染料的发展动态[J]. 自然杂志, 2018, 40(2): 79-89. DOI:10.3969/j.issn.0253-9608.2018.02.001 |
| [13] |
林伟豪, 张钦发, 刘蔚, 等. 热稳定型有机光致变色材料研究进展[J]. 新型工业化, 2021, 11(11): 19-21. DOI:10.19335/j.cnki.2095-6649.2021.11.008 |
| [14] |
朱世琴, 李文龙, 朱为宏. 新型烯桥二芳基乙烯光致变色体系[J]. 化学进展, 2016, 28(7): 975-992. DOI:http://dx.doi.org/1005-281X(2016)07-0975-18.
|
| [15] |
李贵珍. 新型非对称二芳基乙烯类化合物的合成及其光谱性质研究[D]. 天津: 河北工业大学, 2006.
|
| [16] |
Li R, Nakashima T, Galangau O, et al. Photon-quantitative 6π-electrocyclization of a diarylbenzo[b]thiophene in polar medium[J]. Chem Asian J, 2015, 10: 1725-1730. DOI:10.1002/asia.201500328 |
| [17] |
Li R, Nakashima T, Kanazawa R, et al. Efficient self-contained photoacid generator system based on photochromic terarylenes[J]. Chem Eur J, 2016, 16250-16257. DOI:10.1002/chem.201603768 |
| [18] |
Li R, Nakashima T, Kawai T. Self-contained photoacid generator system for super acid based on photochromic terarylene[J]. Chem Commun, 2017, 53: 4339-4341. DOI:10.1039/c7cc01635b |
| [19] |
Galangau O, Delbaere S, Ratel-Ramond N, et al. Dual photochemical bond cleavage for a diarylethene-based phototrigger containing both methanolic and acetic sources[J]. J Org Chem, 2016, 81(22): 11282-11290. DOI:10.1021/acs.joc.6b02256 |



