随着冠心病发病率逐年上升,冠状动脉病变的影像学评估和检查方法也越来越多,包括冠状动脉CT(CTA), 冠状动脉造影(coronory arteriography,CAG), 血管内超声(intravenous ultrasound,IVUS), 光学相干断层扫描(optical coherence tomography,OCT)[1-3],曾作为冠心病诊断的“金标准”CAG表现出越来越多的局限性,尤其是在多支冠脉临界病变介入治疗的策略选择中。冠状动脉多支临界病变指的是3支冠状动脉中至少2支狭窄程度目测介于40%~70%的狭窄病变,冠状动脉临界病变进行血运重建一直存在争议,仅按照CAG显示的血管狭窄程度来判断是否需要介入血运重建存在很多限制,CAG只能提供冠状动脉血管形态学上的信息,不能进行生理功能学上的有效评估,临床上并非所有狭窄>70%的血管均需治疗,狭窄<70%的血管无须治疗,仅凭借CAG提供的血管狭窄程度进行支架植入术治疗,有可能导致过度治疗或治疗不足。
冠状动脉生理功能性评估的发展有效地弥补了冠状动脉造影在功能学评估上的不足。研究证明,与冠状动脉解剖学评估相比,冠状动脉功能学评估提高了患者的临床收益[4-6],现在国际上公认的能够提供冠状动脉功能学参数的“金标准”血流储备分数(fractional flow reserve,FFR)[7-10]也表现出一定的局限性。FFR检查需要压力导丝,该导丝检查过程中需要为患者注射药物,费用高,手术时间相对较长。定量血流分数(quantitative flow ratio,QFR)是一种无须压力导丝的无创功能学评估方法。本研究探索在冠脉血管多支临界病变中应用QFR优化指导经皮冠状动脉介入治疗(PCI)的作用及价值。
1 资料与方法 1.1 临床资料选取2020年10月至2021年4月在济宁医学院附属医院介入手术室行冠状动脉多支临界病变(均经CAG证实)介入治疗患者270例,其中男性188例,女性82例,年龄在41~82岁,平均年龄62.8岁,其中合并高血压125例,糖尿病112例,吸烟史112例。所有患者均无严重左主干病变及严重钙化病变,无手术禁忌证,所有患者均拒绝搭桥。符合条件的270例患者随机分成3组,QFR指导组90例,201处病变,行QFR分析;IVUS指导组90例,198处病变,行IVUS检查;CAG指导组90例,191处病变,均不做QFR分析和IVUS检查。见表 1。本研究经医院伦理委员会批准,征得家属同意并签署知情同意书。
| 表 1 3组患者一般情况比较 |
3组患者分别于术前化验血常规、肾功能、血脂、血糖、出凝血指标,并行超声心动图检查,术前与术后均给予抗血小板与调脂治疗。
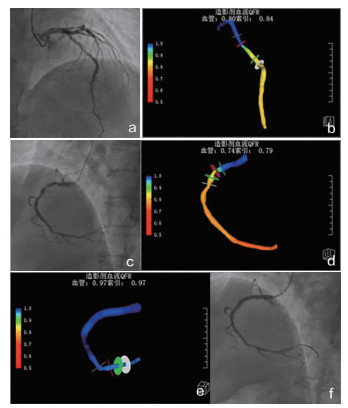
1.2.1 QFR指导组采用设备为博动医学影像科技(上海)有限公司生产的第二代QFR系统,采用离线QFR测量平台(版本Angio Plus1.01),对入组的多支临界病变行标准QFR分析。具体操作如下: 1)选取目标血管投照体位>25°的造影体位2个; 2) 尽量选择舒张末期且血管显示充分的投照体位用于分析(开口病变及存在肌桥的血管除外); 3) 标记血管同一位置并进行严证,选择血管远端;4) 形成血管轮廓生成目标血管三维图像; 5)选择血管行TIMI数帧; 6)基于三维模型及流体动力学原理测量QFR值[11]。对QFR<0.80的血管行PCI,所选择支架型号均严格按照系统推荐的残余QFR≥0.90的标准选择支架型号,术后再次进行QFR分析,残余QFR≥0.90者结束手术。通过CAG认定临界病变的狭窄经QFR分析后得出不同的结果,前降支QFR值0.8,未行PCI, 右冠状动脉QFR值0.74,行PCI, 植入3.0*28支架一枚,术后QFR值0.97(图 1)。
|
图 1 冠脉多支病变患者QFR评估结果 注:a. LAD造影中段75%狭窄; b. LAD QFR 0.8,未与治疗; c. RCA造影近中段80%狭窄; d. RCA QFR 0.74, 支架治疗; e. RCA支架术后QFR 0.97; f. RCA支架后造影无残余狭窄 |
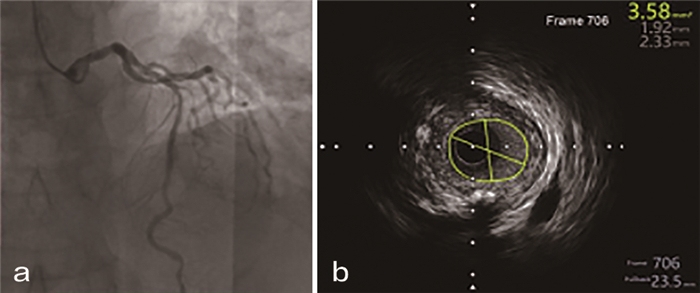
所用设备为波士顿科学(美国)生产的ILAB ULtrasound Imaging System,所用导管为波士顿科学(美国)生产的OptisCross 40MHz超声导管。肝素抗凝和冠脉内推注硝酸甘油,超声导管常规排气后将2.9F OptisCross 40MHz超声导管沿工作导丝送入病变远端5~10mm处,采用自动回撤装置回撤,回撤速度为1mm/s, 超声导管进入左右冠状动脉指引导管后结束回撤。术后由同一技师对所采集的IVUS图像严格按照2018版血管内超声中国专家共识进行解读,对血管直径<3.0mm的血管, 最小管腔面积(MLA)<2.4mm2、血管直径>3.0mm的血管, 最小管腔面积(MLA)<2.8mm2的血管进行支架干预,支架近端及远端参考(落脚点)优先选择正常管腔,对于弥慢性病变选择斑块负荷≤50%处为支架落脚点,术后再次行IVUS检查,支架边缘3mm内无夹层、血肿,支架贴壁良好,膨胀完全(术后MSA≥5mm2),无明显组织脱垂,支架后造影血流TIMI 3级结束手术。目测临界病变的血管经IVUS检查后MLA 3.58mm2,未植入支架(图 2)。
|
图 2 前降支近端造影临界狭窄,IVUS测量MLA无须干预 注:a. LAD近中段75%左右狭窄(CAG显示); b. IVUS测量狭窄处MLA3.58,未予治疗 |
所有手术均在PHILIPS FD20设备上完成冠脉造影,由术者对CAG结果进行评估,对狭窄程度>70%的狭窄血管行支架植入术,支架型号由术者依据经验进行选择,术后造影显示无明显夹层及残余狭窄,血流TIMI 3级后结束手术。
1.3 观察指标3组不同方法指导下的多支临界病变患者的支架置入个数、手术花费、随访12月复发心绞痛及主要心血管事件(MACE)的发生率。
1.4 统计学分析方法采用SPSS24.0软件进行统计分析,采用Pearson卡方、Fisher精准概率、单因素方差分析进行三组间比较。P<0.05为差异有统计学意义。
2 结果 2.1 一般资料3组患者性别、年龄、高血压史、糖尿病史、吸烟史等对比无统计学意义(P>0.05)。见表 1。
2.2 3组患者支架置入数目、医疗花费、术后12月复发心绞痛情况QFR指导组植入支架91枚,人均植入1.01枚;IVUS指导组植入支架115枚,人均植入1.28枚;CAG指导组植入支架134枚,人均植1.49枚;QFR指导组置入支架总数少于IVUS指导组和CAG指导组(P<0.001),QFR指导组手术花费少于IVUS指导组和CAG指导组(P<0.001)。见表 2。
| 表 2 3组患者支架植入个数、医疗花费、复发心绞痛、MACE比较 |
CAG对冠状动脉狭窄程度的评估具有一定的局限性,而多角度投照也只能对偏心病变的评估具有一定的补充作用,对重构血管、临界病变、多支病变尤其是罪犯血管的评估其局限性更加明显。CAG对血管狭窄是否引起心肌缺血不能进行有效评估,冠状动脉多支病变患者仅凭CAG常规结果进行PCI干预,可能会增加支架置入的个数,增加手术时间及造影剂用量,同时增加患者的手术花费,过多支架的置入还会增加支架内血栓及再狭窄的风险,影响患者的远期预后等。
IVUS相对于CAG可更好地评估冠状动脉狭窄程度, 可依据目标血管管腔最小面积(MLA)作为评价心肌是否缺血的标准,还可以观察血管内部的斑块分布、斑块性质及斑块负荷的识别,同时可以明确血管是否存在负性重构,因为有些造影上看到的狭窄实际上是血管的负性重构,可有效地减少支架置入数量[12]。IVUS可在术中指导支架型号的选择及支架近端远端参考管腔的选择,还可以有效评估支架的贴壁及膨胀情况,降低术后支架内血栓形成及再狭窄的概率。另外IVUS的检查需要增加额外一次性耗材,而且IVUS仅通过单一的最小管腔面积(MLA)作为评价心肌缺血的标准是不够的,IVUS只能显示冠状动脉的病变解剖及影像学分析,不能提供功能学评估。
近年来,冠状动脉功能学评估指导下的经皮冠状动脉介入术越来越受到重视,冠状动脉血流储备分数(FFR)作为评估冠状动脉病变生理学意义的“金标准”,可识别是否有必要行冠状动脉血运重建治疗,已被写入各项PCI指南, 用于指导临床实践[13],已证实FFR指导PCI术治疗可降低支架植入数目,并改善患者预后。鉴于FFR的测定需要特定的压力导丝,置入冠状动脉狭窄病变远端,同时需要药物激发冠状动脉最大血流,操作导丝的并发症(血管痉挛、夹层)、费用高、操作复杂等因素限制了临床应用[11]。新型无创的冠状动脉生理功能学评估方法—定量血流分数(QFR)的出现和应用弥补了FFR的一些不足,QFR基于造影图像计算机三维定量分析(3D-QCA),不需要压力导丝检测,不需要药物激发最大冠状动脉血流,FAVOR study[14]研究表明QFR诊断准确率在患者水平和血管水平分别为92.4%和92.7%,QFR作为一项新型的冠状动脉病变生理学功能评估技术,在评估中度狭窄病变的血流动力学意义中与传统FFR具有良好的一致性,但临床可操作性更强、费用低[15-17]。本研究结果显示,QFR指导组的植入支架数明显少于CAG指导组和IVUS指导组,而IVUS指导组和CAG指导组相比无统计学意义;QFR指导组的手术费用明显低于CAG组和IVUS指导组,而IVUS指导组因一次性耗材费用略高。这说明在QFR的帮助下,可以减少支架的植入数量及患者的手术费用,同时我们在后期的随访中发现患者的卒中、血栓形成、死亡及血运重建在内的临床事件。在后期的研究中,我们将加大样本量,以期取得更为可靠的研究证据。本研究中QFR指导的冠状动脉多支病变的介入治疗,是3组中支架置入总数及单支血管置入支架平均数最少且复发心绞痛最少的,QFR术前可有效地评估心肌缺血程度并有效识别罪犯血管,减少不必要的支架置入及各种器械耗材的使用,减少了手术时间,降低了医疗成本。术中可依据残余QFR值指导支架型号的选择,避免漏掉血管段的干预,也是术后复发心绞痛少的原因之一,并可及时评估术后功能学改变。
综上所述,QFR可用于冠状动脉多支临界病变患者PCI的指导, 术中精确进行冠状动脉功能学评估,在精准医疗的背景下减少支架置入的数量,从而使血运重建率显著减低,并可明显降低术后复发心绞痛的数量。
利益冲突:所有作者均申明不存在利益冲突。
| [1] |
张晓娇, 侯爱洁, 罗德锋, 等. 基于血流储备分数标准评估冠状动脉CT、血管内超声、冠状动脉造影定量分析在中重度病变的诊断价值[J]. 中国循证心血管医学杂志, 2018, 10(9): 1070-1073. DOI:10.3969/j.issn.1674-4055.2018.09.10 |
| [2] |
刘帅, 林闽江, 许亚飞. 冠状动脉CT血管造影定量分析预测冠心病患者心血管事件风险的价值[J]. 中华全科医学, 2019, 17(8): 1320-1322, 1407. DOI:10.16766/j.cnki.issn.1674-4152.000933 |
| [3] |
王萍, 龙滔, 邵江. 两种血清标志物联合24 h动态心电图对老年冠心病并发无症状心肌缺血的诊断价值[J]. 中华老年心脑血管病杂志, 2020(9): 934-937. DOI:10.3969/j.issn.1009-0126.2020.09.010 |
| [4] |
Yang HM, Tahk SJ, Lim HS, et al. Relationship between intravascular ultrasound parameters and fractional flow reserve in intermediate coronary artery stenosis of left anterior descending artery: intravascular ultrasound volumetric analysis[J]. Catheter Cardiovasc Interv, 2014, 83(3): 386-394. DOI:10.1002/ccd.25088 |
| [5] |
Safi M, Mehrabi MA, Alipour PS, et al. The role of FFR in clinical decision making in patients with moderate coronary lesions: a pilot study[J]. Acta Biomed, 2018, 89(3): 378-381. DOI:10.23750/abm.v89i3.5605 |
| [6] |
Shiono Y, Kubo T, Tanaka A, et al. Long-term outcome after deferral of revascularization in patients with intermediate coronary stenosis and gray-zone fractional flow reserve[J]. Circ J, 2015, 79(1): 91-95. DOI:10.1253/circj.CJ-14-0671 |
| [7] |
Nakamura M, Yamagishi M, Ueno A, et al. Prevalence of visual-func-tional mismatch regarding coronary artery stenosis in the CYIT-DEFER registry[J]. Cadiovasc Interv Ther, 2014, 29(2): 300-308. DOI:10.1007/s12928-014-0259-3 |
| [8] |
惠波, 邵一兵, 刘玉昊, 等. 血管内超声与血流储备分数在冠状动脉多支病变中的应用比较[J]. 中国临床研究, 2020, 33(5): 646-649. DOI:10.13429/j.cnki.cjcr.2020.05.018 |
| [9] |
Mejía-Rentería H, Nombela-Franco L, Paradis JM, et al. Angiography-based quantitative flow ratio versus fractional flow reserve in patients with coronary artery disease and severe aortic stenosis[J]. EuroIntervention, 2020, 16(4): e285-285e292. DOI:10.4244/EIJ-D-19-01001 |
| [10] |
Parikh V, Agnihotri K, Kadavath S, et al. Clinical application of fractional flow reserve-guided percutaneous coronary intervention for stable coronary artery disease[J]. Curr Cardiol Rep, 2016, 18(4): 32. DOI:10.1007/s11886-016-0711-3 |
| [11] |
Tu S, Westra J, Yang J, et al. Diagnostic accuracy of fast computational approaches to derive fractional flow reserve from diagnostic coronary angiography: the international multicenter FAVOR pilot study[J]. JACC Cardiovasc Interv, 2016, 9(19): 2024-2035. DOI:10.1016/j.jcin.2016.07.013 |
| [12] |
李梦寰, 柳杨, 何源, 等. 利用血管内超声结果验证定量血流分数对冠状动脉造影临界病变诊断价值的研究[J]. 中国循环杂志, 2020, 35(6): 546-555. DOI:10.3969/j.issn.1000-3614.2020.06.005 |
| [13] |
袁圆, 张奇. 定量血流分数的临床研究及应用进展[J]. 国际心血管病杂志, 2020, 47(1): 19-22. DOI:10.3969/j.issn.1673-6583.2020.01.005 |
| [14] |
Kanaji Y, Murai T, Lee T, et al. Efficacy of pressure parameters obtained during contrast medium-induced submaximal hyperemia in the functional assessment of intermediate coronary stenosis in comparison with instantaneous wave-free ratio[J]. Int J Cardiol, 2016, 208: 128-136. DOI:10.1016/j.ijcard.2016.01.205 |
| [15] |
Kim SH, Hong MK, Park DW, et al. Impact of plaque characteristics analyzed by intravascular ultrasound on long-term clinical outcomes[J]. Am J Cardiol, 2009, 103(9): 1221-1226. DOI:10.1016/j.amjcard.2009.01.015 |
| [16] |
Spitaleri G, Tebaldi M, Biscaglia S, et al. Quantitative flow ratio identifies nonculprit coronary lesions requiring revascularization in patients with ST-segment-elevation myocardial infarction and multivessel disease[J]. Circ Cardiovasc Interv, 2018, 11(2): e006023. DOI:10.1161/CIRCINTERVENTIONS.117.006023 |
| [17] |
Asano T, Katagiri Y, Chang CC, et al. Angiography-derived fractional flow reserve in the SYNTAX Ⅱ trial: feasibility, diagnostic performance of quantitative flow ratio, and clinical prognostic value of functional SYNTAX score derived from quantitative flow ratio in patients with 3-vessel disease[J]. JACC Cardiovasc Interv, 2019, 12(3): 259-270. DOI:10.1016/j.jcin.2018.09.023 |

