2. 济宁市中医院, 济宁 272027
2. Jining Traditional Chinese Medicine Hospital, Jining 272027, China
乌头碱,新乌头碱等二萜类生物碱是乌头类药材的主要的药效成分,具有镇痛消炎的良好功效[1-4],但毒性很强,用药不当易造成中毒[5]。经炮制后,其中的乌头碱类化合物可转化为单酯型生物碱,单酯型生物碱具有良好的药理活性,且毒性远远低于双酯型生物碱[6],所以乌头类药材常不直接药用,而是将其炮制之后降低毒性。
目前,中成药乌头碱类成分的检测主要使用高效液相色谱法[7-10]。该方法检测灵敏度高,对于微量检测有着重要作用;重复性好,应用广泛,常用于大批量检测。本实验采用超声提取结合高效液相色谱法方法,对市售乌头类中药和中成药中的乌头碱类物质进行测定,为安全用药提供依据和参考。
1 仪器与材料 1.1 仪器SHIMADZU LC-2OAT双泵高效治相色谱仪(日本鸟津公司);GZY-P20-B超纯水仪(湖南科尔顿水务有限公司);FA2104N电子天平(上海菁海仪器有限公司);FW-100高速万能粉碎机(天津市泰斯特仪器有限公司);SB25-12DTD超声波清洗机(宁波新芝生物科技股份有限公司)。
1.2 试剂及样品乌头碱对照品(批号140303,北京恒元天启标准品有限公司);新乌头碱对照品(批号AB664W,天津一方科技有限公司);川乌,附子(济宁广联医药公司),附子理中丸(批号19013455、18011765,北京同仁堂科技发展股份有限公司制药厂),桂附地黄丸(批号190313、181201,北京同仁堂科技发展股份有限公司制药厂),伤湿止痛膏(批号191209、181101,湖南杏林春药业有限公司)。
2 方法与结果 2.1 乌头碱、新乌头碱的提取 2.1.1 标准品储备液制备准确称取乌头碱和新乌头碱固体标准品,以甲醇作为溶剂,溶解、定容至10ml,制得浓度分别为3.8μg/ml和5.6μg/ml的乌头碱和新乌头碱标准储备液。
2.1.2 样品处理根据药材和中成药不同的形态分别处理。附子和川乌为块状干药材,直接用粉碎机粉碎,全部过60目筛备用;附子理中丸为大蜜丸,将其剪碎,研钵研细备用;桂附地黄丸为黑棕色浓缩丸,研钵研细备用;伤湿止痛膏为片状橡胶膏,除去盖衬,剪成小块备用。
2.1.3 供试液的制备取按照2.1.2项处理的样品2g左右,精密称定,置锥形瓶中,加入25ml pH=2的盐酸水溶液,确保没过样品上端,用保鲜膜封住锥形瓶口防止溶剂在超声过程中挥发,于25 ℃下超声60min,对提取液进行过滤,过滤后弃去固体,滤液室温(30 ℃)下过夜挥至近干,残渣以流动相比例混合溶液复溶至2ml,用于随后的HPLC分析。
2.1.4 影响萃取效率的单因素实验为了获得最佳萃取效率,本实验以附子样品为基质,对可能影响萃取效率的多个因素,包括提取溶剂的种类、超声时间和超声温度等进行了优化,确定了最佳的提取条件。
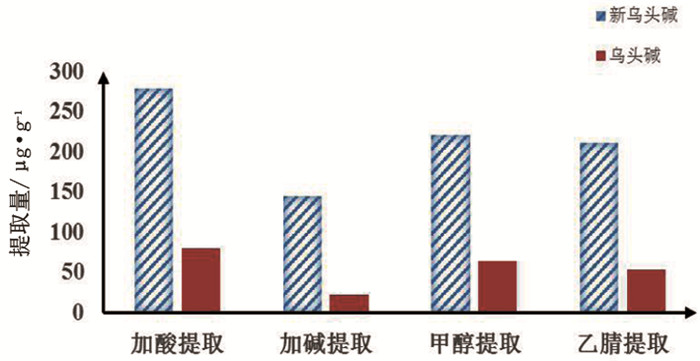
1) 提取溶液。本研究分别用甲醇、乙腈、pH=2的盐酸水溶液、pH=10的三乙胺水溶液进行超声提取,控制超声时间为45min,超声温度为25℃,酸性条件下提取效果最优。见图 1。
|
图 1 提取溶剂的优化 |
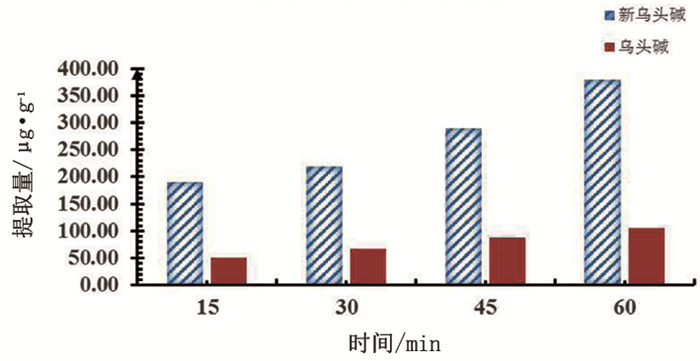
2) 超声时间。超声时间会影响萃取效率,本实验分别考察了超声15min、30min、45min、60min时的萃取效率,提取效果随着超声时间的延长而增加[11],结果显示为60min为最优超声时间。见图 2。
|
图 2 超声时间的优化 |
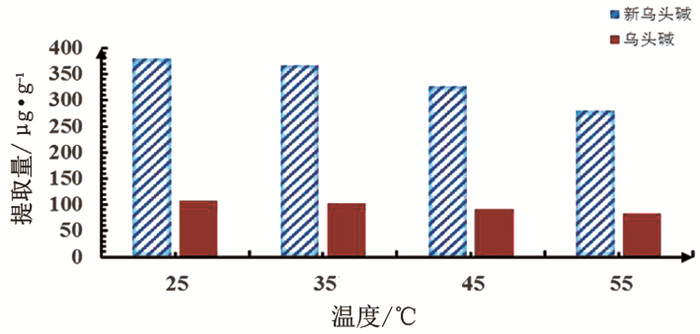
3) 提取温度。本实验探究了提取温度对萃取效率的影响。结果表明,25℃为最佳提取温度(见图 3)。这可归因于待测物质对热不稳定,超声温度过高易导致分解[12]。
|
图 3 提取温度的优化 |
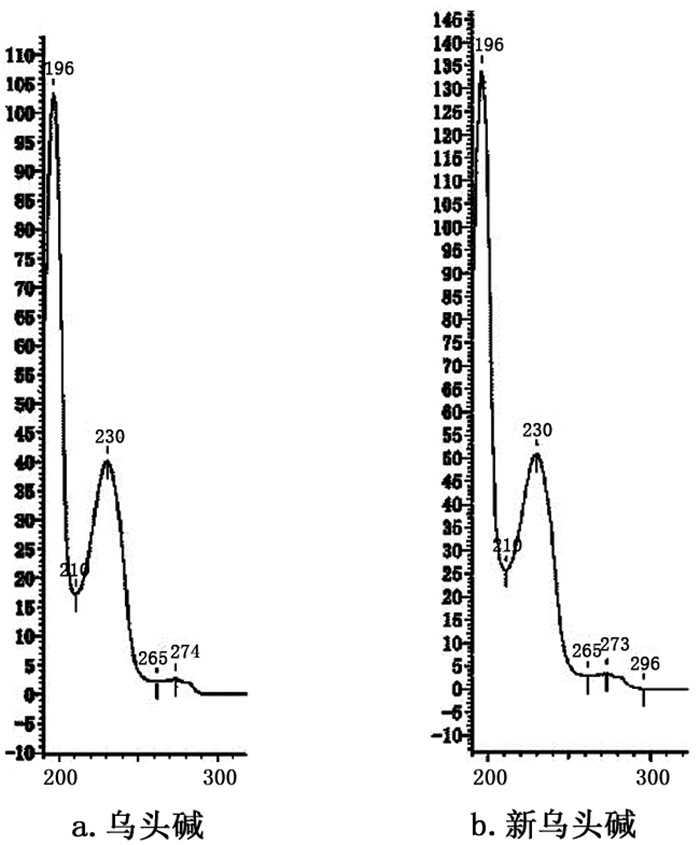
以标准溶液进液相分析,以SPD-M20A检测器对乌头碱和新乌头碱在200~700 nm范围内进行全波段扫描,发现乌头碱(图 4a)和新乌头碱(图 4b)均在196nm、230nm处出现两个较大吸收峰,考虑到196nm处产生紫外吸收的物质较多,易对样品测定产生较大基质干扰,最终选择230nm为乌头碱和新乌头碱的检测波长。
|
图 4 乌头碱和新乌头碱标准溶液紫外-可见光谱扫描图 |
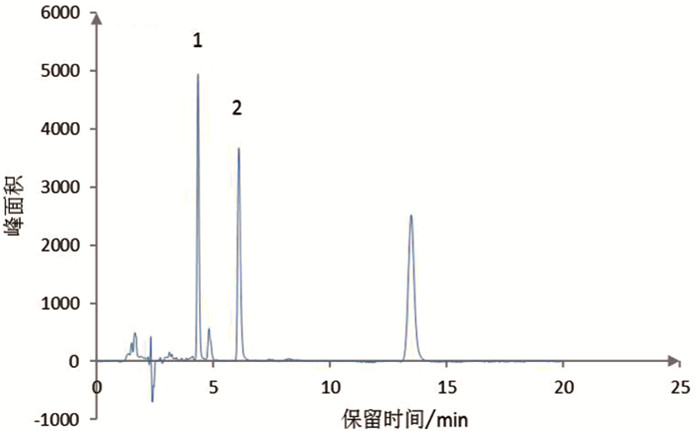
仅以标准溶液进样时,乙腈和0.03%三乙胺水溶液(pH=8)以体积比85 :15(v/v)的混合溶液能将新乌头碱与乌头碱二者较好地分离。但应用于实际样品时,因中药材成分复杂,分离效果不理想。因此更换流动相比例,选择乙腈和0.03%三乙胺水溶液(pH=8)以体积比60 :40(v/v)的混合溶液为流动相时,样品能实现较好的分离。见图 5、6。
|
图 5 85%乙腈色谱图 注:1为新乌头碱,2为乌头碱 |

|
图 6 60%乙腈色谱图 注:1为新乌头碱,2为乌头碱 |
吸取乌头碱、新乌头碱浓度分别为3.8μg/ml、5.6μg/ml的混合标准溶液,稀释至合适浓度,按照1.1色谱条件上机测定,以三倍信噪比所对应的浓度为检出限。见表 1。
| 表 1 检出限及线性关系 |
以甲醇为溶剂,分别配制乌头碱浓度为3.8μg/ml, 7.6μg/ml, 15.2μg/ml, 30.4μg/ml, 60.8μg/ml,新乌头碱浓度为5.6μg/ml, 11.2μg/ml, 22.4μg/ml, 44.8μg/ml, 89.6μg/ml的混合标准溶液。以1.1描述的仪器条件进HPLC检测,记录峰面积。以标准品的浓度为横坐标(μg/ml),以峰面积为纵坐标,得到线性方程(表 1)。
2.2.4 日内精密度吸取乌头碱浓度为15.2μg/ml,新乌头碱浓度为22.4μg/ml的混合标准溶液10μl,在24h内,每隔1h进样1次,连续进样6次,计算6次峰面积的平均值及RSD值。见表 2。
| 表 2 精密度 |
选取配制好的乌头碱浓度为3.8μg/ml,新乌头碱浓度为5.6μg/ml的混合标准溶液,两星期内选取3d,每天平行测定3次,计算三日峰面积的平均值及RSD值,见表 2。
2.2.6 稳定性取按照2.1.3制备的桂附地黄丸样品供试液,按照确定的色谱条件,分别在0、2、4、6、8、10、12、24h测定各成分的峰面积,记录各化合物的峰面积并计算相对标准偏差。乌头碱和新乌头碱峰面积的RSD值为4.8%和4.5%。供试液可在1d内保持基本稳定。
2.2.7 重复性取5份同一批次桂附地黄丸样品,按照2.1.3方法制备供试液,将供试液进HPLC分析,记录峰面积并计算RSD值。乌头碱和新乌头碱峰面积的RSD值分别为4.6%和4.2%。
2.2.8 加标回收率依据桂附地黄丸(批号181201)中乌头碱和新乌头碱含量的80%,100%,120%,加适量对照品到桂附地黄丸样品中,按照2.1.2和2.1.3的步骤进行提取,每个样品平行进样3次,计算加标回收率。乌头碱和新乌头碱在低、中、高3个浓度范围内,加标回收率均控制在99.84%~103.28%,该方法准确可靠。见表 3。
| 表 3 加标回收率 |
将购买的川乌和附子两种中药,两个批次的3种常见含附子类药材的中成药,按照样品处理步骤处理后,进HPLC分析,每个样品测定3次,利用3次峰面积平均值计算每种药物中乌头碱和新乌头碱的含量,检测结果如表 4、5所示。
| 表 4 中药材中乌头碱及新乌头碱测定结果(μg/g) |
| 表 5 中成药中乌头碱及新乌头碱测定结果(μg/g) |
查阅《中华人民共和国药典》(2015版)可知,制川乌中所允许存在的双酯型生物碱最大浓度为0.40mg/g,根据小鼠灌胃的LD50推算,双酯型生物碱LD50为1.01mg/kg,若以一个60kg体重的成年人的服用剂量计算,结果显示附子理中丸、桂附地黄丸未超过服用计量;通过伤湿止痛膏摄入的乌头碱含量也低于LD50的剂量,但是没有经过炮制的川乌、附子含量较高,不宜直接服用。
3 结论本实验建立的超声提取结合高效液相色谱法,能准确测定原药材和相关中成药中乌头碱与新乌含量。所建立的方法准确、高效、可靠,可为中成药类的用药安全和质量评估提供依据和参考。
| [1] |
张卫东, 韩公羽, 梁华清, 等. 国内外对中药附子成分与活性的研究[J]. 药学实践杂志, 1996, 14(2): 91-95. |
| [2] |
荣宝山, 韩雪梅, 麻春杰, 等. 《金匮要略》中预防乌头类方剂中毒方法浅谈[J]. 中华中医药杂志, 2016, 31(4): 1454-1456. |
| [3] |
Sun B, Wu SM, Li L, et al. A metabolomic analysis of the toxicity of Aconitum sp.Alkaloids in rats using gas chromatography/mass spectrometry[J]. Rapid Commun Mass Spectr, 2009, 23(1): 1221-1228. DOI:10.1002/rcm.3992 |
| [4] |
Oyama T, Isono T, Suzuki Y, et al. Anti-nociceptive effects of aconiti tuber and its alkaloids[J]. America J Chin Medi, 1994, 22(2): 175-182. DOI:10.1142/S0192415X94000218 |
| [5] |
彭劭, 刘莉萍, 金永日, 等. RP-HPLC-ELSD测定草乌中准噶尔乌头碱的含量[J]. 中国实验方剂学杂志, 2016, 22(11): 80-83. DOI:10.13422/j.cnki.syfjx.2016110080 |
| [6] |
刘菊, 张惠霞, 张红伟, 等. HPLC法同时测定痹通药酒中4种生物碱成分[J]. 中成药, 2017, 39(12): 26-32. DOI:10.3969/j.issn.1001-1528.2017.12.045 |
| [7] |
史煜华, 黄文康, 黄琴伟, 等. SPE-HPLC测定风湿骨痛片中6种生物碱类物质的含量[J]. 中国现代应用药学, 2018, 35(12): 1797-1800. DOI:10.13748/j.cnki.issn1007-7693.2018.12.009 |
| [8] |
张聿梅, 何轶, 李耀磊, 等. 高效液相色谱与QDA质谱联用同时测定附子理中丸中6个单酯及双酯型生物碱含量[J]. 药物分析杂志, 2018, 38(7): 1248-1253. DOI:10.13422/j.cnki.syfix.2016110080 |
| [9] |
昝珂, 旺杰次仁, 鲁静, 等. HPLC测定蒙药材草乌叶中4种双酯型二萜生物碱含量[J]. 中国中药杂志, 2018, 43(4): 766-771. DOI:10.19540/j.cnki.cjcmm.20180104.08 |
| [10] |
何风艳, 何轶, 戴忠, 等. HPLC-MS/MS法同时测定骨刺片中7个生物碱的含量[J]. 药物分析杂志, 2018, 38(10): 1810-1816. |
| [11] |
李艳芝, 刘树玲, 刘文杰, 等. 蒲公英黄酮类成分超声辅助半仿生提取及含量测定[J]. 济宁医学院学报, 2020, 43(1): 5-9. DOI:10.3969/J.issn.1000-9760.2020.01.002 |
| [12] |
李萌, 张根衍, 潘桂湘. 乌头类生物碱稳定性研究[J]. 辽宁中医药大学学报, 2014, 16(1): 52-55. DOI:10.13194/j.issn.1673-842x.2014.01.019 |



