2. 山东广育堂国药有限公司, 济宁 272071
2. Shandong Guangyu Tang Guo Yao Co., Ltd., Jining 272071, China
二仙膏(Erxiangao)组方主要有人参、枸杞、鹿角胶、龟板、牛鞭、黄芪、黑芝麻、核桃仁、熟地黄(砂仁拌)、制何首乌、五味子(酒制)、沙苑子、远志、牛膝、丹参、山药十六味药,辅料为蜂蜜。二仙膏滋阴助阳,益气养血。用于治疗气血两虚,神疲体倦,周身懒软,神经衰弱。其组方合理,是广育堂传承的经验方,国家首批中药保护品种,入选国家非物质文化遗产保护代表性项目。
二仙膏用于肿瘤患者康复治疗,显著提高患者的生活质量和生存时间,得到许多患者的一致好评。初步药理试验结果表明,二仙膏对化疗药致白细胞减少症小鼠模型的免疫功能有明显改善作用,可显著增加白细胞和造血细胞的数量,增强机体免疫力[1-2]。中药复方成分复杂,研究其药效物质基础对于阐明整体功效、作用机制及提高质量标准具有关键作用,其中,中药复方有效成分的研究能够在一定程度上明确中药发挥药效的物质基础,寻找并定量测定其有效部位是现阶段中药药效物质基础研究的最基础、最重要环节[3-4]。中药复方质量标准的完善制定是确保疗效稳定、用药安全的有效依据[5]。虽然二仙膏有很好的临床疗效,但是现有质量标准简单,且药效物质基础尚不明确,需进一步深入研究。通过分析二仙膏的方解及文献报道药味的有效成分,表明总皂苷、总多糖提高机体免疫力效果明显[6-8],且预实验表明这2大类成分含量较高,故本文研究紫外可见分光光度法测定二仙膏总皂苷、总多糖的含量,为提高质量控制方法和下一步药效物质基础的深度研究奠定基础。
1 仪器与材料 1.1 仪器TU-1901光双束紫外可见分光光度计(北京普析通用仪器有限责任公司);102-2A电热鼓风干燥箱(龙口市先科仪器公司);JJ224BC电子天平(G&G公司);旋转蒸发仪(巩义市予华仪器有限公司);SHK-IIIS循环水式多用真空泵(郑州科泰实验设备有限公司);玻璃仪器气流烘干器(河南省予华仪器有限公司)。
1.2 试药二仙膏(山东广育堂国药有限公司,批号20190501、20190601、20190701);齐墩果酸(中国药品生物制品检定所,批号110709-201705);AR无水葡萄糖(天津市登科化学试剂有限公司,批号161111);AB-8大孔树脂(天津市光复精细化工研究所,批号20170408);正丁醇,无水乙醇,硫酸,乙酸,高氯酸,甲醇,蒽酮均为分析纯,水为蒸馏水。
2 方法与结果 2.1 二仙膏总皂苷的测定 2.1.1 对照品溶液的制备精密称取干燥至恒重的齐墩果酸对照品14.00mg,置10ml容量瓶中,加入甲醇溶解,摇匀,定容;精密吸取1.0ml,用甲醇定容至10ml,摇匀,即得。
2.1.2 供试品溶液的制备精密称取二仙膏0.6g,加水2ml,溶解后用正丁醇萃取4次,合并正丁醇减压蒸干,浸膏用甲醇溶解,过滤,定容至50ml,精密吸取5.0ml,用甲醇定容至10ml,摇匀,即得。
2.1.3 溶液的显色精密量取对照品溶液或供试品溶液0.4ml,置于25ml具塞试管中,水浴挥干溶剂,依次加入0.2ml 5%香草醛-冰醋酸溶液和0.8ml高氯酸,摇匀后置70℃恒温水浴15min,随后立即取出,置冰浴中冷却3min,加冰乙酸5.0ml,摇匀,放置10min,用于吸光度测定。
2.1.4 测定波长的选择分别精密量取齐墩果酸对照品溶液和供试品溶液0.4ml,置于25ml具塞试管中,按照“2.1.3”项下方法进行显色,以相应试剂为空白对照,于400~800nm波长处扫描,结果显示对照品溶液和样品溶液均在(540±2)nm处有最大吸收,故确定检测波长为540nm。
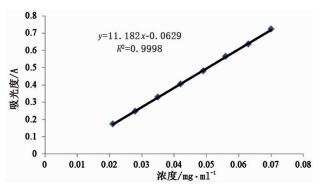
2.1.5 标准曲线的绘制和线性范围分别精密量取0.15、0.20、0.25、0.30、0.35、0.40、0.45、0.50ml对照品溶液,分别置于25ml具塞试管中,按照“2.1.3”项下方法进行显色,以空白溶剂同法处理作参比,于540nm波长下测定吸光度,以吸光度(A)为纵坐标,浓度(C)为横坐标,绘制标准曲线,计算回归方程为:y=11.182x-0.0629(r=0.9999),表明齐墩果酸在0.021~0.070mg/mL浓度范围内与吸光度有良好的线性关系。见图 1。
|
图 1 齐墩果酸对照品标准曲线 |
取同一供试品溶液(批号20190601)0.4ml,置25ml具塞试管中,按“2.1.3”项方法进行显色,以空白溶剂同法处理作参比,于540nm波长下测定吸光度,平行测定吸光度值6次。计算吸光度的RSD为0.23%(n=6),表明精密度良好。
2.1.7 稳定性试验精密吸取供试品溶液(批号20190601)0.4ml,置25ml具塞试管中,按“2.1.6”项操作,分别在0、20、40、60、80、100、120min时各测定一次吸光度,计算吸光度的RSD为1.54%(n=7),结果表明供试品溶液在120min内稳定性良好。
2.1.8 重复性试验精密称量二仙膏(批号20190601),共6份,置50ml烧杯中,按“2.1.2”项方法制备,精密吸取供试品溶液0.4ml,置25ml具塞试管中,按“2.1.6”项操作,在540nm处测定其吸光度,计算总皂苷的平均含量为8.10mg/g,RSD为3.53%(n=6),表明该方法重复性良好。
2.1.9 加样回收率试验精密称定已知含量的批号为20190601的二仙膏6份,每份0.3000g,分别精密加入0.14mg/ml的齐墩果酸对照品溶液16.9ml,依“2.1.2”项制备供试品溶液,依法测定,测得齐墩果酸的平均回收率为96.77%,RSD为1.61%,表明该方法准确性良好。见表 1。
| 表 1 加样回收率实验结果 |
精密称取不同批次二仙膏0.6g,按“2.1.2”项制备供试品溶液,依法测定,计算总皂苷含量。见表 2。
| 表 2 样品总皂苷测定实验结果 |
精密称取干燥至恒重的葡萄糖对照品6.0mg,加水溶解,并定容至50ml,摇匀,即得。
2.2.2 供试品溶液的制备精密称取二仙膏2.0g,加3.0ml水溶解,过AB-8大孔树脂柱(内径2.4cm,高22.5cm),用水洗脱3个柱体积,洗脱液浓缩,加水定容至50ml,从中精密吸取0.5ml,加水定容至100ml,混匀,即得。
2.2.3 溶液的显色精密吸取葡萄糖对照品溶液或供试品溶液0.5ml,置25ml具塞试管中,加水至2ml,加0.2%蒽酮-浓硫酸溶液6.0ml,摇匀,置水浴中加热15min,取出,放入冰浴中冷却15min,用于吸光度测定。
2.2.4 测定波长的选择分别精密量取葡萄糖对照品溶液和供试品溶液0.50ml,置于25ml具塞试管中,按照“2.1.3”项进行显色,以相应试剂为空白对照,于400~800nm波长处扫描,结果显示对照品溶液和样品溶液均在620nm处有最大吸收,故确定检测波长为620nm。
2.2.5 标准曲线的绘制和线性范围分别精密吸取浓度为0.12mg/ml葡萄糖对照品溶液0.2、0.4、0.6、0.8、1.0ml置25ml具塞试管中,加水至2ml,精密加入0.2%硫酸-蒽酮溶液6.0ml,摇匀,置水浴中加热15min,取出,放入冰浴中冷却15min,在620nm处测定吸光度,计算回归方程为:y=6.8708x+0.0231(r=0.9999),表明葡萄糖在0.024~0.120mg/mL浓度范围内与吸光度有良好的线性关系。见图 2。

|
图 2 葡萄糖对照品标准曲线 |
取同一供试品溶液(批号20190701)0.5ml,置25ml具塞试管中,按“2.2.3”项进行显色,以空白溶剂同法处理作参比,于620nm波长下测定吸光度,平行测定吸光度值6次。计算吸光度的RSD为0.12%(n=6),表明精密度良好。
2.2.7 稳定性试验精密吸取同一供试品溶液(批号20190701)0.5ml,置25ml具塞试管中,按“2.2.6”项操作,分别在0、20、40、60、80、100min时各测定一次吸光度,计算吸光度的RSD为0.71%(n=6),结果表明供试品溶液在100min内稳定性良好。
2.2.8 重复性试验精密称量二仙膏(批号20190701),共6份,按“2.2.2”项方法制备,精密吸取供试品溶液0.5ml,置25ml具塞试管中,按“2.2.6”项操作,在620nm处测定其吸光度,计算总糖的平均含量为34.78%,RSD为3.58%(n=6),表明该方法重复性良好。
2.2.9 加样回收率试验精密称定已知含量的批号为20190701的二仙膏6份,每份1.0g,分别精密加入347.8mg的葡萄糖对照品,依“2.2.2”项制备供试品溶液,依法测定,测得葡萄糖的平均回收率为101.83%,RSD为0.92%,表明该方法准确性良好。见表 3。
| 表 3 加样回收率试验结果 |
精密称取不同批次二仙膏2.0g,按“2.2.2”项下方法制备供试品溶液,依法测定,计算总糖含量。见表 4。
| 表 4 样品总糖含量测定结果 |
二仙膏有滋阴助阳,益气养血的功效,结合文献报道分析该药的处方组成及方解,通过系统化学成分预试验的方法,初步确定二仙膏中含量较高的有效成分主要有皂苷类、多糖类[9-12]。本文通过方法学考察,表明紫外可见分光光度法测定总皂苷及总糖的含量方法简便、准确、灵敏度高、重复性好、稳定性高,可作为二仙膏中总皂苷、总糖的含量测定方法。本文二仙膏中大类成分的含量测定,为后续其物质基础研究和质量控制奠定了基础。
| [1] |
许律捷, 康德, 贾皓, 等. 二仙膏对环磷酰胺致白细胞减少症小鼠免疫功能的影响与免疫的初步研究[J]. 中国新药杂志, 2018, 27(8): 940-947. |
| [2] |
许律捷, 康德, 王金华, 等. 二仙膏对化疗后白细胞减少症的药效作用[J]. 中国药理学与毒理学杂志, 2016, 30(10): 1032-1033. |
| [3] |
张王宁, 李爱平, 李科, 等. 中药药效物质基础研究方法进展[J]. 中国药学杂志, 2018, 53(10): 761-764. |
| [4] |
汪小莉, 刘晓, 韩燕全, 等. 中药药效物质基础主要研究方法概述[J]. 中草药, 2018, 49(4): 941-947. |
| [5] |
张宏梅, 崔佰吉. 中药复方质量标准研究方法与思路[J]. 世界最新医学信息文摘, 2017, 17(101): 83. |
| [6] |
Wang JW, Li YX, Luo P, et al. Oral supplementation with ginseng polysaccharide promotes food intake in mice[J]. Brain Behav, 2019, 9(9): e01340. DOI:10.1002/brb3.1340 |
| [7] |
Riaz Muhammad, Rahman Najm Ur, Zia-Ul-Haq, et al. Ginseng:A dietary supplement as immune-modulator in various diseases[J]. Trends Food Sci Tech, 2019, 83: 12-30. DOI:10.1016/j.tifs.2018.11.008 |
| [8] |
Li P, Liu QP. Analysis of astragalus membranaceus in promoting anti-tumor immune function and international spread of TCM[J]. B Malariol Salud AMB, 2019, 59(2): 21-28. |
| [9] |
平静, 李清, 陈晓辉, 等. 山药总皂苷提取工艺研究[J]. 中国民族民间医药, 2010, 21: 33-35. |
| [10] |
孙红祥.远志中皂苷类免疫佐剂活性成分的分离机活性评价[D].杭州:浙江大学, 2005.
|
| [11] |
沈舒, 王琼, 李友宾. 牛膝的化学成分和药理作用研究进展[J]. 海峡药学, 2011, 23(11): 1-6. DOI:10.3969/j.issn.1006-3765.2011.11.001 |
| [12] |
孙政华, 邵晶, 郭玫. 黄芪化学成分及药理作用研究进展[J]. 中医临床研究, 2015, 7(25): 22-25. DOI:10.3969/j.issn.1674-7860.2015.25.009 |

