阿胶是传统的滋补佳品,李时珍著《本草纲目》载:阿胶为马科动物驴的皮,经煎煮、浓缩制成的固体胶[1]。阿胶主要由骨胶原组成,其水解可得明胶、蛋白质及多种氨基酸[2-3]。现代药理研究表明,阿胶对血液、造血系统、钙代谢、免疫系统等均有保护作用,且有增强记忆、抗疲劳、耐缺氧等作用[4-8]。但是,长期以来由于技术条件和传统中药制药思想的制约,阿胶的很多功效作用还未得到足够的实验证实,特别是在调节机体免疫功能方面,相关的实验研究较少。本文旨在通过观察对比不同品牌阿胶对由环磷酰胺(cyclophosphamide,Cy)致免疫低下小鼠免疫功能的影响,为阿胶的合理开发应用提供参考。
1 材料与方法 1.1 材料 1.1.1 实验动物健康ICR小鼠,4~8周鼠龄,平均体重为19~22g,雌雄各半,由济宁医学院动物房提供。所有动物实验均遵循国家实验动物饲养管理条例和使用指南以及济宁医学院实验动物管理条例。
1.1.2 仪器与试剂DYY-7C型电泳仪(北京六一生物科技有限公司);SW-CJ-2FD型净化工作台(苏洁医疗有限公司);Multiskan酶标仪(上海赛默飞世尔仪器有限公司);T100TM Thermal Cycler PCR仪(BIORAD公司)。阿胶:A、B、C 3种品牌的阿胶购自日照海力日盛药业有限公司,阿胶经粉碎机粉碎后,室温贮存,实验时以蒸馏水配置成5%(0.08g/1.6ml)的悬浊液,备用;环磷酰胺注射液(上海源叶生物科技有限公司);10%豚鼠血清;PBS溶液。
1.2 方法 1.2.1 动物分组及模型建立健康ICR小鼠75只,随机分成5组:对照组、Cy组、A品牌阿胶组、B品牌阿胶组和C品牌阿胶组,每组15只。3种品牌阿胶组每天灌胃5%的阿胶溶液0.1ml,对照组每天灌胃等体积的氯化钠溶液。Cy造模:实验第4天,3种品牌阿胶组和Cy组腹腔注射80mg/kg Cy 0.2ml,对照组腹腔注射0.2ml的氯化钠溶液。
1.2.2 小鼠免疫器官胸腺、脾脏指数的测定第7天实验结束后,称取小鼠的体重并做好记录,颈椎脱臼,处死小鼠后,经无菌操作解剖取其胸腺和脾脏,称重并做记录,计算脾脏及胸腺指数。计算公式:胸腺(脾脏)指数=胸腺(脾脏)质量(mg)/体重(g)。
1.2.3 小鼠血清溶血素测定在实验第6天每组小鼠均腹腔注射10%的绵羊红细胞进行初次免疫,实验第7天最后一次给药2h后,眼球取血2ml,置于EP管中,用2000r/min离心10min,取上清,标注,分别稀释为1 :25,1 :100,1 :800,1 :1500,1 :2500,1 :3000,37℃放置1h后,分别取0.1ml与0.2% SRBC 0.1ml和0.1ml 10%豚鼠血清混合,2000r/min离心10min,取上清,置于酶标板4个孔中,检测OD值。
1.2.4 小鼠血清TNF-α和GM-CSF含量测定实验第7天最后一次灌胃后,小鼠眼球取血1ml,置于37℃放置30min后,2000r/min转速,离心10min,吸取上层血清置于微量反应孔,参照ELISA试剂盒说明书进行操作,酶标仪在450nm处测量OD值。
1.2.5 小鼠脾脏TNF-α和GM-CSF mRNA表达测定最后一次灌胃后8h,取小鼠脾脏,Trizol法提取脾脏总RNA,将获得的总RNA进行反转录。首先将2μl RNA,1μl Oligo dT Primer,1μl dNTP mixture和6μl ddH2O加入0.2ml EP管中,然后在65℃下保温5min,拿出后冰上迅速冷却,然后加入4μl 5×PrimeScript Ⅱ Buffer,0.5μl RNase Inhibitor,1μl PrimeScript RTase和4.5μl ddH2O,反转录得cDNA,随即进行PCR扩增反应。TNF-α引物(209bp):上游5′-ACCGTCAGCCGAT TTGCTAT-3′下游3′-CCGGACTCCGCAAAGTCTAA-5′;GM-CSF引物(283bp):上游5′-GCCAGGAGA TTCCACAACTCAG-3′,下游5′-GCATGTCATCCAGGAGGTTCAGG-3′。内参采用小鼠GAPDH(183bp):上游5′-ATTCAACGGCACAGTCAAGG-3′,下游5′-GCAGAAGGGGCCGGAGATGA-3′。PCR产物行2%的琼脂糖凝胶电泳,计算光密度值。
1.3 统计学方法数据分析采用SPSS21.0软件进行分析。
2 结果 2.1 阿胶对小鼠胸腺和脾脏指数的影响与对照组比,Cy模型组小鼠胸腺指数、脾脏指数显著降低(P < 0.001),说明成功制备免疫抑制小鼠模型。与Cy组相比,3种品牌阿胶组的胸腺和脾脏指数均升高(P < 0.001),说明不同品牌的阿胶均能够提升小鼠免疫器官的功能。A、B、C 3种品牌阿胶相比较,A、B两种品牌阿胶效果较好。
| 表 1 阿胶对小鼠免疫器官的影响 |
与对照组小鼠比较,Cy组小鼠血清溶血素OD值降低(P < 0.001),说明使用环磷酰胺造模成功。与Cy组比,3种品牌阿胶组的小鼠血清溶血素OD值均升高(P < 0.001),提示阿胶能够提高小鼠体液免疫。A、B、C 3种品牌阿胶组相比较,A、B两种品牌阿胶组效果较好。
| 表 2 5组小鼠溶血功能的影响 |
与对照组比较,Cy组小鼠血清中TNF-α和GM-CSF浓度均显著降低(P < 0.001)。与Cy组比,3种品牌阿胶组小鼠血清中的TNF-α和GM-CSF浓度均明显提高(P < 0.001)。其中,A品牌阿胶组与B、C品牌阿胶组相比较,GM-CSF的浓度最高(P < 0.001),3种品牌阿胶组TNF-α的浓度无显著性差异。
| 表 3 5组小鼠血清TNF-α和GM-CSF的比较 |
与对照组相比较,Cy组小鼠脾脏TNF-α和GM-CSF mRNA的表达均显著下降(P < 0.001)。与Cy组小鼠比较,3种品牌的阿胶均可提高小鼠脾脏TNF-α和GM-CSF mRNA的表达(P < 0.001),其中,与B、C品牌阿胶组相比较,A品牌阿胶组提高GM-CSF mRNA的表达更为显著(P < 0.001)。
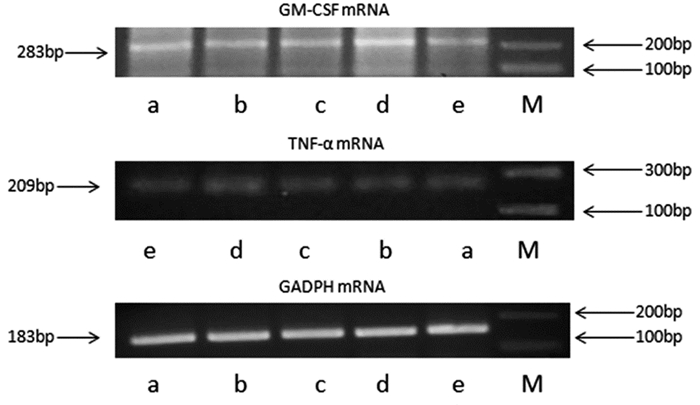
|
图 1 各组GM-CSF mRNA和TNF-α mRNA的表达 注:a.A品牌阿胶; b.B品牌阿胶; c.C品牌阿胶; d.对照组; e.Cy M:Marker |
| 表 4 5组小鼠TNF-α mRNA和GM-CSF mRNA的比较 |
阿胶与人参、鹿茸并称为“滋补三宝”,被收入《中华人民共和国药典》。阿胶味甘、性平,临床应用广泛,具有补血、止血、抗氧化、抑制肿瘤、增强免疫力等多方面的功效。本次研究主要关注阿胶对机体免疫功能的影响。阿胶能够增强由氢化可的松诱导免疫抑制小鼠的固有免疫应答,改善迟发型超敏反应、碳清除指数,显著提高脾脏内淋巴细胞转化能力和腹腔巨噬细胞吞噬活性[9-10]。但目前有关阿胶对机体免疫功能调节的具体机制及对细胞因子的影响研究较少。近年来,阿胶市场火爆,涌现出大量不同品牌,其制备工艺有所不同,产品价格也高低不一,市场份额差别大。不同品牌的阿胶在免疫方面的功效是否存在差异,也有待验证。本实验使用Cy建立免疫低下模型,探究阿胶对小鼠免疫活性的影响及对细胞因子产生的影响;同时对比分析不同品牌的阿胶对机体免疫活性的影响是否存在较大差异。
Cy属于烷化剂类的抗肿瘤药物,除用于肿瘤的治疗外,也可以作为免疫抑制剂使用[11]。高剂量Cy能够通过抑制DNA复制,促使细胞凋亡,从而使机体处于免疫抑制状态,可用于构建免疫功能低下的动物模型;而低剂量的Cy可通过下调Treg细胞的数量,提高免疫细胞的功能,反而产生免疫促进作用[12-13]。因此, 本次实验采用了腹腔注射高剂量(80mg/kg)的Cy建立免疫低下模型,结果显示无论是小鼠的胸脾指数,还是外周血抗体的生成率,均表现为显著下降,说明免疫抑制模型成功制备。
免疫器官的脏器系数是衡量机体免疫功能的初步指标。胸腺是T细胞分化成熟的场所,胸腺指数的改变可直观反映出机体的细胞免疫水平的变化;脾脏作为T、B细胞定居及发生免疫应答的场所,脾脏指数也能够很好地反映机体的免疫水平。本文结果显示,阿胶能显著的增加由Cy所致的免疫低下小鼠的胸腺及脾脏指数,对机体有很好的免疫保护作用。溶血素实验结果显示外周血抗体生成增加,反映了免疫应答较后期阶段体液免疫的增强,3组品牌的阿胶均能够提升小鼠外周血抗体的浓度,增强小鼠特异性免疫功能。
阿胶的一大著名功效是能够刺激造血,增强造血干细胞的活性[14]。GM-CSF(granulocyte-macrophage colony stimulating factor)是粒细胞-巨噬细胞集落刺激因子,是造血干细胞向巨噬细胞和粒细胞定向分化过程中所需的一种非常重要的造血细胞因子。TNF-α主要由单核细胞和巨噬细胞产生,因此TNF-α水平可很好地评价巨噬细胞的免疫效应,而巨噬细胞在非特异性免疫中发挥极为重要的作用。TNF-α含量升高后,能够刺激单核-巨噬细胞增殖,进一步增加GM-CSF的合成[15-16]。因此,TNF-α和GM-CSF的变化一致,相辅相成。本文结果显示,无论是小鼠的外周血还是脾脏中,阿胶的应用可大大提高由免疫抑制所导致的GM-CSF的下降,说明阿胶可刺激造血,提升造血性细胞因子的表达;同时,阿胶能显著提高小鼠TNF-α水平,促进机体的非特异性免疫,进一步增加GM-CSF的合成,刺激造血。
综上所述,3种品牌的阿胶均对由Cy致免疫抑制的小鼠具有很好的免疫保护作用,提升整体免疫水平,对体液免疫和非特异性免疫均有良好的促进作用。提示阿胶可能是通过促进TNF-α和GM-CSF的表达,促进免疫细胞的功能,提升机体造血能力。作为一种药食同源的传统本草,阿胶具有很好的研究价值与应用前景,其对机体免疫机能的调节机制今后仍需进一步的深入研究。
| [1] |
Sun T, Li S, Xia X, et al. ASIP gene variation in Chinese donkeys[J]. Anim Genet, 2017, 48(3): 372-373. DOI:10.1111/age.12530 |
| [2] |
杜怡波, 樊慧蓉. 阿胶的化学成分及药理作用研究进展[J]. 天津医科大学学报, 2018, 24(3): 267-270. |
| [3] |
刘谷全. 中药阿胶的临床应用及药理作用[J]. 临床合理用药杂志, 2014, 7(12): 74-75. DOI:10.3969/j.issn.1674-3296.2014.35.063 |
| [4] |
Wu H, Ren C, Yang F, et al. Extraction and identification of collagen-derived peptides with hematopoietic activity from Colla Corii Asini[J]. J Ethnopharmacol, 2016, 182: 129-136. DOI:10.1016/j.jep.2016.02.019 |
| [5] |
李敏, 庞萌萌, 田晨颖, 等. 不同阿胶酶解液相对分子量分布及补血升白作用对比研究[J]. 中国食品添加剂, 2017, 28(6): 105-111. DOI:10.3969/j.issn.1006-2513.2017.06.010 |
| [6] |
Ma LX, Ai P, Li H, et al. The prophylactic use of Chinese herbal medicine for chemotherapy-induced leucopenia in oncology patients:a systematic review and meta-analysis of randomized clinical trials[J]. Support Care Cancer, 2015, 23(2): 561-579. DOI:10.1007/s00520-014-2469-8 |
| [7] |
Xu HY, Wang SS, Yang HJ, et al. Study on action mechanism of adjuvant therapeutic effect compound Ejiao slurry in treating cancers based on network pharmacology[J]. Zhongguo Zhong Yao Za Zhi, 2014, 39(16): 3148-3151. |
| [8] |
孙叙敏, 陈信义. 复方阿胶浆对小鼠lewis肺癌CyclinD1、CD44表达的影响[J]. 世界中医药, 2013, 8(3): 318-321. DOI:10.3969/j.issn.1673-7202.2013.03.025 |
| [9] |
樊庆利. 探讨中药阿胶的临床应用和药理[J]. 中医临床研究, 2016, 8(11): 28-30. DOI:10.3969/j.issn.1674-7860.2016.11.012 |
| [10] |
吴伯姝. 阿胶的临床应用及药理作用[J]. 首都医药, 2014, 48(24): 151. |
| [11] |
Jia D, Lu W, Wang C, et al. Investigation on immunomodulatory activity of calf spleen extractive injection in cyclophosphamide-induced immunosuppressed mice and underlying mechanisms[J]. Scand J Immunol, 2016, 84(1): 20-27. DOI:10.1111/sji.12442 |
| [12] |
康慧琳, 樊卫平, 雷波, 等. 不同剂量环磷酰胺对小鼠免疫功能的影响[J]. 免疫学杂志, 2018, 34(4): 308-312. DOI:10.13431/j.cnki.immunol.j.20180047 |
| [13] |
Heylmann D, Bauer M, Becker H, et al. Human CD4+ CD25+ regulatory T cells are sensitive to low dose cyclophosphamide:implications for the immune response[J]. PLoS One, 2013, 8(12): e83384. DOI:10.1371/journal.pone.0083384 |
| [14] |
Wang D, Ru W, Xu Y, et al. Chemical constituents and bioactivities of Colla corii asini[J]. Drug Discov Ther, 2014, 8(5): 201-207. DOI:10.5582/ddt.2014.01038 |
| [15] |
Santiago E, Mora L, Bautista M, et al. Granulocyte colony-stimulating factor induces neutrophils to secrete macrophage colony-stimulating factor[J]. Cytokine, 2001, 15(6): 299-304. DOI:10.1006/cyto.2001.0937 |
| [16] |
吕慧, 刘建忠. 小儿急性肾炎患者血清中TNF-α、IGF-Ⅱ、GM-CSF和VEGF水平的研究[J]. 中国妇幼保健, 2014, 29(25): 4089-4091. DOI:10.7620/zgfybj.j.issn.1001-4411.2014.25.23 |



