2. 济宁医学院基础医学院, 济宁 272067
2. College of Basic Medicine, Jining Medical University, Jining 272067, China
抑郁症是一种常见的精神障碍性疾病,主要表现为情绪低落、兴趣缺乏、回避交往等[1]。随着现代社会生活节奏加快、工作压力加大,使得该症状逐渐显露,严重危害人类身心健康。迄今为止,对于抑郁症的发病机制尚未明确,严重制约了该病的有效防治。肠屏障是指肠道能够防止肠内的有害物质穿过肠黏膜进入人体,由机械屏障、化学屏障、免疫屏障与生物屏障共同构成[2],其中以机械屏障最为重要,正常情况下机械屏障由上皮细胞紧密连接、黏液与菌膜构成,其他屏障发生作用有赖于机械屏障的完整性。近年调查发现,慢性心理应激、不良生活事件等是肠易激综合征和炎症性肠病的发病因素[3],主要机制为慢性应激作用中枢神经系统,调控肠神经活动影响肠蠕动和分泌系统,进而导致炎症反应[4]。
抑郁症状态下肠黏膜机械屏障功能的情况,目前还不清楚。本文拟通过慢性社会击败应激模型模拟社会压力状态,评价其所致抑郁样小鼠肠道黏膜机械屏障的功能性变化,为抑郁症的治疗提供新治疗方案。
1 材料和方法 1.1 材料 1.1.1 动物C57BL/6小鼠,雄性,7周龄,体重22~24g,购于北京维通利华实验动物有限公司,标准环境饲养。退役雄性CD1种鼠,体重32~34g,购于北京维通利华实验动物有限公司,标准环境饲养。实验符合实验动物福利和动物伦理学要求。
1.1.2 实验器材显微镜(Moticam Pro 282A)、组织包埋机(Leica)、组织切片机(Leica)、实时荧光定量PCR仪(Thermo)、双板夹辛电泳槽(Bio-rad)、凝胶成像分析系统(Bio-rad)。
1.1.3 主要试剂HE染色液(国药集团)、二甲苯、无水乙醇、盐酸、中性树胶、总RNA提取试剂(上海生工)、通用反转录试剂盒(上海生工)、2×SG Fast qPCR Master Mix(上海生工)。
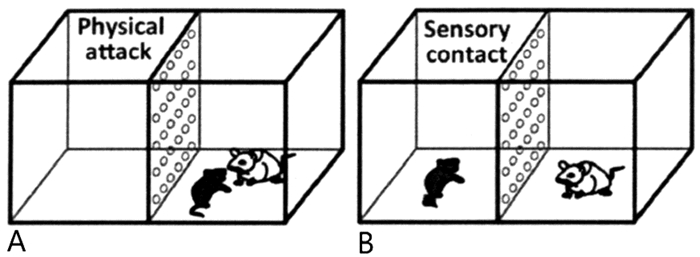
1.2 方法 1.2.1 慢性社会击败应激构建抑郁模型慢性社会击败应激模型的构建方法参照有关文献[5]。首先,筛选CD1小鼠攻击性。同时,选取C57BL/6小鼠随机分为对照组(CON)10只和应激组16只,单笼饲养,正常饮食1周。如图 1所示,取应激组C57BL/6小鼠1只,放入有陌生CD1小鼠的饲养笼隔间中使CD1小鼠会对C57BL/6小鼠进行间歇性的攻击,5min后,两只鼠被透明带孔的隔板分隔,持续24h。第2天将C57BL/6鼠放入另一只陌生CD1小鼠笼中;第3天再放入第3只CD1小鼠笼中,如此连续应激10d。在此期间,对照组则保持2只一笼,每天相互更换接触不同的C57BL/6小鼠。
|
图 1 慢性社会击败应激示意图 注:A.身体攻击;B.感官刺激 |
社会交互实验的具体过程参照相关文献[6]。第一阶段无社会交互对象(No Target),第二阶段有社会交互对象(Target),两个测试阶段均历时150s。如图 2所示,在敞(50cm×50cm×50cm)一侧正中放入底部有孔小盒,用来放置CD1小鼠,以一侧中点为中心,划出一矩形区域作为交互区域(interaction zone),另一侧两角落划出方形区域作为非交互区(Corners)。通过Anymaze动物行为学视频分析系统统计交互时间。计算对照组和应激组在Target中交互区与非交互区累积时间比率(interaction rate,IR),根据测试结果分亚组,应激组中IR < 1为抑郁敏感组(SUS, n=10),IR≥1为抑郁抵抗组(RES,n=6)。

|
图 2 社会交互实验示意图 |
抑郁造模成功后,眼球取血处死小鼠,迅速取出回肠、结肠。取相同部位部分回肠、结肠组织固定于4%多聚甲醛,用于HE染色。剩余组织,液氮速冻,并转移到-80℃保存,用于后期荧光定量PCR分析。
1.2.4 HE染色取固定好的组织,经脱水透明、浸蜡包埋、切片、脱蜡染色等步骤制作HE染色组织切片。镜检:每张切片随机取5个不同视野(60μm),进行组织病理学评分(表),包括炎细胞浸润程度、肠黏膜损伤程度及肠隐窝损伤程度3项。见表 1。总评分=每项评分×该项所涉及肠黏膜面积占总面积的百分比参数(0%~25%,1;26%~50%,2;51%~75%,3;76%~100%,4);0≤总分≤40;评分由2位病理专科医生双盲评估[7]。
| 表 1 肠道组织炎症损伤病理学评分 |
提取组织mRNA并纯化,反转录成cDNA后,进行qRT-PCR(以β-action作为内参照,即管家基因),琼脂糖凝胶电泳,分析各组小鼠绒毛组织中Muc2 mRNA表达量。使用-2△△Ct方法判断相对值。引物序列如下:
Muc2 上游引物 GCTATGTGCCTGGCTCTAATATGG
下游引物 GTGGGCACTTCACAGAGCAGAC
β-Actin 上游引物 GGGTCAGAAGGACTCCTATG
下游引物 GTAACAATGCCATGTTCAAT
1.3 统计学方法应用SPSS 22.0统计软件对数据进行分析。多组间比较采用方差分析,进一步两两比较采用SNK-q检验。以P<0.05为差异有统计学意义。
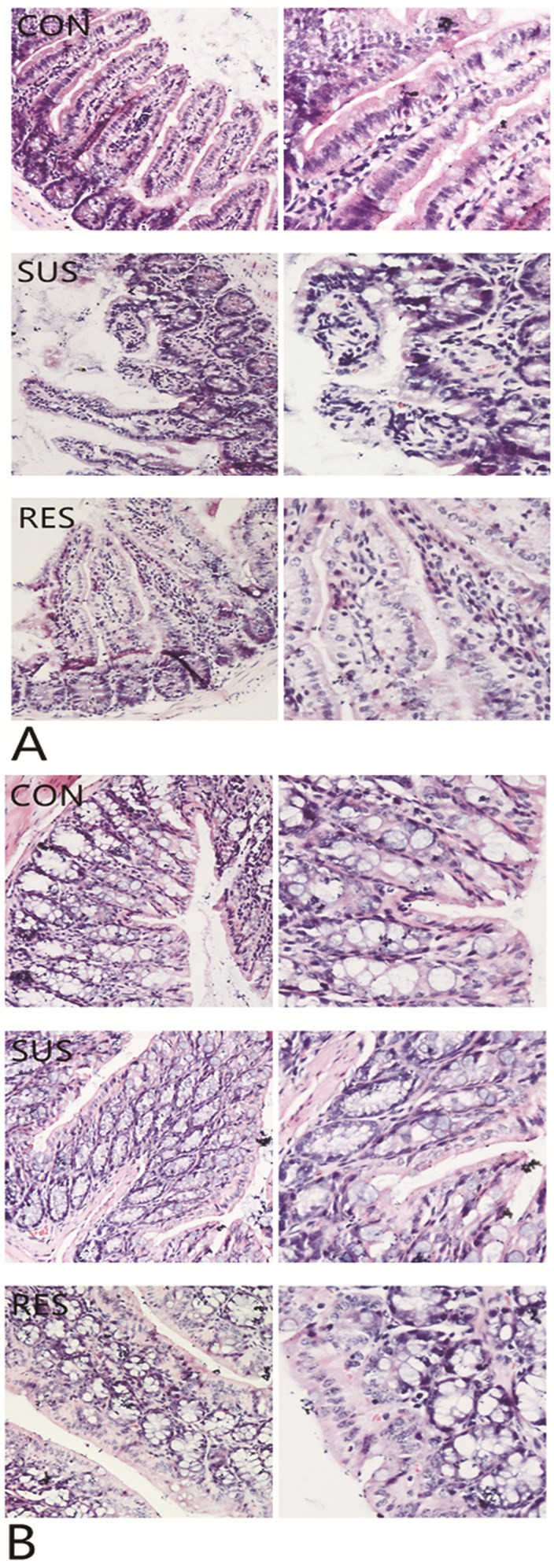
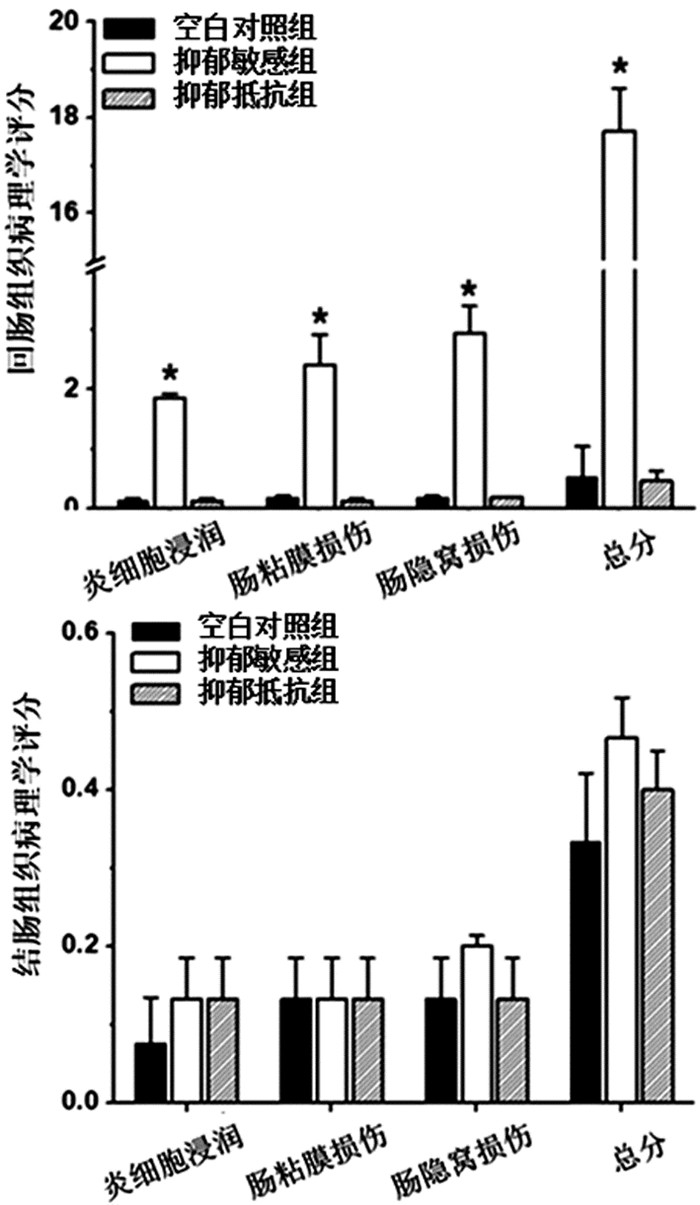
2 结果 2.1 小鼠肠组织切片HE染色结果与空白对照组小鼠相比,抑郁敏感组小鼠回肠组织结构发生改变,主要表现在炎细胞浸润数量增加、肠黏膜及肠隐窝出现损伤,抑郁抵抗组小鼠回肠无明显变化。与空白对照组相比,抑郁敏感组和抑郁抵抗组小鼠结肠组织结构均无明显变化。与空白对照组小鼠相比,抑郁敏感组小鼠回肠组织病理学评分明显提高(P<0.05),抑郁抵抗组小鼠无显著性差异(P>0.05)。与空白对照组小鼠相比,抑郁敏感组和抑郁抵抗组小鼠结肠组织病理学均无显著性差异(P>0.05)。见图 3、图 4。
|
图 3 小鼠肠道组织切片HE染色 注:A.回肠(60μm,30μm);B.结肠(60μm,30μm) CON.空白对照组;SUS.抑郁敏感组;RES.抑郁抵抗组 |
|
图 4 小鼠肠组织切片组织病理学评分 注:与CON相比,*P<0.05 |
与空白对照组小鼠相比,抑郁敏感组小鼠回肠Muc2基因表达量显著增加3.1倍(P<0.05),抑郁抵抗组小鼠与空白对照组无显著性差异(P>0.05)。见图 5。

|
图 5 小鼠回肠Muc2基因表达量 注:与CON相比,*P<0.05 |
肠道是人体最大、最直接的外环境[8],在维持人体健康方面发挥着重要作用。近几年研究表明,脑-肠轴是由中枢、自主、肠神经及免疫系统所构成的复杂双向调控网络[9],成为现在解析神经精神疾病发病机制的热点。
本文通过慢性社会击败应激模拟现今社会压力状态,构建抑郁模型,通常采用观察肠组织形态结构、内分泌体系等指标探究肠黏膜屏障的损伤状况[10]。本文中HE染色结果表明抑郁可导致小鼠肠黏膜机械屏障受损,主要表现为炎细胞浸润、肠黏膜及隐窝损伤,属于肠道炎症的常见症状[11],表明抑郁所致肠黏膜损伤主要表现为肠炎。且主要表现在回肠,结肠不明显。回肠作为小肠的一部分,表面有裸露的淋巴组织突起,即派伊尔结(PPs),Chassaing等[12]发现,炎症性肠炎复发的最早部位是PPs,可见小肠是机体内炎症发生发展的最初部位,结肠作为大肠的一部分,没有PPs,上皮有较厚的黏液层覆盖,是肠道微生物聚集的主要部位。本文中应用慢性社会击败应激造模时间为10d,分析小鼠可能处于抑郁初期,即炎症初发期,所以仅观察到回肠受损。本文中抑郁抵抗组小鼠较空白对照组小鼠肠组织形态学无显著性差异,从侧面说明,肠黏膜损伤可能对抑郁症的发生发展有重要影响。
肠黏膜表面有许多突起,称为肠绒毛,绒毛根部上皮向固有层下陷形成管状的小肠腺,称为肠隐窝,绒毛表面和隐窝侧壁分布有杯状细胞,分泌黏蛋白(Mucin,Muc2)形成黏液保护层,具有杀菌、润滑、通讯作用,通过观察黏液层及Muc2的表达可间接反映杯状细胞的功能性[13]。有研究发现慢性应激导致Muc2含量降低,提示黏液素分泌的减少是慢性应激造成黏膜损伤的可能诱因[14]。然而我们的qRT-PCR结果显示抑郁抵抗组较空白对照组小鼠回肠Muc2基因表达量显著增加(P<0.05),表明抑郁抵抗组小鼠回肠中杯状细胞代谢活性增强,推测Muc2的mRNA表达增加可能是抑郁初期杯状细胞对其数量减少和黏液层损伤的一种暂时性负反馈现象。
以上结果提示慢性社会击败应激所致小鼠的抑郁症状与肠粘膜机械屏障损伤程度正相关,且主要与回肠相关。
| [1] |
张景岳. 类经[M]. 北京: 人民卫生出版社, 2000: 245.
|
| [2] |
Baumgart DC, Dignass AU. Intestinal barrier function[J]. Curr Opin Clin Nutr Metab Care, 2002, 5(6): 685-694. DOI:10.1097/01.mco.0000038813.16540.3b |
| [3] |
Santos J, Alonso C, Vicario M, et al. Neuropharmacology of stress-induced mucosal inflammation:implications for inflammatory bowel disease and irritable bowel syndrome[J]. Curr Mol Med, 2008, 8(4): 258-273. DOI:10.2174/156652408784533788 |
| [4] |
Santos J, Yates D, Guilarte M, et al. Stress neuropeptides evoke epithelial responses via mast cell activation in the rat colon[J]. Psychoneuroendocrinology, 2008, 33(9): 1248-1256. DOI:10.1016/j.psyneuen.2008.07.002 |
| [5] |
Golden SA, Covington HE 3rd, Berton O, et al. Corrigendum:a standardized protocol for repeated social defeat stress in mice[J]. Nat Protoc, 2015, 10(4): 643. DOI:10.1038/nprot0415-644a |
| [6] |
Wook Koo J, Labonté B, Engmann O, et al. Essential role of mesolimbic brain-derived neurotrophic factor in chronic social stress-induced depressive behaviors[J]. Biol Psychiatry, 2016, 80(6): 469-478. DOI:10.1016/j.biopsych.2015.12.009 |
| [7] |
Scaldaferri F, Sans M, Vetrano S, et al. Crucial role of the protein C pathway in governing microvascular inflammation in inflammatory bowel disease[J]. J Clin Invest, 2007, 117(7): 1951-1960. DOI:10.1172/JCI31027 |
| [8] |
Clemente JC, Ursell LK, Parfrey LW, et al. The impact of the gut microbiota on human health:an integrative view[J]. Cell, 2012, 148(6): 1258-1270. DOI:10.1016/j.cell.2012.01.035 |
| [9] |
Dinan TG, Cryan JF. Brain-gut-microbiota axis and mental health[J]. Psychosomatic Medicine, 2017, 79(8): 920-926. DOI:10.1097/psy.0000000000000519 |
| [10] |
Mazzon E, Sturniolo GC, Puzzolo D, et al. Effect of stress on the paracellular barrier in the rat ileum[J]. Gut, 2002, 51(4): 507-513. DOI:10.1136/gut.51.4.507 |
| [11] |
毛靖伟, 王英德. 肠黏膜屏障在炎症性肠病中作用机制的研究进展[J]. 世界华人消化杂志, 2010, 18(7): 695-698. DOI:10.3969/j.issn.1009-3079.2010.07.011 |
| [12] |
Chassaing B, Etienne-Mesmin L, Bonnet R, et al. Bile salts induce long polar fimbriae expression favouring Crohn's disease-associated adherent-invasive Escherichia coli interaction with Peyer's patches[J]. Environ Microbiol, 2013, 15(2): 355-371. DOI:10.1111/j.1462-2920.2012.02824.x |
| [13] |
余晶仪, 郝小燕, 龙敏, 等. MUC2基因表达对益生菌调节肠屏障作用的影响[J]. 南方医科大学学报, 2013, 33(2): 197-201. DOI:10.3969/j.issn.1673-4254.2013.02.08 |
| [14] |
Cummins EP, Crean D. Hypoxia and inflammatory bowel disease[J]. Microbes Infect, 2017, 19(3): 210-221. DOI:10.1016/j.micinf.2016.09.004 |



