2. 济宁医学院附属医院, 济宁 272029
2. Affiliated Hospital of Jining Medical University, Jining 272029, China
胶质细胞瘤(Glioblastoma,GBM)是颅内最常见的恶性肿瘤,其以侵袭性强、增殖速度快和术后易复发为显著特点[1]。即使经过手术、放疗和化疗等综合治疗后,患者的平均生存时间也只有18个月左右[2]。而且,治疗GBM的一线化疗药物替莫唑胺(Temozolomide,TMZ)已表现出明显的耐药性。目前,具有抗肿瘤[3]、抗炎[4]和神经保护[5]等作用的柯里拉京(Corilagin)关注度与探索价值越来越高。本实验以不同浓度的Corilagin干预U373 MG细胞,并检测药物干预后不同时间段的细胞增殖活性及迁移能力的变化,观察Corilagin对胶质瘤细胞的影响,并为Corilagin的临床运用提供一个新的依据。
1 材料与方法 1.1 材料U373MG胶质瘤细胞系(中国典型培养物保藏中心);RPMI-1640培养基(美国Gibco公司);青-链霉素双抗(美国HyClone公司); 胎牛血清(fetal bovine serum,FBS)(美国HyClone公司);胰蛋白酶(美国Gibco公司); PBS磷酸缓冲液(普诺赛生命科技有限公司);Corilagin(美国Sigma公司);Cell CountingKit-8(CCK-8)试剂盒(碧云天生物技术研究所); MK3型酶标仪(美国赛默飞世尔科技公司)。
1.2 U373MG细胞培养取U373MG细胞接种在含有完全培养基(RPMI-1640+1%青-链霉素双抗+10%FBS)的25cm2的透气细胞培养瓶中,置于恒温细胞培养箱(37℃,5%CO2饱和湿度)中进行培养。每日用显微镜观察细胞的生长状况,每2日更换一次细胞培养液,当肿瘤细胞铺满培养瓶底约80%(48~72h)时即可传代,如此循环培养,直至所需细胞数。
1.3 CCK-8试剂盒检测细胞增殖活性选取培养的U373MG细胞接种于96孔板上,每孔约5000个(100μl)细胞,完全培养基培养24h后弃掉培养基,重新加入RPMI-1640 100μl,24h后再弃掉96孔板中的RPMI-1640培养基,配制的含不同浓度的Corilagin培养液(完全培养基+Corilagin),Corilagin浓度分别为25、50、100、200μmol·L-1(以0μmol·L-1为对照组,用RPMI-1640代替),按实验设计每孔加100μl,每组均设3个复孔,分别干预24、48、72h,并分别加入100μl RPMI-1640+CCK-8混合液(RPMI-1640 :CCK-8=10 :1),置于恒温培养箱中培养2h后,用酶标仪检测每个孔的吸光度值,每个检验重复3次,检测波长450nm,参照波长630nm。计算细胞存活率(%)=[(干预组OD值-空白组OD值)/(对照组OD值-空白组OD值)]×100%。
1.4 细胞划痕实验选培养至传代的U373MG细胞接种于6孔板中,每孔约2×105个(2ml)细胞,正常培养24h后,用无菌枪头(10μl)均匀划痕,并用PBS冲洗掉细胞碎片,更换细胞培养液,实验组培养液含Corilagin浓度为200μmol·L-1,对照组为不加Corilagin的培养液,再继续培养24、48和72h,在显微镜下每24h观察1次,并测量细胞的迁移距离,拍照记录并计算细胞迁移度,迁移度(%)=(划痕时两侧距离-检测时两侧距离)/划痕时两侧距离×100%。
1.5 统计学方法采用SPSS 24.0软件进行分析,数据以均数±标准差的形式表示,采用t检验进行组间比较,P<0.05为差异有统计学意义。
2 结果 2.1 U373MG细胞形态观察未经Corilagin干预的U373MG细胞,其状态良好,铺满孔底,紧密贴壁生长,并且细胞结构完整,胞体大致呈圆形、多角形、椭圆形等。而25、50、100、200μmol·L-1浓度Corilagin干预U373MG细胞后,随着药物浓度的升高或者干预时间的延长,U373MG细胞的形态逐渐发生变化,细胞有不同程度皱缩,细胞生长密度液逐渐降低,并可见大量散在的细胞碎片,细胞生长受到明显抑制。
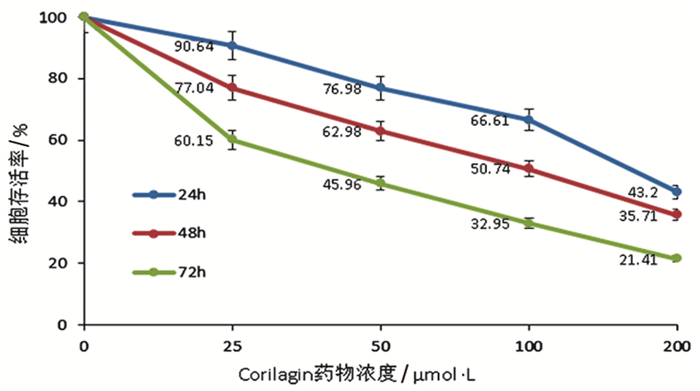
2.2 Corilagin对U373MG细胞增殖活性的影响U373MG细胞经不同浓度Corilagin干预24、48、72h后,经CCK-8试剂盒检测发现,在干预时间相同的条件下,与对照组相比,U373MG细胞的存活率随着Corilagin浓度的增加而逐渐降低,差异具有统计学意义(P<0.05);在药物浓度相同的条件下,与对照组相比,U373MG细胞的存活率随着Corilagin干预时间的延长逐渐降低,差异具有统计学意义(P<0.05)。见图 1。
|
图 1 Corilagin对U373MG细胞存活率的影响 |
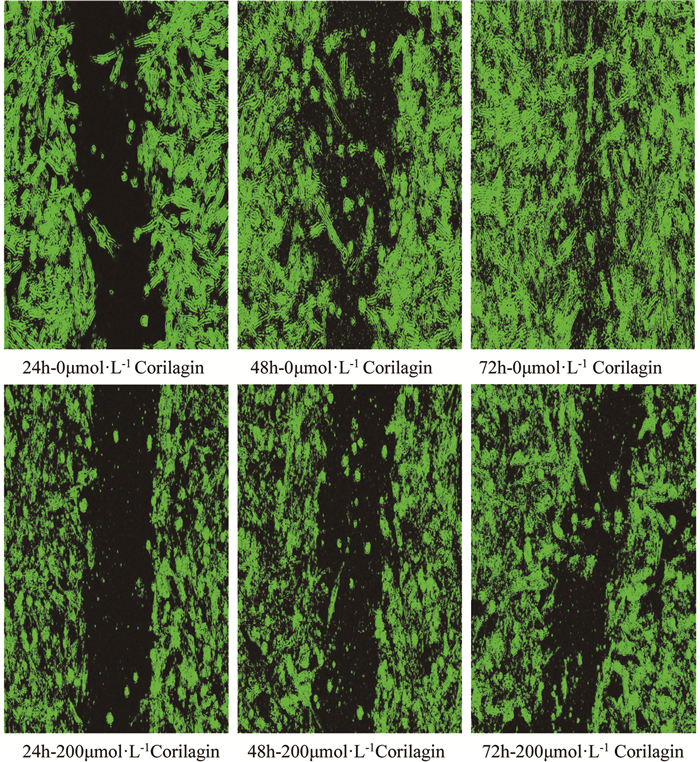
与对照组相比,在含200μmol·L-1 Corilagin血清培养基中培养24、48和72h后U373MG细胞的迁移度均明显降低,差异具有统计学意义(P<0.05)。见表 1、图 2。
| 表 1 两组U373MG细胞不同时间点迁移能力的比较 |
|
图 2 各组U373MG细胞迁移能力比较(×100) |
脑胶质瘤具有侵袭性强和复发率高的特点[6-7],经过手术切除后行化疗等标准治疗后,胶质瘤患者的生存期依旧很低[8],而且,治疗GBM的一线化疗药物TMZ已存在明显的耐药性[9],因此,目前急切需要一种新的化疗药物来替换或提高TMZ的疗效。Corilagin又名柯子次鞣素,属天然植物多酚单宁酸类化合物,分子式是C27H22O18,分子量634.46,为白色针晶状粉末,是蜜柑草总甙抗肿瘤作用的主要活性成分[10-11]。Corilagin具有多种药理作用,主要涉及抗肿瘤[3]、抗炎[4]、神经保护[5]等作用,应用前景良好,已有大量研究人员对其作用机制进行了密切关注及探索。
本文应用Corilagin干预胶质瘤U373MG细胞,发现随着药物浓度的增加或者干预时间的延长,Corilagin促使胶质瘤U373MG细胞的增殖活性逐渐降低;U373MG细胞划痕实验的迁移度降低,说明Corilagin能够有效抑制U373MG细胞的生长。通常细胞增殖与细胞程序性凋亡是正常的生理过程,并维持在一个平衡状态[12],如果能够打破细胞增殖与凋亡之间的平衡状态,那么就可对肿瘤的生长进行有效的干预[13],因而,可通过干涉细胞增殖及程序性凋亡等途径对肿瘤进行治疗[14]。本文结果显示,U373MG细胞在不受药物干预的情况下培养不同时间后进行CCK-8检测,细胞生长不受抑制; U373MG细胞在Corilagin干预下生长遭到抑制,U373MG细胞增殖活性与培养时间呈负性依赖关系。在药物浓度相同的条件下,Corilagin对U373MG细胞的抑制作用随着药物干涉时间的延长逐渐增强,并且细胞裂解也越严重。在干预时间相同的条件下,随着药物浓度的增加,Corilagin对U373MG细胞的抑制作用,以及细胞的裂解程度越来越明显。通过划痕实验证实,U373MG细胞在含有200 μmol·L-1 Corilagin的培养基中培养24、48和72h后,U373MG细胞的迁移度均明显低于对照组,说明Corilagin对U373MG细胞的生长具有明显的抑制作用。
综上所述,Corilagin能有效抑制人脑胶质瘤U373MG细胞的增殖活性和迁移能力,为Corilagin能否应用于胶质瘤的临床化学治疗提供一个新的实验依据。
| [1] |
Louis DN, Perry A, Reifenberger G, et al. The 2016 world health organization classification of tumors of the central nervous system:a summary[J]. Acta Neuropathol, 2016, 131(6): 803-820. DOI:10.1007/s00401-016-1545-1 |
| [2] |
Alphandéry E. Glioblastoma treatments:an account of recent industrial developments[J]. Front Pharmacol, 2018, 9: 879. DOI:10.3389/fphar.2018.00879 |
| [3] |
Ding YB, Huang LX, Chen J, et al. Corilagin attenuates the parkinsonismin japanese encephalitis virus induced parkinsonism[J]. Transl Neurosci, 2018, 9: 13-16. DOI:10.1515/tnsci-2018-0003 |
| [4] |
Tong YP, Zhang GY, Li Y, et al. Corilagin inhibits breast cancer growth via reactive oxygen species-dependent apoptosis and autophagy[J]. J Cell Mol Med, 2018. DOI:10.1111/jcmm.13647 |
| [5] |
Deng Y, Li XD, Li X, et al. Corilagin induces the apoptosis of hepatocellular carcinoma cells through the mitochondrial apoptotic and death receptor pathways[J]. Oncol Rep, 2018, 39(6): 2545-2552. DOI:10.3892/or.2018.6396 |
| [6] |
Liu P, Yu JY, Tian XY, et al. The effect of downregulation of Stathmin gene on biological behaviors of U373 and U87-MG glioblastoma cells[J]. Biol Res, 2018, 51(1): 16. DOI:10.1186/s40659-018-0160-0 |
| [7] |
Seystahl K, Wick W, Weller M. Therapeutic options in recurrent glioblastoma——An update[J]. Crit Rev Oncol Hematol, 2016, 99: 389-408. DOI:10.1016/j.critrevonc.2016.01.018 |
| [8] |
刘永吉, 魏明华, 张永斌, 等. 胶质母细胞瘤的治疗现状[J]. 中国保健营养, 2017, 27(17): 178-179. DOI:10.396/j.issn.1004-7484.2017.17.25 |
| [9] |
Milani R, Brognara E, Fabbri E, et al. Corilagin induces high levels of apoptosis in the temozolomide-resistant T98G glioma cell line[J]. Oncol Res, 2017. DOI:10.3727/096504017X14928634401187 |
| [10] |
刘阳, 靳峰. 柯里拉京在脑胶质瘤治疗中的应用前景[J]. 中国临床神经外科杂志, 2014, 19(7): 444-445. |
| [11] |
周广洲, 陈俊, 靳峰. 柯里拉京对人脑胶质瘤细胞U251生物学特性的影响[J]. 济宁医学院学报, 2018, 41(4): 246-249. DOI:10.3969/j.issn.1000-9760.2018.04.005 |
| [12] |
Li X, Deng Y, Zheng ZZ, et al. Corilagin, a promising medicinal herbal agent[J]. Biomed Pharmacother, 2018, 99: 43-50. DOI:10.1016/j.biopha.2018.01.030 |
| [13] |
Yang WT, Li GH, Li ZY, et al. Effect of corilagin on the proliferation and NF-κb in U251 glioblastoma cells and U251 glioblastoma stem-like cells[J]. Evid Based Complement Alternat Med, 2016, 2016: 1418309. DOI:10.1155/2016/1418309 |
| [14] |
Balça-Silva J, Matias D, Carmo AD, et al. Cellular and molecular mechanisms of glioblastoma malignancy:Implications in resistance and therapeutic strategies[J]. Semin Cancer Biol, 2018, S1044-S579X(18): 30072-5. DOI:10.1016/j.semcancer.2018.09.007 |



