基于荧光探针的荧光成像技术,能够实现对细胞活动可视化和实时监控,并具有灵敏度高、选择性好和无创伤等优点,在生命医学领域发挥着重要作用,已成为近几年研究的热点[1]。其中,近红外(near-infrared, NIR)荧光探针(吸收和发射波长在600~900 nm之间)因比短波长探针具有对生物样品光损伤小,不受样品自发荧光的干扰,且能穿透深层组织等显著优势而备受关注。随着荧光成像技术在药物输送及癌症诊断和治疗等生物医药领域的广泛应用,对NIR荧光探针的需求也日益增加,迫切需要开发更多新型结构和功能的NIR荧光染料[2]。
香豆素类荧光染料具有优异的光物理和化学性质,如荧光量子产率高、Stokes位移大、光稳定性好和易于修饰等,被广泛用于各种离子、活性物质的检测以及核酸和蛋白质分子的荧光标记[3]。但该类染料主要在短波长(400~520nm)区域发射,易受背景荧光的干扰,限制了其在活体成像中的应用。所以,对香豆素进行结构修饰,开发在NIR区域发射的香豆素类荧光染料具有重要的学术和应用价值。为此,化学家们付出了大量努力,已开发了许多新颖的香豆素类NIR荧光染料。本文将根据结构类型进行分类,对近几年报道的香豆素类NIR荧光染料及其应用进行归纳总结,为设计开发更多具有新型结构和功能的香豆素类NIR荧光染料提供参考。
1 含半花菁结构的NIR香豆素类荧光染料花菁染料是近些年备受青睐的大分子荧光标记和显像染料,具有摩尔吸光系数大、荧光性能良好等优点,但光稳定性较差是其一个严重的缺陷。花菁染料中带正电的半花菁部分作为优异的电子受体,被广泛用于新型荧光染料的开发。近些年,科研工作者将半花菁结构引入到香豆素中,开发出了大量新型的NIR香豆素-半菁类荧光染料,它们的结构见图 1,光学性质和应用见表 1。

|
图 1 含半花菁结构的NIR香豆素类荧光染料 |
| 表 1 含半花菁结构的NIR香豆素类荧光染料的光学性质与应用 |
香豆素-半菁类染料可通过不同的反应机制与各种离子、活性物质和生物大分子反应,从而产生荧光的变化,因此其可作为探针被广泛用于以上各种物质的检测和显像,并且具有选择性好、灵敏度高以及细胞渗透性好等优点。
如染料1和2通过氧化还原机制分别检测活体细胞中的·OH和ONOO-[4-5];染料3可通过与乙烯基的亲核加成实现环境和生物体内HSO3-/SO32-的定量检测,检测限低至27.6nM[6];染料4的硫酯衍生物5通过自然化学连接和环化级联反应,可用作高选择性检测半胱氨酸(Cys)的荧光探针[7];基于荧光共振能量转移(FRET)机制,染料6可作为比率型探针高选择性地检测线粒体中的H2S[8];染料7通过酸碱反应,可用作新的比率型pH敏感探针定量检测细胞内的pH分布[9];染料8和9在与G-四链体作用后,可用于G-四链体复合物的活体检测[10-11]。基于染料10设计的芳醚类化合物,可通过一个由酶引发的多米诺反应来实现对青霉素G酰基转移酶(PGA)的检测[12]。
另外,将香豆素与半菁结构结合,不仅能改善花菁部分的光稳定性,还能使香豆素的吸收和发射光谱显著向NIR区域移动。从表 1可知,这些染料均具有较大的发射波长和Stokes位移。它们的最大发射波长大多在630~720nm的NIR区域,Stokes位移大多在50~90nm,而化合物7和10b高达150nm和130nm。
对比图 1的结构不难发现,通过延长共轭链可以明显增大化合物的最大发射波长和Stokes位移,如染料7较染料1和2,染料10b较染料10a,最大发射波长和Stokes位移均有显著增大;但随着共轭链的增加,合成难度也会相应增大。通过在结构中引入一些水溶性基团,还可以明显改善染料的水溶性,如染料4和10,分别在结构中引入了羧基和磺酸基,大大提高了它们的水溶性。
总之,香豆素-半菁类染料以其优异的光学性质,较高的选择性和灵敏度,良好的细胞渗透性,多样的反应机制和易于修饰的优势,已被广泛用于生物检测和成像,相信未来会有更多反应机制和新型结构的此类染料会被设计开发出来。
2 共轭刚性环并香豆素类NIR荧光染料将共轭刚性环引入到荧光母体中,往往能增大其发射波长,增强光稳定性和提高荧光量子效率。科研工作者在香豆素的结构中并入共轭刚性环,合成了一些具有优异光学性质的共轭刚性环并香豆素类NIR荧光染料。它们的结构见图 2,光学性质和应用见表 2。

|
图 2 共轭刚性环并香豆素类NIR荧光染料 |
| 表 2 共轭刚性环并香豆素类NIR荧光染料的光学性质及应用 |
Wang课题组[13-14]将派洛宁Y结构并入到香豆素中,设计合成了多个半月形(Crescent-shape)香豆素类NIR荧光染料11和12;随后,该课题组又在结构中引入羧酸,合成了水溶性NIR染料13[15]。Huang等[16]将苯并咪唑结构并入亚氨基香豆素结构合成了新型结构NIR荧光染料14。
从表 2可以看出,染料11、12、13的最大发射波长在640~690nm的NIR区域,Stokes位移介于53~78nm之间;结构分析可以发现,当香豆素7-位氮上连有环状结构时,其最大发射波长和Stokes位移都要大于连二甲基时。基于苯并咪唑和亚氨基香豆素结构设计的染料14,虽然Stokes位移较染料11、12、13有所减小,其最大发射波长却高达715nm以上,这种结构为合成含多种功能基团的NIR荧光染料提供一个新的思路。
细胞成像实验证明,染料11、12和13适用于活细胞中线粒体、溶酶体以及核仁RNA的成像,并具有优异的光稳定性、良好的细胞通透性和较低的细胞毒性。其中,染料12b通过与核仁RNA结合,能快速染色活细胞核仁,比核仁色素SYTO RNASelect,更高的光稳定性和选择性,具有非常好的应用前景。
3 含有二氟硼络合物结构的香豆素NIR染料二氟硼结构是强缺电子体系,是非常好的电子受体。以二氟硼结构为母体的分子大都具有优良的光物理和光化学性能。如二吡咯甲川(BODIPY)是其中的杰出代表,但它们的缺点是Stokes位移一般较小(15~30nm)。将二氟硼结构引入香豆素,一些近红外发射的二氟硼-香豆素类染料相继被开发出来,其结构见图 3,光学性质见表 3。
|
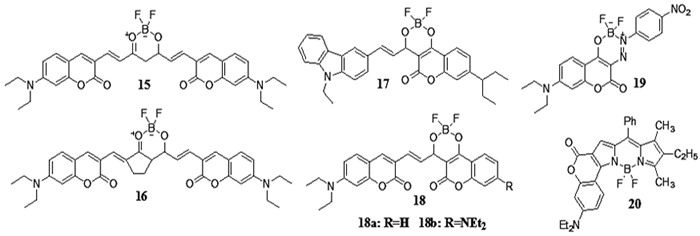
图 3 含有二氟硼络合物结构的香豆素NIR染料 |
| 表 3 含有二氟硼络合物结构的香豆素NIR染料的光学性质 |
其中,Sekar课题组在二氟硼-香豆素类NIR染料的开发中做了大量工作,如他们基于姜黄素结构,合成了含有二氟硼结构的双香豆素染料15和16[3];将二氟硼和咔唑环引入到香豆素结构中合成了染料17[17];将二氟硼和查耳酮结构引入到香豆素中,合成了染料18[18];将芳基偶氮(Ar-N=N-)和二氟硼引入香豆素中,合成了染料19[19]。Bochkov等[20]将香豆素并入BODIPY中,合成了一系列新型不对称香豆素并BODIPY的NIR染料20。
从表 3可以看出,这些染料具有优异的光学性质,特别是Stokes位移较BODIPY类化合物有着显著增大,大都在90nm以上,而化合物20高达144nm。它们的最大发射波长均在640nm以上,化合物20和16甚至达到750和780nm。从图 3中的结构可以发现,染料最大发射波长与连接两个芳环的共轭链长度有关,如染料15和16的最大发射波长明显大于17,18和19。
虽然二氟硼-香豆素类NIR染料具有较大的最大发射波长和Stokes位移,但在极性溶剂中极低的荧光量子产率限制了其在生物检测和成像方面的应用,未来如能解决这一缺陷,相信这类染料会有很大的应用空间。
4 含多个氰基的香豆素类NIR荧光染料氰基作为一个强吸电子基团,是荧光染料中常用的电子受体。在香豆素3-位通过共轭双键引入多氰基基团,而在7-位引入给电子基如羟基和二乙胺基,可通过分子内电荷转移(ICT)实现香豆素发射光谱的红移。
如图 4所示,Li课题[21-22]组分别将丙二腈和2, 2, 3-三甲基-4-氰基-5(二氰基亚甲基)-2, 5-二氢呋喃结构通过共轭双键引入到香豆素的3-位,先后设计合成了NIR荧光染料21和22,可分别用作检测SO32-和SO2衍生物的比率和比色荧光探针。Tathe等[23]在香豆素的3位引入苯并噻唑乙腈或苯并噁唑乙腈,在4位引入氰基,合成了NIR荧光染料23a和23b。Shreykar等[24]最近将4-羟基香豆素与噻唑环通过共价连接,合成了NIR荧光染料24,噻唑环同时与作为电子供体的吗啉环和作为受体的含丙二腈的共轭刚性环相连。

|
图 4 含多个氰基的NIR香豆素荧光染料 |
从表 4可以发现,这些染料大都具有超过650nm的最大发射波长和非常大(>90nm)的Stokes位移,染料22b和24甚至能达到149和150nm。对比它们的结构可以发现,随着共轭体系的增大,化合物的最大发射波长也相应发生红移,如染料21、22和24的最大发射波长依次增大;而Stokes位移与共轭体系大小无直接联系。Tathe等[23]通过计算证实,在香豆素4-位引入氰基会使分子发射光谱发生明显红移。
| 表 4 含多个氰基的NIR香豆素荧光染料的光学性质与应用 |
目前,染料21,22仅用作检测SO32-和SO2衍生物荧光探针,具有选择性好,灵敏度高和低毒性等特点,其检测机制与香豆素-半菁染料3一致,均通过与乙烯基的亲核加成反应来实现荧光的改变;而染料23和24还没有其应用方面的报道。今后对这类染料进行合理设计,如在香豆素7-位引入羟基,然后进行酯化或成醚,有望实现对其他活性物质如H2S、酶等的检测和成像。
5 基于罗丹明或苯并吡喃鎓结构的NIR香豆素类荧光染料罗丹明和苯并吡喃鎓类荧光染料具有对光稳定性好、较宽的波长范围和较高的荧光量子产率等优点,被广泛应用于生物医学领域的荧光检测和标记。为开发更多新型结构和优异性能的荧光染料,科研工作者将香豆素引入到这两种结构中,开发了几种基于罗丹明或苯并吡喃鎓结构的NIR香豆素类荧光染料,其结构见图 5,光学性质和应用见表 5。
|
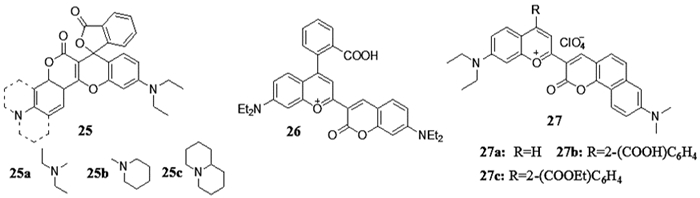
图 5 基于罗丹明或苯并吡喃鎓结构的NIR香豆素荧光染料 |
| 表 5 基于罗丹明或苯并吡喃鎓结构的NIR香豆素荧光染料的光学性质与应用 |
如Chen等[25]将香豆素并入罗丹明分子骨架中,开发了新型深红色荧光染料25。25酯化得到的化合物可以选择性地染色线粒体和检测Hg2+。Dai等[26]基于香豆素和苯并吡喃鎓盐结构,开发了对肼有高选择性和敏感性的NIR比率荧光探针26,对肼的检测限为1.5ppb,并成功地用于胎牛血清和活体细胞中肼的成像。Niu等[1]将基于香豆素和苯并吡喃鎓盐,构建了三个新的NIR荧光染料27a-27c。从表 5可知,基于罗丹明结构的染料25最大发射波长在640~690nm之间,Stokes位移介于50~75nm之间,其最大发射波长和Stokes位移随香豆素7-位氮原子上刚性环的个数增加而变大。基于苯并吡喃鎓的香豆素类染料的光学性质受结构影响更为明显,在香豆素上多一个苯环的染料27,其最大发射波长和Stokes位移分别达到814和148nm以上,比染料26分别增大120nm和100nm以上,27是目前已知香豆素染料中拥有最长发射波长的化合物,为以后设计此类NIR染料提供了重要的参考。
细胞成像实验表明,这两类染料都显示了良好的耐光性和较低的细胞毒性,其中染料25比市售染料MitoTracker具有更好的光学性质和更低的细胞毒性,表明这些染料在活体成像中具有良好的开发潜力和应用前景。
6 总结与展望综上所述,香豆素优异的光学性质和易于修饰的结构特点,使得香豆素类染料一直是研究开发的热点。根据不同的合成策略,引入不同的基团,近些年已有许多不同结构类型的香豆素类NIR荧光染料被相继开发出来,并被应用到各种小分子、离子、活性粒子、pH的检测和细胞成像上。目前来看,香豆素-半菁染料是研究最多和应用最广的一类化合物;而二氟硼-香豆素类NIR染料虽具有优异的光学性质,但在极性溶剂中较低的荧光量子产率限制了其在生物检测和成像中的应用。随着更多新型NIR荧光染料的涌现,将它们与香豆素结构相融合,相信未来会有更多结构新颖和性能良好的香豆素类NIR荧光染料会被开发出来。
| [1] | Niu GL, Liu WM, Xiao HY, et al. Keto-benzo[h]-coumarin-based near-infrared dyes with large stokes shifts for bioimaging applications[J]. Chem Asian J, 2016, 11(4): 498–504. DOI:10.1002/asia.201501026 |
| [2] | Yang GB, Liu JJ, Wu YF, et al. Near-infrared-light responsive nanoscale drug delivery systems for cancer treatment[J]. Coordin Chem Rev, 2016, 320: 100–117. DOI:10.1016/j.ccr.2016.04.004 |
| [3] | Margar SN, Sekar N. Red and near-infrared emitting bis-coumarin analogues based on curcumin framework-synthesis and photophysical studies[J]. J Photoch Photobio A, 2016, 327: 58–70. DOI:10.1016/j.jphotochem.2016.05.009 |
| [4] | Yuan L, Lin WY, Song JZ. Ratiometric fluorescent detection of intracellular hydroxyl radicals based on a hybrid coumarin-cyanine platform[J]. Chem Commun, 2010, 46(42): 7930–7932. DOI:10.1039/c0cc02390f |
| [5] | Zhou X, Kwon Y, Kim G, et al. A ratiometric fluorescent probe based on a coumarin-hemicyanine scaffold for sensitive and selective detection of endogenous peroxynitrite[J]. Biosens Bioelectron, 2015, 64: 285–291. DOI:10.1016/j.bios.2014.08.089 |
| [6] | Xiang KQ, Chang SZ, Feng JG, et al. A colorimetric and ratiometric fluorescence probe for rapid detection of SO2 derivatives bisulfite and sulfite[J]. Dyes Pigments, 2016, 134: 190–197. DOI:10.1016/j.dyepig.2016.07.001 |
| [7] | Liu J, Sun YQ, Zhang HX, et al. A carboxylic acid-functionalized coumarin-hemicyanine fluorescent dye and its application to construct a fluorescent probe for selective detection of cysteine over homocysteine and glutathione[J]. RSC Adv, 2014, 4(110): 64542–64550. DOI:10.1039/c4ra10865e |
| [8] | Feng X, Zhang T, Liu JT, et al. A new ratiometric fluorescent probe for rapid, sensitive and selective detection of endogenous hydrogen sulfide in mitochondria[J]. Chem Commun, 2016, 52(15): 3131–3134. DOI:10.1039/c5cc09267a |
| [9] | Liu XD, Xu Y, Sun R, et al. A coumarin-indole-based near-infrared ratiometric pH probe for intracellular fluorescence imaging[J]. Analyst, 2013, 138(21): 6542–6550. DOI:10.1039/c3an01033c |
| [10] | Yan JW, Chen SB, Liu HY, et al. Development of a new colorimetric and red-emitting fluorescent dual probe for G-quadruplex nucleic acids[J]. Chem Commun, 2014, 50(52): 6927–6930. DOI:10.1039/c4cc01472c |
| [11] | Yan JW, Tian YG, Tan JH, et al. Colorimetric and fluorescence detection of G-quadruplex nucleic acids with a coumarin-benzothiazole probe[J]. Analyst, 2015, 140(21): 7146–7149. DOI:10.1039/c5an01573a |
| [12] | Richard JA, Massonneau M, Renard PY, et al. 7-Hydroxycoumarin-hemicyanine hybrids:A new class of far-red emitting fluorogenic dyes[J]. Org Lett, 2008, 10(19): 4175–4178. DOI:10.1021/ol801582w |
| [13] | Zhou B, Liu W, Zhang H, et al. Imaging of nucleolar RNA in living cells using a highly photostable deep-red fluorescent probe[J]. Biosens Bioelectron, 2015, 68: 189–196. DOI:10.1016/j.bios.2014.12.055 |
| [14] | Liu WM, Zhou BJ, Niu GL, et al. Deep-red emissive crescent-shaped fluorescent dyes:substituent effect on live cell imaging[J]. ACS Appl Mater Interfaces, 2015, 7(13): 7421–7427. DOI:10.1021/acsami.5b01429 |
| [15] | Li Q, Liu WM, Wu JS, et al. Deep-red to near-infrared fluorescent dyes:Synthesis, photophysical properties, and application in cell imaging[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2016, 164: 8–14. DOI:10.1016/j.saa.2016.03.042 |
| [16] | Huang ST, Jian JL, Peng HZ, et al. The synthesis and optical characterization of novel iminocoumarin derivatives[J]. Dyes Pigments, 2010, 86(1): 6–14. DOI:10.1016/j.dyepig.2009.10.020 |
| [17] | Tathe AB, Sekar N. Red-emitting NLOphoric carbazole-coumarin hybrids-Synthesis, photophysical properties and DFT studies[J]. Dyes Pigments, 2016, 129: 174–185. DOI:10.1016/j.dyepig.2016.02.026 |
| [18] | Tathe AB, Sekar N. NLOphoric red emitting bis coumarins with O-BF2-O core-synthesis, photophysical properties and DFT Studies[J]. J.Fluoresc., 2016, 26(2): 471–486. DOI:10.1007/s10895-015-1733-8 |
| [19] | Tathe AB, Sekar N. Red emitting coumarin-azo dyes:Synthesis, characterization, linear and non-linear optical properties-experimental and computational approach[J]. J Fluoresc, 2016, 26(4): 1279–1293. DOI:10.1007/s10895-016-1815-2 |
| [20] | Bochkov AY, Akchurin IO, Dyachenko OA, et al. NIR-fluorescent coumarin-fused BODIPY dyes with large Stokes shifts[J]. Chem Commun, 2013, 49(99): 11653–11655. DOI:10.1039/c3cc46498a |
| [21] | Wu MY, He T, Li K, et al. A real-time colorimetric and ratiometric fluorescent probe for sulfite[J]. Analyst, 2013, 138(10): 3018–3025. DOI:10.1039/c3an00172e |
| [22] | Wu MY, Li K, Li CY, et al. A water-soluble near-infrared probe for colorimetric and ratiometric sensing of SO2 derivatives in living cells[J]. Chem Commun, 2014, 50(2): 183–185. DOI:10.1039/c3cc46468g |
| [23] | Tathe AB, Gupta VD, Sekar N. Synthesis and combined experimental and computational investigations on spectroscopic and photophysical properties of red emitting 3-styryl coumarins[J]. Dyes Pigments, 2015, 119: 49–55. DOI:10.1016/j.dyepig.2015.03.023 |
| [24] | Shreykar MR, Sekar N. Resonance induced proton transfer leading to NIR emission in coumarin thiazole hybrid dyes:Synthesis and DFT insights[J]. Tetrahedron Lett, 2016, 57(37): 4174–4177. DOI:10.1016/j.tetlet.2016.07.097 |
| [25] | Chen JH, Liu WM, Zhou BJ, et al. Coumarin-and rhodamine-fused deep red fluorescent dyes:Synthesis, photophysical properties, and bioimaging in vitro[J]. J Org Chem, 2013, 78(12): 6121–6130. DOI:10.1021/jo400783x |
| [26] | Dai X, Wang ZY, Du ZF, et al. A simple but effective near-infrared ratiometric fluorescent probe for hydrazine and its application in bioimaging[J]. Sensor Actuat B Chem, 2016, 232: 369–374. DOI:10.1016/j.snb.2016.03.159 |



