2. 济宁医学院附属医院, 济宁 272029
2. The Affiliated Hospital of Jining Medical University, Jining 272029, China
胶质母细胞瘤(glioblastoma,GBM)是目前最常见的颅内恶性肿瘤,多发于神经外胚层,占颅内肿瘤的40%~50%[1]。该肿瘤增殖速度快、浸润性生长和术后易复发,即使在成功切除、放疗和化疗(替莫唑胺)治疗后,肿瘤复发率仍然很高,导致治疗效果非常差[2]。柯里拉京(Corilagin)具有抗肿瘤[3]、抗炎[4]和保肝作用[5]等。然而,由于复杂而低效的提取方法,它的药理性能很少受到关注。近年来,随着萃取技术的发展,Corilagin比以往更容易获得。因此,人们开始重新关注其抗肿瘤、保肝和抗炎活性。本实验通过在不同时间点分别用200μg/ml Corilagin干预胶质瘤细胞, 分析Corilagin对人脑胶质瘤U251细胞的影响,为胶质瘤的进一步药物治疗提供新的研究思路。
1 材料与方法 1.1 材料U251细胞系(中国典型培养物保藏中心); DMEM/F12(上海博升生物科技有限公司); 胎牛血清(浙江天杭生物科技股份有限公司); PBS缓冲液(普诺赛生命科技有限公司); 双抗(美国Solarbio公司); 胰蛋白酶(美国Gibco公司); DMSO(美国Sigma公司); 柯里拉京(美国Sigma公司); 细胞凋亡检测试剂盒(碧云天生物技术研究所)。
1.2 U251细胞培养取出U251细胞系放在含有DMEM/F12和10%FBS的细胞完全培养基中,在37℃,5%CO2的饱和湿度的恒温细胞培养箱中进行培养。培养基每1~2天更新1次。
1.3 凋亡试剂盒检测细胞凋亡将细胞接种到6孔板中,实验组每孔加2ml配制的含200μg/ml Corilagin的培养基,对照组每孔加入2ml完全培养基,分别干预24、48、72h,每组都设3个复孔,培养结束后,根据凋亡试剂盒说明书上的程序对细胞进行染色,染色完成即通过流式细胞仪进行检测, 其中AnnexinV-FITC显示为绿色荧光, PI显示为红色荧光。记录AnnexinV-FITC(+)PI(+)和AnnexinV-FITC(+)PI(-)作为凋亡细胞, 每次计数10000个细胞, 计算各组凋亡率。
1.4 细胞划痕实验在恒温箱中取出接种于6孔板生长良好的胶质瘤U251细胞,吸尽培养液后,用直尺在6孔板背后用记号笔均匀画横线,用无菌10μl移液管头与标尺比齐,尽可能在6孔板后方的水平线上均匀划行;用200μg/ml药物浓度的柯里拉京干预细胞3个时间点(24、48、72h),每组设置5个平行孔;最终将6孔板放置于荧光倒置显微镜下观察细胞迁移情况;测量并记录细胞迁移距离;细胞迁移度(%)=(划痕时两侧细胞距离-检测时两侧细胞距离)/划痕时两侧细胞距离×100%。
1.5 统计学方法采用SPSS 19.0软件进行数据分析。
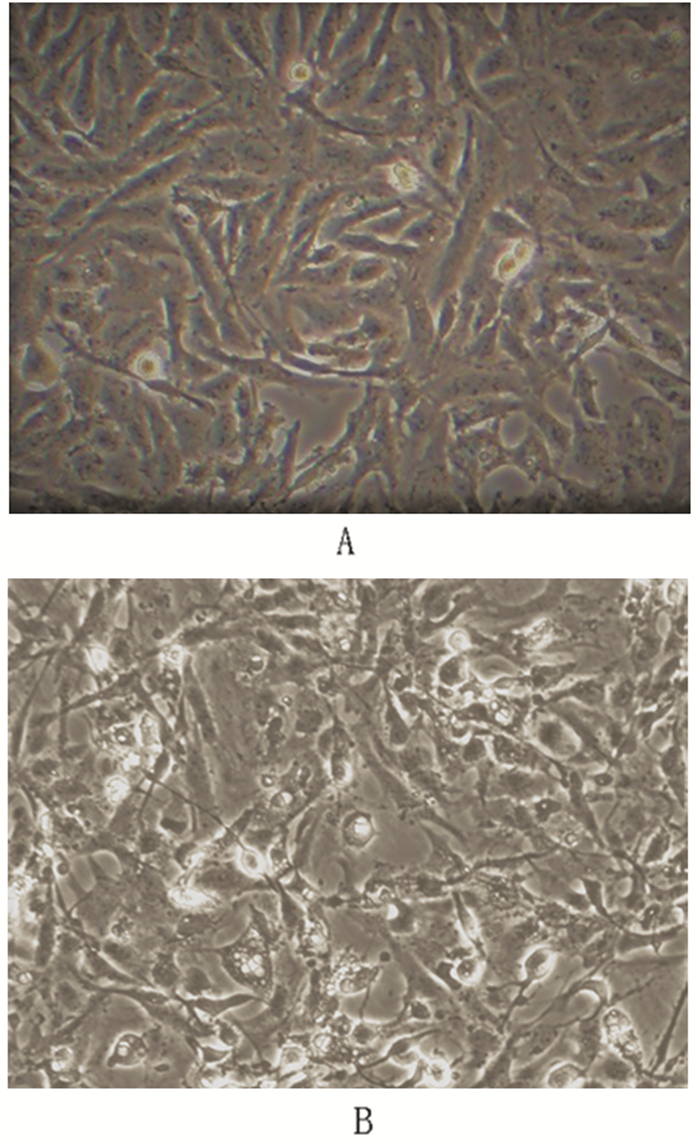
2 结果 2.1 U251细胞形态观察在恒温箱中分别取出接种于6孔板生长良好的胶质瘤U251细胞,分别用不同药物浓度的Corilagin 3个不同时间点(24、48、72h)干预细胞,然后放在荧光倒置显微镜下观察,可以发现未经Corilagin干预的U251细胞生长良好,具有完整的细胞结构,并附着于6孔板的壁上(见图 1A)。200μg/ml Corilagin干预72h后,细胞变小,细胞密度减少,细胞碎片增多,细胞凋亡增加(见图 1B)。
|
图 1 200μg/ml Corilagin对U251细胞的影响(×100) 注:A, 正常培养的U251;B, 200μg/ml Corilagin干预U251细胞72h |
U251细胞经200μg/ml的Corilagin干预24、48、72h后,经凋亡试剂盒检测发现,在200μg/ml浓度干预下,U251细胞凋亡率随Corilagin干预时间的延长而增高(P<0.05)。见表 1。
| 表 1 两组U251细胞不同时间点细胞凋亡率比较(%) |
Corilagin能抑制U251细胞的迁移能力,与对照组相比,200μg/ml Corilagin能明显降低U251细胞的迁移度。划痕后的U251细胞在含200μg/ml Corilagin血清培养基中培养24、48、72h后U251细胞迁移度均低于对照组,差异有统计学意义(均P<0.05)。见图 2、表 2。

|
图 2 200μg/ml Corilagin对U251细胞迁移能力的影响(×100) |
| 表 2 两组U251细胞不同时间点迁移能力的比较(x±s) |
胶质瘤是一种最常见的脑肿瘤类型,具有侵袭性强和复发率高的特点[6],尽管经过手术、化疗、放疗等综合治疗后,胶质瘤患者的中位生存期仍仅有18个月[7]。为提高胶质瘤患者的临床治疗效果,目前迫切需要一种新的治疗方法来替代传统的手段。根据肿瘤增殖/凋亡理论[8],肿瘤的形成跟细胞增殖与凋亡的失衡有很大关系,因此,探索诱导肿瘤细胞凋亡的相关药物及其作用靶点,能够为恶性肿瘤的治疗提供新的思路和实验依据。
本文应用Corilagin干预神经胶质瘤U251细胞,发现随着药物干预时间延长,Corilagin促使胶质瘤U251细胞的凋亡率逐渐增高,胶质瘤U251细胞的迁移度降低,说明Corilagin能够抑制胶质瘤U251细胞的生长。细胞凋亡是由基因控制的细胞程序性死亡过程,它对哺乳动物的发育和维持机体平衡方面起着关键作用[9],它可以消除任何不必要或不需要的细胞,并且这是一个受到严格控制的过程。有多种因素可导致凋亡途径被激活,包括DNA损伤或不受控制的增殖[10]。细胞凋亡有细胞内和细胞外两种途径激活。细胞内途径激活信号包括DNA损伤、生长因子剥夺和细胞因子剥夺,最常见的细胞外途径激活信号是由受损或感染的细胞免疫系统的细胞毒性T细胞产生的死亡诱导信号来介导[11]。对于Corilagin促进胶质瘤U251细胞凋亡及抑制其迁移的机制尚不十分明确。Livin(又称KIAP或ML-IAP)是细胞凋亡蛋白抑制因子家族中的一员。该蛋白在细胞凋亡、细胞增殖和细胞周期中起关键作用。Livin在胶质瘤U251细胞中的表达显著高于人脑胶质细胞[12]。Corilagin可能通过抑制Livin的表达从而促进U251细胞凋亡。研究发现,基质金属蛋白酶(matrix metalloproteinases,MMPs)通过对细胞外基质中的各种蛋白的分解,破坏体内的组织学屏障,从而使胶质瘤更容易浸润和转移[13],因此,抑制胶质瘤细胞侵袭及扩散的方法就是首先要抑制肿瘤细胞中MMPs的活性。已经有研究发现,中草药提取物Corilagin能够有效抑制MMPs的活性,可以显著抑制胶质瘤在体内迁移和扩散[14]。但是Corilagin作为一种新药,关于其对胶质瘤U251细胞的确切分子机制尚不完全清楚,还需要进一步探索。
综上所述,Corilagin能促进人脑胶质瘤U251细胞的凋亡,并抑制其迁移能力,说明Corilagin对胶质瘤细胞具有较强的细胞毒作用。该结论补充了胶质瘤细胞的凋亡、耐药理论,揭示了新型化疗药物Corilagin对胶质瘤细胞生物学特性的影响。尽管本研究还存在一定的局限性,但是Corilagin的上述作用为胶质瘤的治疗拓宽了思路,对恶性胶质瘤的临床治疗提供了理论依据。
| [1] | Madany M, Thomas TM, Edwards L, et al. Immunobiology and immunotherapeutic targeting of glioma stem cells[J]. Adv Exp Med Biol, 2015, 853: 139–166. DOI:10.1007/978-3-319-16537-0_8 |
| [2] | 刘永吉, 魏明华, 张永斌, 等. 胶质母细胞瘤的治疗现状[J]. 中国保健营养, 2017(17): 178–179. DOI:10.3969/j.issn.1004-7484.2017.17.257 |
| [3] | Jia L, Jin H, Zhou J, et al. A potential anti-tumor herbal medicine, Corilagin, inhibits ovarian cancer cell growth through blocking the TGF-beta signaling pathways[J]. BMC Complement Altern Med, 2013, 13: 33. DOI:10.1186/1472-6882-13-33 |
| [4] | Jin F, Cheng D, Tao JY, et al. Anti-inflammatory and anti-oxidative effects of corilagin in a rat model of acute cholestasis[J]. BMC Gastroenterol, 2013, 13: 79. DOI:10.1186/1471-230X-13-79 |
| [5] | Cheng JT, Lin TC, Hsu FL. Antihypertensive effect of corilagin in the rat[J]. Can J Physiol Pharmacol, 1995, 73(10): 1425–1429. DOI:10.1139/y95-198 |
| [6] | 汪翔, 周修明, 张协军, 等. STAT3信号通路在恶性脑胶质瘤中的研究进展[J]. 中华神经医学杂志, 2016(3): 245–250. DOI:10.3760/cma.j.issn.1671-8925.2016.03.006 |
| [7] | 杨凯元, 任晓辉, 林松. 生酮饮食疗法在脑胶质瘤治疗中的研究现状[J]. 中华神经外科杂志, 2018(1): 94–97. DOI:10.3760/cma.j.issn.1001-2346.2018.01.022 |
| [8] | Lopes RB, Gangeswaran R, Mc Neish IA, et al. Expression of the IAP protein family is dysregulated in pancreatic cancer cells and is important for resistance to chemotherapy[J]. Cancer, 2007, 120(11): 2344–2352. DOI:10.1002/ijc.22554 |
| [9] | 李帅, 张炳东. 细胞凋亡途径的研究进展[J]. 山东医药, 2017(37): 103–106. DOI:10.3969/j.issn.1002-266X.2017.37.036 |
| [10] | Lopez J. Mitochondrial apoptosis:killing cancer using the enemy within[J]. British journal of cancer, 2015, 112(6): 957–962. DOI:10.1038/bjc.2015.85 |
| [11] | Zaman S, Wang R. Targeting the apoptosis pathway in hematologic malignancies[J]. Leukemia&lymphoma, 2014, 55(9): 1980–1992. DOI:10.3109/10428194.2013.855307 |
| [12] | Jin F, Zhao L, Guo YJ, et al. Influence of Etoposide on anti-apoptotic and multidrug resistance-associated protein genes in CD133 positive U251 glioblastoma stem-like cells[J]. Brain research, 2010, 1336: 103–111. DOI:10.1016/j.brainres.2010.04.005 |
| [13] | Roomi MW, Kalinovsky T, Niedzwiecki A. Modulation of uPA, MMPs and their inhibitors by a novel nutrient mixture in human glioblastoma cell lines[J]. Int J Oncol, 2014, 45(2): 887–894. DOI:10.3892/ijo.2014.2465 |
| [14] | Ulasov I, Thaci B, Sarvaiya P, et al. Inhibition of MMP14 potentiates the therapeutic effect of temozolomide and radiation in gliomas[J]. Cancer Med, 2013, 2(4): 457–467. DOI:10.1002/cam4.104 |



