2. 济宁医学院药学院;
3. 日照市120紧急救援指挥中心, 日照 276826
2. College of Pharmacy, Jining Medical University;
3. 120 Emergency Rescue Command Center of Rizhao City, Rizhao 276826, China
近年,经皮冠状动脉腔内成形术、冠脉搭桥术等缺血-再灌注治疗手段增多,心肌缺血-再灌注(ischemia-reperfusion,IR)损伤备受关注[1]。红花(Carthamus tinctorius L)可通过清除自由基、增强酶的活性、扩张血管等方面起到抗心肌缺血作用[2]。本实验通过结扎右冠状动脉建立心肌缺血动物模型,并从心肌酶检测、BCL-2蛋白表达、心肌梗死面积测量及病理切片镜像改变等方面研究红花对心肌缺血-再灌注损伤的保护作用。
1 材料与方法 1.1 材料 1.1.1 试剂氯化三苯四唑啉(上海化学试剂厂); BCL-2免疫试剂盒(武汉博士德生物工程有限公司); 红花注射液(亚宝药业集团股份有限公司)。
1.1.2 仪器心电图机(ECG-1150日本);OLYMPUS显微镜(TOKYO日本);LX20全自动生化分析仪(Beckman-Couher美国);病理切片机(美国AO公司)。
1.1.3 实验动物及分组健康兔30只,实验过程中死亡7只, 补7只, 共37只,体重2.0~2.5kg, 雌雄不拘,济宁医学院动物房提供,动物许可证号:SCXK(鲁)2014-0007,实验动物符合实验动物福利和动物伦理学的要求。
动物随机分为3组,每组10只,假手术组,在右冠状动脉下穿无创伤丝线,但不结扎;缺血-再灌注损伤组,缺血30min,再灌注120min;红花组为红花注射液在缺血前30min,2ml/kg耳缘静脉注射,缺血30min,再灌注120min。
1.2 方法 1.2.1 兔心肌缺血-再灌注模型建立20%乌拉坦5ml/kg兔耳缘静脉缓慢注入,兔呼吸慢而平稳、肌张力下降且角膜反射消失即表示麻醉成功。随后将兔仰卧于手术台上将四肢和上颚固定,胸前剪毛。先沿胸骨中线右侧逐层剪开皮肤、皮下组织,可见肋骨,再沿肋骨右缘剪断3~5根肋骨,撑开胸腔,暴露心脏。观察到心脏跳动有力,右肺略有萎缩,用镊子轻夹起心包膜后剪开2cm左右的开口,牵拉右心耳,暴露右房室间沟。在距右房室间沟约5mm处右心室壁上可见右冠状动脉。将无创伤缝合线环绕右冠状动脉,将该缝合线从自制皮管内穿出置于体外,迅速缝合关胸。用针管从自制皮管中抽气,使右肺膨胀,抽紧环绕线造成右冠状动脉缺血,用止血钳夹住皮管,防止空气进入胸腔,观察呼吸是否平稳、心率是否正常。逐层将胸腔和表皮缝合,缺血30min,心电图机行心电监护,随后松开环绕线恢复心肌灌注120min。在心肌再灌注2h后从心脏取血,测定CK和LDH含量。取出心脏,在右心室前壁取1.2cm×1.5cm心肌,备用做病理切片,每组5个心脏冷藏后取出做心脏切片观察心肌梗死面积。红花组红花注射液在缺血前30min,2ml/kg耳缘静脉注射,假手术组、缺血-再灌注损伤组在缺血前30min注射等量生理盐水。
1.2.2 心电图观测采用ECG-1150心电图机对各组兔做心电图。以针刺电极插于兔四肢皮下,全程监测标准肢体Ⅱ导联心电图。再灌注后ST值均有降低,降低的ST值称为ST回落值,即ΔST值(ΔST=结扎后30min ST值-复灌后ST值)。
1.2.3 心肌酶检测再灌注2h后从心脏取血,用LX20全自动生化分析仪(美国)检测心肌酶含量,包括CK、LDH,速率法检测。
1.2.4 心肌梗死范围观测1) 取材动物缺血-再灌注后取出心脏生理盐水冲洗后放置冰箱冷藏。2)心肌梗死范围观测取兔冷藏心脏,每组各取5只,去除心房,沿水平方向将心室肌切成约2~3mm的圆薄片,用滤纸将心肌薄片吸干,置于37℃的1%氯化三苯四唑啉磷酸缓冲液(pH=7.4)内,水浴15~30 min,确定梗死组织面积,观察梗死区域(灰白色)和正常心肌区域(红色)面积。
心肌损伤观测:1)取材动物缺血-再灌注后取心脏,在右心室前壁上取1.2cm×1.5cm的心肌。2)固定把取出的标本放入4%多聚甲醛缓冲液中6~8h。3)染色石蜡包埋HE染色。4)拍照用OLYMPUS光学显微镜观察,明美数码成像系统拍照。
1.2.5 检测BCL-2蛋白阳性细胞数采用HP IAS-1000高清晰度彩色病理图文分析系统,于200倍光镜下选择血肿周围阳性细胞表达明显区域的3个相邻视野区,计数阳性细胞数,计算平均值。
1.3 统计学方法采用统计软件SPSS 13.5分析实验数据。
2 结果 2.1 各组兔心电图变化与假手术组相比,缺血-再灌注损伤组心电图ST段抬高,差异有统计学意义(P<0.05);与缺血-再灌注损伤组相比,红花组心电图ST段抬高降低,差异有统计学意义(P<0.05)。见表 1。
| 表 1 3组心电图ST段高度值比较(x±s) |
与假手术组相比,缺血-再灌注损伤组CK和LDH水平增加, 差异有统计学意义(P<0.05);与缺血-再灌注损伤组相比,红花组CK和LDH水平显低, 差异有统计学意义(P<0.05)。见表 2。
| 表 2 3组心肌酶检测数值比较(x±s,U/L) |
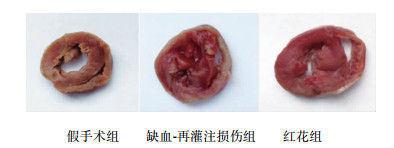
假手术组右心室无梗死发白,缺血-再灌注损伤组右心室梗死发白较明显,红花组与缺血-再灌注损伤组比较右心室梗死发白减轻。见图 1。
|
图 1 3组兔心肌梗死检测结果 |
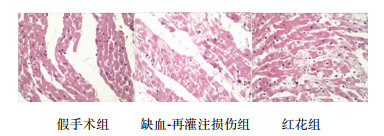
缺血-再灌注损伤组梗死区部分毛细血管扩张,细胞出现空泡,模糊不清晰,细胞核颜色变浅,细胞质出现肿胀,纤维排列不规则,红花组出现轻微的血管充血,较少出现细胞固缩、形态结构改变。见图 2。
|
图 2 3组兔心肌细胞形态 |
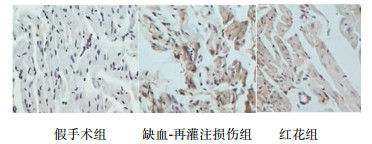
与假手术组相比,缺血-再灌注损伤组BCL-2蛋白阳性细胞数增多,与缺血-再灌注损伤组相比,红花组BCL-2蛋白阳性细胞数显著减少。见表 3、图 3。
| 表 3 3组心肌组织BCL-2蛋白阳性细胞数比较(x±s) |
|
图 3 各组兔BCL-2蛋白表达情况(×200) |
缺血-再灌注损伤可发生于溶栓、经皮穿刺冠状动脉腔内成形术、冠状动脉旁路移置术、各种冠状动脉再通术和心脏移植术后,严重威胁人类健康。国内外同行[3-5]对左冠状动脉缺血-再灌注损伤做了较多研究,而人及哺乳类动物90%以上的房室结动脉及2/3的窦房结动脉均起源于右冠状动脉,右冠状动脉位置深,变异较大,从而对右冠状动脉的研究增加了难度。本文观察了红花注射液[6-7]对在体兔右心缺血-再灌注损伤的影响,通过红花预处理后结扎右冠状动脉缺血30min,再灌注120min后心肌损伤减轻,其对右心缺血-再灌注损伤的保护,在国内外未见报道。
本文缺血-再灌注损伤组与假手术组比较,心电图抬高显著,CK、LDH明显升高,右心室心肌梗死明显,病理切片HE染色细胞损伤严重, BCL-2蛋白表达升高,说明结扎右冠状动脉造成右心缺血-再灌注损伤明显;红花组与缺血-再灌注损伤组比较,红花组的各项指标均降低,说明红花减轻了缺血-再灌注的损伤。
当发生心肌梗死时心肌氧摄取率降低,对自由基清除能力下降,心肌细胞内氧自由基爆发式增长[8],通过系列病理生理作用,引发心肌缺血-再灌注损伤。红花通过抑制氧自由基生成、增强心肌酶活性、改善微循环等作用减轻缺血-再灌注过程中心肌细胞的损伤[9],对兔心肌缺血-再灌注损伤起到保护作用,临床上在应用红花预防心缺血-再灌注损伤具有广阔前景,对临床治疗具有指导意义。
| [1] | Jiang G, Liu X, Wang M, et al. Oxymatrine ameliorates renal ischemia-reperfusion injury from oxidative stress through Nrf2/HO-1 pathway[J]. Acta Cir Bras, 2015, 30(6): 422–429. DOI:10.1590/S0102-865020150060000008 |
| [2] | Hu T, Wei G, Xi M, et al. Synergistic cardioprotective effects of Danshensu and hydroxysafflor yellow A against myocardial ischemia-reperfusion injury are mediated through the Akt/Nrf2/HO-1 pathway[J]. Int J Mol Med, 2016, 38(1): 83–94. DOI:10.3892/ijmm.2016.2584 |
| [3] | Aulakh AS, Randhawa PK, Singh N, et al. Neurogenic pathways in remote ischemic preconditioning induced cardioprotection:Evidences and possible mechanisms[J]. Korean J Physiol Pharmacol, 2017, 21(2): 145. DOI:10.4196/kjpp.2017.21.2.145 |
| [4] | Hu SY, Zhang Y, Zhu PJ, et al. Liraglutide directly protects cardiomyocytes against reperfusion injury possibly via modulation of intracellular calcium homeostasis[J]. J Geriatr Cardiol, 2017, 14(1): 57–66. DOI:10.11909/j.issn.1671-5411.2017.01.008 |
| [5] | Liu H, Wang C, Qiao Z, et al. Protective effect of curcumin against myocardium injury in ischemia reperfusion rats[J]. Pharm Biol, 2017, 55(1): 1144–1148. DOI:10.1080/13880209.2016.1214741 |
| [6] | Qazi N, Khan RA, Rizwani GH. Short communication-Evaluation of antianxiety and antidepressant properties of Carthamus tinctorius L.(Safflower) petal extract[J]. Pak J Pharm Sci, 2015, 28(3): 991–995. |
| [7] | Gao Y, Song J, Chen H, et al. TRPV1 activation is involved in the cardioprotection of remote limb ischemic postconditioning in ischemia-reperfusion injury rats[J]. Biochem Biophys Res Commun, 2015, 463(4): 1034–1039. DOI:10.1016/j.bbrc.2015.06.054 |
| [8] | Jeremic N, Petkovic A, Srejovic I, et al. Effects of ischemia and omeprazole preconditioning on functionalrecovery of isolated rat heart[J]. 2015, 30(2): 266-275. DOI: 10.5935/1678-9741.20150020. http://www.ncbi.nlm.nih.gov/pubmed/26107460 |
| [9] | Cao J, Chen Z, Zhu Y, et al. Huangqi-Honghua combination and its main components ameliorate cerebral infarction with Qi deficiency and blood stasis syndrome by antioxidant action in rats[J]. J Ethnopharmacol, 2014, 155(2): 1053–1060. DOI:10.1016/j.jep.2014.05.061 |



