2. 上海市重性精神病重点实验室, 上海 200030;
3. 上海交通大学脑科学与技术研究中心, 上海 200242
2. Shanghai Key Laboratory of Psychotic Disorders, Shanghai 200030, China;
3. Brain Science and Technology Research Center, Shanghai Jiao Tong University, Shanghai 200242, China
强迫症(obsessive-compulsive disorder,OCD)是一种常见的精神障碍,以反复出现且无法控制的闯入性强迫观念和(或)强迫行为为主要临床表现。近年来,研究者更倾向于将强迫症视为多维异质性疾病,根据症状表现可划分为清洁、检查、排列等维度[1]。不同症状维度的患者在临床表现及预后上存在差异。在强迫症重复经颅磁刺激(repetitive tanscranial magnetic stimulation, rTMS)的研究中,研究者发现刺激不同脑区所产生的治疗效果不尽相同。如刺激额叶可改善强迫思维[2], 而刺激背外侧前额叶(dorsolateral prefrontal cortices, DLPFC)则对改善强迫行为更有效[3]。提示临床表现差异下存在不同的生物学基础。因此,探明不同强迫症状所涉及的特定脑区可能对rTMS的个体化治疗存在一定临床价值。
前额叶-纹状体-丘脑-皮质(cortico-striatal-thalamic-cortical,CSTC)环路为强迫症发生机制中的经典环路,影像学研究发现强迫症患者的前额叶,纹状体及丘脑存在异常[4]。而有关顶叶、颞叶、枕叶等经典CSTC环路核心结构以外脑区的报道却不尽一致[5-6]。功能磁共振研究发现强迫清洗与顶叶及尾状核功能异常有关,检查症状与颞叶区域功能异常有关,而排列症状与视辐射、运动皮质、岛叶、颞叶及顶叶功能异常有关[7]。因此,我们假设强迫症的不同临床表现可能部分受到经典CSTC环路外的特定脑区调控。
本研究将采用扩散峰度成像(diffusion kurtosis imaging, DKI)对强迫症患者的脑结构进行检测,探索其改变与不同强迫症状维度间的联系。DKI的理论是基于生物体内水分子的扩散遵循非正态分布这一基础,其提供的参量不依赖于组织的各向异性,能同时反映脑灰质及白质的神经微结构变化[8]。目前,该方法已被广泛应用于帕金森病[9], 注意力缺陷与多动障碍[10], 双相情感障碍[11]等疾病的研究。
1 资料与方法 1.1 一般资料研究自2013年8月1日起至2014年12月30日,于上海交通大学医学院附属精神卫生中心门诊部就诊的强迫症患者共计43例。本研究已通过上海交通大学医学院附属精神卫生中心伦理委员会审核批准。入组标准:1) 年龄为18~55岁;2) 符合DSM-Ⅳ强迫症诊断标准;3) 耶鲁-布朗强迫量表(Yale-Brown Obsessive Compulsive Scale,Y-BOCS)评分≥16分;4) 未经精神科药物治疗;5) 初中及以上文化程度;6) 汉族,右利手;7) 本人签署知情同意。排除标准:1) 符合DSM-Ⅳ除强迫症以外的其他轴I诊断(MINI评估筛查);2) 强迫症状严重,使患者无法完成所需评估检查;3) 怀孕或准备近期怀孕、哺乳的女性;4) 存在严重躯体疾病,或实验室检查异常;5) 体内存在金属植入物或常规磁共振检查发现脑结构异常;6) 不能配合完成磁共振检测。
1.2 方法 1.2.1 临床评估采用耶鲁-布朗强迫量表(Y-BOCS)[12]评估被试的强迫症状严重程度,采用强迫症状分类量表(修订版)(Obsessive-Compulsive Inventory-Revised, OCI-R),该量表为2002年Foa等[13]编制,是由包含42个条目的OCI简化而来的强迫症状自评工具。总共包括有18个条目,分为6个分量表,每个分量表包含3个条目,分别从清洗(Washing)、强迫观念(Obsessing)、囤积(Hoarding)、排序(Ordering)、检查(Checking)及精神中和(Neutralizing)6个维度评估患者的强迫症状[14]。该量表采用0~4分5级评分,其中文版具有良好的信效度,且支持原版的六维度模型。本研究将强迫症患者以OCI-R各维度得分中位数(清洗:8分,强迫观念:7分,检查:7分),为界分为该维度症状的高得分组与低分组。采用贝克抑郁量表第2版(Beck Depression Inventory-Ⅱ, BDI-Ⅱ)[15]和贝克焦虑量表(Beck Anxiety Inventory, BAI)[16]评估被试的抑郁及焦虑情绪。
1.2.2 图像采集本研究采用西门子公司3.0T磁共振成像系统完成所有扫描(3.0T MRI Siemens Verio System)(Siemens Medical Solutions, Erlangen, Germany),使用12通道标准正交头线圈采集信号。所有被试均完成T1及T2结构像扫描,由一名专业放射科医生对常规结构像扫描结果进行查看,排除在结构像扫描中存在脑结构异常的被试。DKI扫描采用平面回波(Echo Planar Imaging,EPI)序列。扫描参数:voxel size=2.0mm×2.0mm×3.0mm,TR=9100ms,TE=95ms,FOV=256mm,b=0,1000,2000s/mm2,30个方向,层厚3mm。全脑共采集45层图像。扫描时间9′42″。
1.2.3 DKI数据处理运用MRIcroN软件中的dcm2nii.exe(http://www.mccauslandcenter.sc.edu/mricro/mricron/dcm2nii.html)工具,将每个被试的DKI数据由DICOM格式转换为4D的NIFTI格式,其中包含30个扩散梯度方向及一个无梯度的b=0数据。运用FSL4.1(http://www.fmrib.ox.ac.uk/fsl/)软件,通过FSL Eddycorrect命令进行涡流校正,将有梯度方向的数据配准到无梯度的b=0的数据上。运用建立于Matlab2011b(The MathWorks, Natick, MA)工作平台上的DKE (Diffusional Kurtosis Estimator)(http://www.nitrc.org/projects/dke/)软件[17],采用线性拟合计算扩散峰度成像各特征量,得到平均峰度(Mean Kurtosis, MK)图像。运用建立于Matlab2011b(The MathWorks, Natick, MA)工作平台上的Statistical Parametric Mapping 8(SPM8)(http://www.fil.ion.ucl.ac.uk/spm)统计软件对所得到的图像进行空间标准化。将扫描所得DKI的b=0图像标准化至SPM8自带的标准MNI(Montreal Neurological Institute, MNI)空间的T2模板上,并将变换参数应用到b=0图像上,重建分辨率2×2×2mm3。将所有被试的b=0图像取平均,并以6mm全宽半高值(Full-Width at Half-Maximun,FWHM)的高斯核做平滑,得到平均的b0模板。将所有被试的MK图像标准化到该b0模板,重建分辨率2×2×2mm3,所得图像以6mm FWHM的高斯核进行空间平滑,以降低噪声并减少空间标准化所带来的误差。运用SPM8中的分割工具将上述步骤中得到的平均b0模板分割为脑灰质、脑白质及脑脊液。使用分割所得的平均脑灰质及白质b0模板,制得二值化的灰质及白质模板,将灰质及白质模板用于MK的图像分析[18]。
1.3 统计学方法一般人口学资料以及症状量表数据采用SPSS 16.0进行统计分析和处理,取P<0.05为两组评分差异有统计学意义。本研究所纳入的患者具有囤积、排序及精神中和症状者少,故仅对清洗、强迫观念及检查维度作以分析。采用SPM8软件,以基于体素的分析(Voxel Based Analysis,VBA)方法对各症状维度高得分组与低得分组患者进行两独立样本t检验,进行分析。在灰质及白质以选取15个及以上连续的有差异像素集合被认为是差异有统计学意义的脑区(未校正P<0.001,体素簇≥15个像素,双侧检验)查看各差异区峰值中心的MNI坐标,使用xjview(http://www.alivelearn.net/xjview8)定位差异区峰值MNI坐标,并定位差异所属脑区。
2 结果 2.1 人口学及临床数据43例强迫症患者(17名女性,26名男性)均为从未经精神科药物治疗者。一般资料及临床特征(见表 1)。各症状高得分组与低得分组间在该症状维度OCI得分上具有显著差异(见表 2)。而其年龄、性别组成、受教育水平、Y-BOCS, BDI-Ⅱ, BAI及OCI-R其他症状维度得分均无显著差异。
| 表 1 一般资料及临床特征 |
| 表 2 两组间各维度强迫症状得分比较(x±s) |
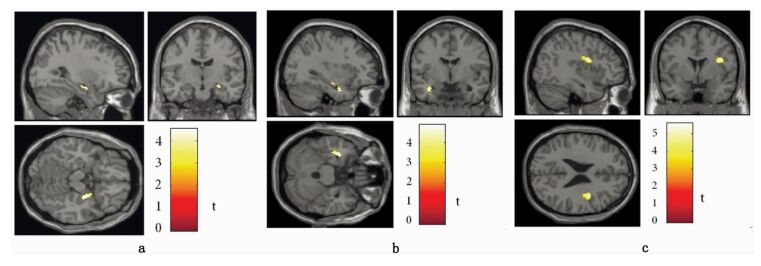
强迫观念症状得分高者较低者,在左侧丘脑灰质(-16,-24,2) 区域MK值增高(见图 1)。强迫清洗症状得分高者较低者在右侧海马旁回灰质(28,-6,-16)、左侧海马旁回白质(-34,-2,-26) 及右侧岛叶白质(40,2,24) MK值增高(见图 2a、2b、2c)。强迫检查症状得分高者较低者在右侧颞中回(58,-18,-16) 区域MK值增高。见图 3。(未校正P<0.001,体素簇≥15个像素,双侧检验)(见表 3a、3b)。

|
图 1 强迫观念维度高分组与低分组平均峰度值有差异的脑区 强迫观念维度高得分组患者(n=23) 的左侧丘脑区域平均峰度值较低得分组(n=20) 显著增高 |
|
图 2
强清洗维度高分组与低分组平均峰度值有差异的脑区
a.强迫清洗维度高得分组患者(n=22) 的右侧海马旁回灰质区域平均峰度值较低得分组(n=21) 显著增高 b.强迫清洗维度高得分组患者(n=22) 的左侧海马旁回白质区域平均峰度值较低得分组(n=21) 显著增高 c.强迫清洗维度高得分组患者(n=22) 的右侧岛叶白质区域平均峰度值较低得分组(n=21) 显著增高 |
|
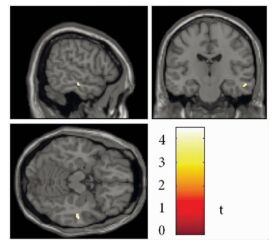
图 3 强迫检查维度高分组与低分组平均峰度值有差异的脑区. 强迫检查维度高得分组患者(n=22) 的右侧颞中回白质区域平均峰度值较低得分组(n=21) 显著增高 |
| 表 3a 不同强迫症状维度中,MK值存在差异的灰质脑区 |
| 表 3b 不同强迫症状维度中,MK值存在差异的白质脑区 |
本研究首次采用DKI技术对未经治疗的强迫症患者脑结构进行检测,探索其微结构改变与不同症状维度间(强迫观念、强迫清洗、强迫检查)的联系。
MK值为DKI的主要参量,用于描述水分子受周围环境中复杂结构影响所发生的扩散受限水平,可量化活体生物组织内水分子非正态分布的扩散情况,脑微结构复杂程度越高,该值越大[19]。MK值在白质区域的增高反映髓鞘化程度的增高,在灰质区域,MK值的增高主要反映神经元密度以及轴突和底树突的数量增加[20]。功能磁共振研究显示,当患者强迫症状被激发时其CSTC环路区域存在过度激活[21]。MK值的增高可能从一定程度上反映大脑神经传导速度及量的增长,造成特定脑区信息传导速度加快,可能与特定症状的产生有关。
本研究中,强迫观念得分高者其左侧丘脑区域MK值显著增高。CSTC环路为目前强迫症的病理生理发生机制中的经典模型。该模型中的丘脑为重要的皮层下信息传递中继结构,负责皮层及皮层下结构间的信息过滤,起到重要门控作用。Guo等[22]在功能磁共振研究中发现强迫症患者丘脑过度活跃,其左侧丘脑的活跃程度与威斯康辛卡片分类测试中的持续性错误数显著相关,提示丘脑过度活跃的功能与认知功能受损间存在密切联系,其门控功能异常,造成认知功能受损,从而引起强迫观念的产生。
强迫检查为最常见的外显强迫症状之一。本研究提示,强迫检查得分高者右侧颞中回白质MK值显著增高。颞中回白质与海马间存在广泛连接,参与记忆过程[23]。Toffolo等[24]研究发现强迫检查者在承受轻微的不确定性时就会产生比常人更多的检查行为,这种不确定性部分源于患者记忆生动性下降。Meta分析[25]结果提示强迫检查者的语言及非语言记忆均显著差于清洗者。而矛盾的是,过度的检查行为会使部分患者愈发无法清楚回忆检查过程,降低患者对自身记忆的信心,使不确定性的增加,反过来加重强迫检查行为[26]。Cottraux等[27]采用功能磁共振发现强迫检查者在症状被激发时,颞叶区域局部血流量显著升高。Van den Heuvel等[7]发现,反复检查与双侧颞叶体积改变显著相关。因此,我们推测颞中回通过参与记忆过程参与了强迫检查行为的调控。
本研究中,强迫清洗维度得分高者右侧岛叶及海马旁回的MK值显著增高。岛叶位于大脑中央,与前扣带回、背外侧前额叶及丘脑间存在广泛纤维连接,并与海马旁回所属的边缘叶共同参与构成边缘系统。厌恶感受是驱使人类进行清洁的内在动力,岛叶与海马同属边缘系统,通过处理并整合内脏感觉信息,参与厌恶感受调控[28]。Verstaen等[29]对84名神经退行性变患者进行研究,发现岛叶体积缩小的患者,其对厌恶感受的主观报告及生理反应明显弱于对照。功能磁共振研究中,研究者发现强迫症患者在面对诱发厌恶感受的视觉刺激时,其右侧岛叶及海马旁回的激活程度显著升高[30]。
另一方面,与其他强迫症状相比,强迫清洗的严重程度与厌恶感受的强弱具有更高相关性[31]。Athey等[32]研究发现在清洗、检查、排序及禁忌四个维度中,仅有清洗维度得分在患者症状减轻后与厌恶感受的减轻程度呈现显著正相关。因此,我们推测岛叶与海马旁回参与构成的边缘系统,通过对厌恶感受的调控,参与了强迫清洗的产生。与我们研究结果一致,Okada等[33]研究发现患者右侧岛叶灰质体积与清洗症状得分呈显著相关,功能磁共振研究中Jhung等[34]发现当强迫清洗症状被激发时,患者岛叶与腹侧纹状体间的功能连接明显增强。
综上所述,经典CSTC环路内核心部位—丘脑的结构改变与强迫观念有关,经典CSTC环路外的脑结构改变涉及不同外显强迫行为的表达。
不足之处:本文主要探讨不同强迫症状与脑结构异常间的联系,而未纳入对健康对照的分析,因此无法准确定义“异常”;其次,本研究尚未纳入随访研究数据,暂无法观察治疗前后患者相关脑区微结构的改变;此外,本研究未考虑病程对患者脑结构改变的影响,因此无法探明脑结构改变与强迫症状发生发展间的联系。
| [1] | Zhang X, Liu J, Cui J, et al. Study of symptom dimensions and clinical characteristics in Chinese patients with OCD[J]. J Affect Disord, 2013, 151(3): 868–874. DOI:10.1016/j.jad.2013.07.025 |
| [2] | Ma X, Huang Y, Liao L, et al. A randomized double-blinded sham-controlled trial of α electroencephalogram-guided transcranial magnetic stimulation for obsessive-compulsive disorder[J]. Chin Med J, 2014, 127(4): 601–606. |
| [3] | Greenberg BD, George MS, Martin JD, et al. Effect of prefrontal repetitive transcranial magnetic stimulation in obsessive-compulsive disorder:a preliminary study[J]. Am J Psychiatry, 1997, 154(6): 867–869. DOI:10.1176/ajp.154.6.867 |
| [4] | Menzies L, Chamberlain SR, Laird AR, et al. Integrating evidence from neuroimaging and neuropsychological studies of obsessive-compulsive disorder:the orbitofronto-striatal model revisited[J]. Neurosci Biobehav Rev, 2008, 32(3): 525–549. DOI:10.1016/j.neubiorev.2007.09.005 |
| [5] | de Wit SJ, Alonso P, Schweren L, et al. Multicenter voxel-based morphometry mega-analysis of structural brain scans in obsessive-compulsive disorder[J]. Am J Psychiatry, 2014, 171(3): 340–349. DOI:10.1176/appi.ajp.2013.13040574 |
| [6] | Piras F, Piras F, Caltagirone C, et al. Brain circuitries of obsessive compulsive disorder:a systematic review and meta-analysis of diffusion tensor imaging studies[J]. Neurosci Biobehav Rev, 2013, 37(10 Pt 2): 28562877. DOI:10.1016/j.neubiorev.2013.10.008 |
| [7] | van den Heuvel OA, Remijnse PL, Mataix-Cols D, et al. The major symptom dimensions of obsessive-compulsive disorder are mediated by partially distinct neural systems[J]. Brain, 2009, 132(Pt 4): 853–868. DOI:10.1093/brain/awn267 |
| [8] | Jensen JH, Helpern JA, Ramani A, et al. Diffusional kurtosis imaging:the quantification of non-gaussian water diffusion by means of magnetic resonance imaging[J]. Magn Reson Med, 2005, 53(6): 1432–1440. DOI:10.1002/mrm.20508 |
| [9] | Kamagata K, Tomiyama H, Hatano T, et al. A preliminary diffusional kurtosis imaging study of Parkinson disease:comparison with conventional diffusion tensor imaging[J]. Neuroradiology, 2014, 56(3): 251–258. DOI:10.1007/s00234-014-1327-1 |
| [10] | Adisetiyo V, Tabesh A, Di Martino A, et al. Attention-deficit/hyperactivity disorder without comorbidity is associated with distinct atypical patterns of cerebral microstructural development[J]. Hum Brain Mapp, 2014, 35(5): 2148–2162. DOI:10.1002/hbm.22317 |
| [11] | Zhao L, Wang Y, Jia Y, et al. Cerebellar microstructural abnormalities in bipolar depression and unipolar depression:A diffusion kurtosis and perfusion imaging study[J]. J Affect Disord, 2016, 195: 21–31. DOI:10.1016/j.jad.2016.01.042 |
| [12] | Goodman WK, Price LH, Rasmussen SA, et al. he Yale-Brown Obsessive Compulsive Scale.Ⅱ.Validit[J]. Arch Gen Psychiatry, 1989, 46(11): 1012–1016. DOI:10.1001/archpsyc.1989.01810110054008 |
| [13] | Foa EB, Huppert JD, Leiberg S, et al. The Obsessive-Compulsive Inventory:development and validation of a short version[J]. Psychol Assess, 2002, 14(4): 485–496. DOI:10.1037/1040-3590.14.4.485 |
| [14] | Peng ZW, Yang WH, Miao GD, et al. The Chinese version of the Obsessive-Compulsive Inventory-Revised scale:Replication and extension to non-clinical and clinical individuals with OCD symptoms[J]. BMC Psychiatry, 2011, 11(1). DOI:10.1186/1471-244x-11-129 |
| [15] | Beck AT, Steer RA, Brown G. Beck depression inventory-Ⅱ[J]. PsycTESTS Dataset, 1996. DOI:10.1037/t00742-000 |
| [16] | Beck AT, Steer RA. Manual for the Beck anxiety inventory[M]. San Antonio, TX: Psychological Corporation, 1990. |
| [17] | Tabesh A, Jensen JH, Ardekani BA, et al. Estimation of tensors and tensor-derived measures in diffusional kurtosis imaging[J]. Magn Reson Med, 2011, 65(3): 823–836. DOI:10.1002/mrm.22655 |
| [18] | Leung LH, Ooi GC, Kwong DL, et al. White-matter diffusion anisotropy after chemo-irradiation:a statistical parametric mapping study and histogram analysis[J]. Neuroimage, 2004, 21(1): 261–268. DOI:10.1016/j.neuroimage.2003.09.020 |
| [19] | Falangola MF, Jensen JH, Babb JS, et al. Age-related non-Gaussian diffusion patterns in the prefrontal brain[J]. J Magn Reson Imaging, 2008, 28(6): 1345–1350. DOI:10.1002/jmri.21604 |
| [20] | Cheung MM, Hui ES, Chan KC, et al. Does diffusion kurtosis imaging lead to better neural tissue characterization A rodent brain maturation study[J]. Neuroimage, 2009, 45(2): 386–392. DOI:10.1016/j.neuroimage.2008.12.018 |
| [21] | Saxena S, Rauch SL. Functional neuroimaging and the neuroanatomy of obsessive-compulsive disorder[J]. Psychiatr Clin North Am, 2000, 23(3): 563–586. DOI:10.1016/s0193-953x(05)70181-7 |
| [22] | Guo H, Zhao N, Li Z, et al. Regional cerebral blood flow and cognitive function in patients with obsessive-compulsive disorder[J]. Arq Neuropsiquiatr, 2014, 72(1): 44–48. DOI:10.1590/0004-282X20130205 |
| [23] | Race E, LaRocque KF, Keane MM, et al. Medial temporal lobe contributions to short-term memory for faces[J]. J Exp Psychol Gen, 2013, 142(4): 1309–1322. DOI:10.1037/a0033612 |
| [24] | Toffolo MB, van den Hout MA, Engelhard IM, et al. Patients With Obsessive-Compulsive Disorder Check Excessively in Response to Mild Uncertainty[J]. Behav Ther, 2016, 47(4): 550–559. DOI:10.1016/j.beth.2016.04.002 |
| [25] | Leopold R, Backenstrass M. Neuropsychological differences between obsessive-compulsive washers and checkers:a systematic review and meta-analysis[J]. J Anxiety Disord, 2015, 30: 48–58. DOI:10.1016/j.janxdis.2014.12.016 |
| [26] | Radomsky AS, Dugas MJ, Alcolado GM, et al. When more is less:doubt, repetition, memory, metamemory, and compulsive checking in OCD[J]. Behav Res Ther, 2014, 59: 30–39. DOI:10.1016/j.brat.2014.05.008 |
| [27] | Cottraux J, Gérard D, Cinotti L, et al. A controlled positron emission tomography study of obsessive and neutral auditory stimulation in obsessive-compulsive disorder with checking rituals[J]. Psychiatry Res, 1996, 60(2-3): 101–112. DOI:10.1016/0165-1781(96)02697-2 |
| [28] | Craig AD. How do you feel--now The anterior insula and human awareness[J]. Nat Rev Neurosci, 2009, 10(1): 59–70. DOI:10.1038/nrn2555 |
| [29] | Verstaen A, Eckart JA, Muhtadie L, et al. Insular atrophy and diminished disgust reactivity[J]. Emotion, 2016, 16(6): 903–912. DOI:10.1037/emo0000195 |
| [30] | Lawrence NS, An SK, Mataix-Cols D, et al. Neural responses to facial expressions of disgust but not fear are modulated by washing symptoms in OCD[J]. Biol Psychiatry, 2007, 61(9): 1072–1080. DOI:10.1016/j.biopsych.2006.06.033 |
| [31] | García-Soriano G, Rosell-Clari V, Serrano Má. Emotional and Cognitive Variables Associated with Contamination-Related Obsessive-Compulsive Symptoms[J]. Span J Psychol, 2016, 19: E25. DOI:10.1017/sjp.2016.27 |
| [32] | Athey AJ, Elias JA, Crosby JM, et al. Reduced disgust propensity is associated with improvement in contamination/washing symptoms in obsessive-compulsive disorder[J]. J Obsessive Compuls Relat Disord, 2015, 4: 20–24. DOI:10.1016/j.jocrd.2014.11.001 |
| [33] | Okada K, Nakao T, Sanematsu H, et al. Biological heterogeneity of obsessive-compulsive disorder:A voxel-based morphometric study based on dimensional assessment[J]. Psychiatry Clin Neurosci, 2015, 69(7): 411–421. DOI:10.1111/pcn.12269 |
| [34] | Jhung K, Ku J, Kim SJ, et al. Distinct functional connectivity of limbic network in the washing type obsessive-compulsive disorder[J]. Prog Neuropsychopharmacol Biol Psychiatry, 2014, 53: 149–155. DOI:10.1016/j.pnpbp.2014.04.007 |



