自身免疫性脑炎(AE)是一类累及海马、杏仁核、导叶及扣带回皮质的自身免疫性疾病,多急性或亚急性起病,临床表现以癫痫发作,认知功能减退,精神行为异常为主。自从2007年抗N-甲基-D-天冬氨酸受体(NMDAR)抗体被发现以来,几乎每年都有与其相关的新型抗神经元抗体不断被发现[1-2],对该病的认识逐渐深入。现对济宁医学院附属医院神经内科近几年收治的AE患者的临床资料进行总结,特别是伴有癫痫发作的脑炎患者的诊疗体会,希望对临床上认识这一组中枢神经系统罕见炎症性疾病有一定帮助。
1 资料和方法 1.1 一般资料2014年5月至2017年7月在济宁医学院附属医院神经内科收治的AE患者10例,其中8例确诊患者,其中5例抗NMDAR脑炎,2例LGI1抗体相关脑炎,1例抗γ-氨基丁酸B型受体(GABABR)脑炎。2例为已发现颅内肿瘤的AE患者,未行抗体筛查。男5例,女5例,年龄14~70岁,平均年龄36岁。
1.2 方法总结分析全部患者资料,包括起病年龄,首发症状,临床表现特点,是否出现前驱症状、精神异常、癫痫发作、意识障碍、认知障碍、运动障碍、中枢性低通气状态、自主神经功能紊乱等症状,以及头部MRI、视频脑电、肿瘤相关筛查、甲状腺相关抗体筛查、脑脊液常规及抗体检测等实验室检查、检验,针对伴有癫痫发作的AE患者,分析其发作类型,合理选用抗癫痫药物,观察其治疗和预后情况。患者血和脑脊液标本冰冻送检北京协和医院神经免疫实验室行AE相关抗体检测。
2 结果 2.1 临床表现多数患者发病前无明显诱因,只有2例患者有头痛及情绪激动的前驱症状。6例患者以意识不清为首发症状,2例以精神行为异常起病,1例以头晕起病,1例以谚语起病。所有患者病程中均伴有典型的癫痫发作,其中7例患者为全面性强直-阵挛发作,表现为发作性意识不清,肢体抽搐,伴有双眼上翻、口吐白沫、面色青紫等,3例患者为局灶性运动型发作,仅表现为头部或肢体的抽动。4例患者出现不自主运动及自主神经功能障碍,表现为口角、肢体的不自主抖动。5例患者出现认知功能障碍,表现为记忆力减退和反应迟钝。2例患者病程中出现了不同程度中枢性低通气状态,并接受了机械辅助通气治疗。
2.2 辅助检查 2.2.1 血及脑脊液抗体筛查8例确诊患者血和脑脊液标本冰冻送检北京协和医院神经免疫实验室行AE相关抗体检测,其中5例抗NMDAR脑炎,2例LGI1抗体相关脑炎,1例抗GABABR脑炎。
2.2.2 颅脑MRI所有患者均接受颅脑MRI平扫,3例提示与本疾病相关的阳性表现,分别为双颞叶、双顶枕部和左颞叶的异常信号;4例未见明显异常;2例由于颅内肿瘤行手术治疗后,表现为明显的术后症像;1例可见脑内缺血灶。
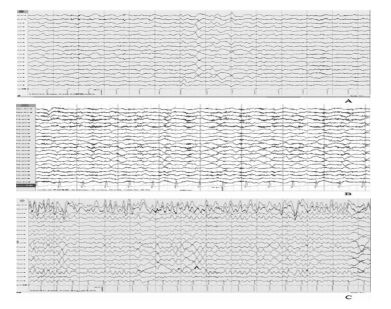
2.2.3 视频脑电确诊的5例抗NMDAR脑炎患者中,3例表现为全面性发作,视频脑电结果:1例各导联少量低至中波幅4~6HZθ波(见图 1A);1例各导联大量低中波幅4~7HZθ波及活动;1例双前头部导联可见稍多散在中高波幅尖波,双侧颞部可见6HZ左右θ波。2例局灶性运动型癫痫,视频脑电结果:1例左侧半球慢波多;1例未见明显异常。5例患者脑电图均为检测到异常δ波,但异常脑电图中均发现有异常慢波。2例LGI1抗体相关脑炎患者1例表现为全面性强直-阵挛发作,脑电图可见轻-中度异常脑电图,各导联慢波多(见图 1B);1例表现为头部不自主运动,为局灶性运动型癫痫,脑电图未见明显异常。2例患者均出现所谓的FBDS发作期。1例抗GABABR脑炎患者表现为癫痫持续状态,脑电图可见各导联大量中波幅与5~6HZθ波及节律夹杂3~3.5HZδ波(见图 1C)。2例疑似患者,均表现为全面性发作,1例进展为癫痫持续状态,脑电图分别示:右前额可见少量散在中高波幅棘波,尖慢波,另1例未见明显异常。
|
图 1
各脑炎患者脑电图
注:A为抗NMDAR脑炎患者脑电图未见明显α波及活动,脑电活动弥漫性减慢,各导联大量低中波幅4~6HZθ波及活动,间以较多低中波幅1.5~2.5HZ大慢波。 B为LGI1抗体相关脑炎患者脑电图未见明显α波及活动,脑电图活动弥漫性减慢,各导联大量低中波幅4~7HZθ波及活动,间以较多低中波幅2.0~3.5HZ大慢波,似左颞部导联为著,慢波上可见较多快波活动。 C为抗GABABR脑炎患者脑电图未见明显α波及活动,脑电图活动弥漫性减慢,各导联大量中波幅5~6HZθ慢波节律,夹杂3~3.5δ波,左侧额、中央、颞、额中线区阵法出现15HZ左右低幅。 |
所有患者进行了肿瘤相关筛查,1例患者发现肺癌,2例患者已确诊颅内肿瘤,分别为“生殖细胞瘤”“颅内血管周细胞瘤”,且肿瘤症状先于脑炎出现。2例患者住院期间发现甲功及甲状腺相关抗体异常。
2.3 治疗转归8例患者采用了免疫球蛋白联合激素、抗癫痫药物疗法,1例患者采用了激素疗法,1例患者采用激素联合抗癫痫药物疗法。所有患者均采用改善脑细胞代谢等一般治疗,个体差异对症处理。见表 1。
| 表 1 10例AE患者的临床资料 |
脑炎是脑实质的弥漫性炎性病变导致的神经功能障碍,病理改变以灰质与神经元受累为主,部分可累及白质和血管。其中,AE泛指一类由自身免疫机制介导的脑炎,AE中合并相关肿瘤者,称为副肿瘤性AE,而副肿瘤性AE中符合边缘性脑炎者,称为副肿瘤性边缘性脑炎[3]。目前AE患病比例占脑炎病例的10%~20%,以抗NMDAR脑炎最常见,约占AE患者的80%,其次为抗富含亮氨酸胶质瘤失活蛋白1(LGIl)抗体相关脑炎与GABABR抗体相关脑炎等[4-7]。本院收集的8例确诊患者中,有5例抗NMDAR脑炎,2例LGI1抗体相关脑炎,1例抗GABABR脑炎,均是现已报道过的较为经典的类型。
过去认为抗NMDAR抗体脑炎与随后发现的抗GABABR脑炎、LGI1抗体相关脑炎都属于神经元表面抗原相关的边缘叶脑炎,随着各种新型的AE相继被发现与报道,逐渐对该病有了更深入的认识。2007年Datmau等[8]指出:抗NMDAR脑炎临床表现呈多样性,不同于与经典的边缘性脑炎,属于弥漫性脑炎。2016年柳叶刀神经病学杂志发表的诊断建议中[9],也分别阐述了两者的诊断标准。抗NMDAR脑炎多发生于年轻女性,有头痛、恶心等类似病毒性感染的前驱症状,临床表现主要以癫痫发作、精神行为异常、记忆障碍、意识水平下降、自主神经功能障碍以及低通气状态为主,患者常合并畸胎瘤,其中自主神经功能障碍也是早期极易忽视的。本文收集的5例抗NMDAR脑炎患者中,3例女性,2例男性,年龄集中在30岁左右,所有患者临床表现形式多样,主要以发作性意识不清或者精神行为异常为主,且均伴有癫痫发作,其中2例患者发病前出现头痛,情绪激动等首发症状,1例患者出现低通气状态,基本吻合文献中所述。抗GABABR脑炎、LGI1抗体相关脑炎属于典型的边缘性脑炎,两者均多见于男性患者,临床表现相对单一。LGI1抗体相关脑炎属于电压门控钾通道,以短暂性肌阵挛发作为主,60%患者可伴有低钠血症,本文2例LGI1抗体相关脑炎患者中,1例男性患者,1例女性患者,男性患者以发作性意识不清起病,相对比,女性患者症状较轻,仅有轻微头痛,且不伴精神行为异常和认知功能障碍,因该病多发于男性患者。是否女性患者本身症状比较轻还是由于该患者病程较短,因样本例数较少,暂不能明确。1例抗GABABR脑炎患者为男性,以“发作性意识不清”起病,伴有典型癫痫发作。
癫痫发作是AE的常见症状,3种类型脑炎均伴癫痫发作,其发作形式也多有不同。伴癫痫发作的AE患者,应常规行视频脑电检测,以明确癫痫发作类型,指导临床抗癫痫药物的应用。抗NMDAR脑炎癫痫发作形式多样,可有全面性癫痫、局灶性癫痫、混合性癫痫和癫痫持续状态,其视频脑电特点:呈弥漫或者多灶的慢波,偶尔可见癫痫波,重症患者可出现较特异性的异常δ波。LGI1抗体相关脑炎患者癫痫发作形式以各种形式的颞叶癫痫常见,先兆以树毛发作(“起鸡皮疙瘩”感)多见,面-臂肌张力障碍发作(faciobrachial dystonic seizure,FBDS)是该病特征性发作症状,表现为单侧手臂及面部乃至下肢的频繁、短暂的肌张力障碍样不自主动作,其发作时间短暂,一般仅数秒,发作频繁者可达每日数十次;可伴有双侧肌张力障碍样发作、感觉异常先兆、愣神、意识改变等,其视频脑点特点:FBDS发作期脑电图异常比例仅占21%~30%,FBDS发作间期可表现为轻度弥漫性慢波或双侧额颞叶慢波,也可完全正常[10]。抗GABABR脑炎通常以全面强直阵挛性发作为主,患者可迅速进展为癫痫持续状态,其视频脑电特点:可见颞叶起源的癫痫放电,以及弥漫或者散在分布的慢波。本文的10例患者均进行了视频脑电监测,如前所述,检测到8例患者存在异常脑电图,主要以慢波异常为主,由于样本例数较少,比较典型的脑电图症像,如抗NMDAR脑炎的异常δ波等并未检测到。
治疗方面,目前国际上尚无AE的诊疗指南与共识,《中国自身免疫性脑炎诊治专家共识》也是近期在中华神经科杂志定稿并发表,其指出AE的治疗包括免疫治疗、对癫痫发作和精神症状的症状治疗、支持治疗、康复治疗,合并肿瘤者进行切除肿瘤等抗肿瘤治疗。免疫治疗方面包括一线免疫治疗的糖皮质激素、静脉注射免疫球蛋白(IVIg)和血浆交换,二线免疫药物包括利妥昔单抗与静脉用环磷酰胺,多用于一线免疫治疗效果不佳的患者,长程免疫治疗药物包括吗替麦考酚酯与硫唑嘌呤等,主要用于复发病例,也可以用于一线免疫治疗效果不佳的患者和肿瘤阴性的抗NMDAR脑炎患者。对可能的AE,也可酌情试用一线免疫治疗药物,这也是AE治疗的大前提。伴癫痫发作的AE患者,最合适的抗癫痫药物(AED)仍在探索中,且鲜有指南提供经验。目前尚无报道在不用AEDs治疗情况下自身免疫脑炎患者癫痫发作能够得到控制的病例,因此AEDs的使用是必须的。AEDs的选择仍然主要根据癫痫发作类型,推荐使用卡马西平、奥卡西平、丙戊酸钠、苯妥英钠、拉莫三秦和左乙拉西坦等。一般先从单药开始,逐渐加量至有效剂量,无效时可考虑联合治疗。Quek等[11]在研究32例癫痫发作的AE患者中指出,81%的患者需要2种或以上AEDs联合应用来控制癫痫发作。值得注意的是,对于LGI1抗体相关脑炎,因患者易并发低钠血症,而卡马西平、奥卡西平本身具有低钠的不良反应,应酌情适量使用或避免使用。目前AEDs控制癫痫发作的机制尚不清楚,推测其可能是通过直接抑制癫痫发作或是通过间接抑制免疫球蛋白的产生从而改善癫痫的治疗。由于AE患者多有精神行为异常和癫痫发作,常容易被误诊为病毒性脑炎。在本研究中,所有患者入院早期,在明确AE之前,因未能排除病毒感染病因,我们预防性的使用了阿昔洛韦等抗病毒药物治疗。8例患者确诊后均采用了IVIg+激素一线免疫药物治疗,其中2例患者由于病情反复发作,加用了吗替麦考酚酯免疫抑制剂。2例未确诊患者中,1例因有生殖细胞瘤病史,加上临床表现及脑电图特点,AE可能性大,我们仍采用IVIg+激素疗法,患者症状改善较为明显。1例患者病史较短,症状较轻,目前仅用了激素治疗,效果较明显。所有患者均采用改善脑细胞代谢等一般治疗,有精神症状的加用奥氮平等改善症状,所有患者症状均较前好转。
4 体会以突发癫痫发作或认知功能损害或精神行为异常的患者,且短期内癫痫发作较为频繁,应警惕AE的可能,及时筛查自身抗体,以免误诊漏诊。Spatola等[12]研究认为,因为亲离子受体性质的自身免疫性抗体可以改变皮层的生理性电活动,所以AE患者伴发的癫痫症状单纯依靠抗癫痫药物治疗效果欠佳,需要结合免疫调节治疗。本文仅阐述了抗NMDAR脑炎、LGI1抗体相关脑炎、抗GABABR脑炎这3种类型伴癫痫发作的诊疗体会,虽然样本例数较少,仍有一定的参考作用。对于伴有癫痫发作的AE患者,在使用IVIg+激素一线免疫治疗的前提下,依据癫痫发作的不同类型,合理选用AEDs联合治疗,才能合理有效控制癫痫发作症状,进而改善患者预后。
| [1] | Graus F, Saiz A, Dalmau J. Antibodies and neuronal autoimmune disorders of the CNS[J]. J Neurol, 2010, 257(4): 509–517. DOI:10.1007/s00415-009-5431-9 |
| [2] | Lancaster E, Martinez-Hernandez E, Dalmau J. Encephalitis and antibodies to synaptic and neuronal cell surface proteins[J]. Neurology, 2011, 77(2): 179–189. DOI:10.1212/WNL.0b013e318224afde |
| [3] | Graus F, Delattre JY, Antoine JC, et al. Recommended diagnostic criteria for paraneoplastic neurological syndromes[J]. J Neurol Neurosurg Psychiatr, 2004, 75(8): 1135–1140. DOI:10.1136/jnnp.2003.034447 |
| [4] | Davies G, Irani SR, Coltart C, et al. Anti-N-methyl-D-aspartate receptor antibodies:a potentially treatable cause of encephalitis in the intensive care unit[J]. Crit Care Med, 2010, 38(2): 679–682. DOI:10.1097/CCM.0b013e3181cb0968 |
| [5] | Guan HZ, Ren HT, Cui LY. Autoimmune encephalitis:an expanding frontier of neuroimmunology[J]. Chin Med J, 2016, 129(9): 1122–1127. DOI:10.4103/0366-6999.180514 |
| [6] | Suh-Lailam BB, Haven TR, Copple SS, et al. Anti-NMDA-receptor antibody encephalitis:performance evaluation and laboratory experience with the anti-NMDA-receptor IgG assay[J]. Clin Chim Acta, 2013, 421: 1–6. DOI:10.1016/j.cca.2013.02.010 |
| [7] | 任海涛, 崔丽英, 关鸿志, 等. 不明病因脑炎中抗N-甲基-D-天冬氨酸受体脑炎的筛查诊断[J]. 中华神经科杂志, 2014, 47(2): 119–122. DOI:10.3760/cma.j.issn.1006-7876.2014.02.011 |
| [8] | Dalmau J, Tüzün E, Wu HY, et al. Paraneoplastic anti-N-methyl-D-aspartate receptor encephalitis associated with ovarian teratoma[J]. Ann Neurol, 2007, 61(1): 25–36. DOI:10.1002/ana.21050 |
| [9] | Graus F, Titulaer MJ, Balu R, et al. A clinical approach to diagnosis of autoimmune encephalitis[J]. Lancet Neurol, 2016, 15(4): 391–404. DOI:10.1016/S1474-4422(15)00401-9 |
| [10] | Irani SR, Michell AW, Lang B, et al. Faciobrachial dystonic seizures precede Lgi1 antibody limbic encephalitis[J]. Ann Neurol, 2011, 69(5): 892–900. DOI:10.1002/ana.22307 |
| [11] | Quek AM, Britton JW, McKeon A, et al. Autoimmune epilepsy:clinical characteristics and response to immunotherapy[J]. Arch Neurol, 2012, 69(5): 582–593. DOI:10.1001/archneurol.2011.2985 |
| [12] | Ferlazzo E, Gasparini S, Sueri C, et al. Status epilepticus of inflammatory etiology:a cohort study[J]. Neurology, 2016, 86(11): 1076. DOI:10.1212/WNL.jnyxyxb-40-05-35002508 |



