编者按:济宁医学院药学院成立于2001年,拥有药学、药物制剂、中药学、制药工程和生物制药5个本科专业,均于2016年被批准为山东省高水平应用型专业群建设项目。其中药学和药物制剂是山东省特色专业,中药学是该校“十三五”特色专业重点发展专业。药学院紧紧围绕山东省生态环境和国民经济发展,深入开展先导化合物的发现与优化、新型医药材料及药物传输系统的开发、药物分子的活性筛选与机理研究以及药物的药物分析与质量控制4个方向的研究。多年来,本学科共承担上级教、研项目85项,发表学术论文200余篇,SCI收录50余篇。授杈国家发明专利5项。目前,该学科已形成了教学、科研和社会服务三位一体的办学格局。本期开辟“药学”专栏,并邀请国内药学界有突出贡献的专家撰稿,集中展示在药物合成、制剂开发、药品质量分析、药理研究等领域取得的研究成果,以飨读者。
纳米银(silver nanoparticles)具有广谱抗菌、安全无毒、无耐药性[1]以及良好的生物相容性等特点,可有效预防感染[2],而且应用纳米银标记DNA作为电化学探针,可应用于生物特定序列的测定[3]。纳米银的合成包括物理方法、化学方法等。近年来纳米银的生物合成法已成为相关领域的研究热点,人们相继采用不同的植物提取物合成纳米银,如利用天竺葵叶、红茶叶等植物提取液合成纳米银[4-11]。纳米银的生物合成简单易行,绿色环保。本研究选用简单易得的蒲公英提取液以及硝酸银为原料,生物合成具有良好抗菌活性的纳米银。在理论和实践上为纳米银的可控合成提供依据。
1 实验部分 1.1 仪器、试剂 1.1.1 仪器UV-2450紫外分光光度计(Shimadzu corporation);SHZ-88水浴恒温振荡器;H1650高速台式离心机(长沙湘仪离心机仪器有限公司);IRTracer-100(日本岛津制作厂);78-1型磁力搅拌器(江苏省金坛市荣华仪器制造有限公司);Zetasizer Nano-ZS型激光粒度仪(英国Malvern Instruments公司);JEOL100CX-Ⅱ透射电子显微镜(日本电子光学公司);FDU-2110冷冻干燥机(上海爱朗仪器有限公司);SW-CJ-2FD型超净工作台(苏州净化设备有限公司);DHP-420型电热恒温培养箱(天津市中环实验电炉有限制造公司);YM50-130302型立式压力蒸汽灭菌器(上海三申医疗器械有限公司)。
1.1.2 试剂硝酸银(分析纯,天津市永大化学试剂有限公司);氨水(分析纯,烟台三和化学试剂有限公司);乙酸(分析纯,莱阳经济技术开发区精细化工厂);硝酸(分析纯,莱阳经济技术开发区精细化工厂);大肠杆菌,金黄色葡萄球菌(济宁医学院微生物实验室提供);营养琼脂(北京奥博星生物技术有限责任公司);阿莫西林分散片(先声药业,国药准字H20140077)。
1.2 实验方法 1.2.1 蒲公英提取液的制备本实验所用的玻璃仪器均用稀硝酸浸泡,再用重蒸水冲洗干净。取5g蒲公英干叶剪碎,置于500ml烧杯中,加100ml重蒸水,用电热套煮沸5min。漏斗过滤,8000r/min离心30min,再用0.45μm的微孔滤膜过滤。将滤液放入4℃冰箱储存备用。
1.2.2 AgNO3溶液的配制精密称取固体AgNO3 0.0425g于50ml烧杯中加重蒸水使其溶解,用玻璃棒引流至250ml容量瓶中,重蒸水冲洗烧杯3次引流至容量瓶,定容,混匀。8000r/min离心30min,再用0.45μm的微孔滤膜过滤。于4℃冰箱储存以备用。
1.2.3 合成纳米银取2ml的蒲公英提取液于50ml锥形瓶中,放入搅拌子,置于磁力搅拌器上,室温下边搅拌边用一次性滴管逐滴滴加20ml AgNO3溶液(用时17min),滴加完成后继续搅拌15min(共搅拌32min),再置于水浴恒温振荡器(100r/min)中反应, 颜色由无色到金黄色或棕黑色即为纳米银形成。
1.2.4 影响纳米银粒径的因素考察1) 蒲公英提取液浓度:分取2ml不同浓度(0.005、0.010、0.125、0.020g/ml)的蒲公英提取液于50ml锥形瓶中,置于磁力搅拌器上,室温下边搅拌边滴加20ml AgNO3溶液(0.001mol/L,用时17min),反应温度85℃,加热震荡2h,pH值为6。滴加完成后继续搅拌15min,室温在磁力搅拌器上反应5h。颜色变为红黄色,即为纳米银。
2) 温度:取2ml的0.01g/ml的蒲公英提取液于50ml锥形瓶中,方法同上,于不同温度下反应。将所得纳米银混悬液用超纯水洗涤、离心后重新分散。考察温度对硝酸银粒径大小、粒度分布及紫外吸收的影响。见表 2。
| 表 1 蒲公英浓度对纳米银粒径的影响 |
| 表 2 反应温度对纳米银粒径的影响 |
3) 硝酸银浓度的影响:将不同浓度硝酸银加入反应体系中,按照前述方法,考察硝酸银浓度对纳米银性质的影响。
4) pH对纳米银特性的影响:分别取5ml蒲公英提取液于4个50ml烧杯中,利用醋酸或氨水调至pH为4、7、9,再分别移液至4个25ml的容量瓶中。分别取2ml不同pH值的蒲公英提取液于50ml锥形瓶中,置于磁力搅拌器上,室温下边搅拌边用一次性滴管滴加20ml AgNO3溶液(用时17min),滴加完成后继续搅拌15min,再置于水浴恒温振荡器(85℃,100r/min)中反应2h, 测定纳米银的特征。
5) 反应时间对纳米银特性的影响:采用前述方法制备纳米银。固定其反应浓度为85℃,考察不同反应时间对纳米银特性的影响。
6) 纳米银特性的测定:采用UV-2450紫外分光光度计以重蒸水作为空白扫描纳米银的最大吸收波长。利用Zetasizer Nano-ZS型激光粒度仪测定纳米银的粒径、分散系数PDI和电位。将反应后的纳米银溶液及蒲公英提取液先用冰箱进行预冻12h,再在冷冻干燥机中冷冻干燥48h,得到固体的纳米银及蒲公英提取物,然后采用FTIR以样品:溴化钾为1:100进行测定反应前后体系官能团峰的强度及位置的变化。将制得的纳米银稀释100倍之后利用JEOL100CX-Ⅱ透射电子显微镜分析纳米银的大小和形状
7) 纳米银的抗菌实验:将营养琼脂按规定比例加热溶于蒸馏水,盖紧瓶塞,置于立式压力蒸汽灭菌器中高压灭菌(121.0℃,20min)。灭菌后取出,待琼脂温度降至50~60℃时,在超净台内以无菌操作倾入一次性无菌平皿中,待琼脂凝固后即制成普通营养琼脂培养基,放置冰箱保存备用。
取所需菌种1~2环在普通营养琼脂培养基上连续划线,用灭菌后的吸管打孔,移液枪移取样品各50μl。取阿莫西林分散片研磨成细粉,称取0.0875g细粉至250ml容量瓶中,加重蒸水定容做对照品。
2 结果与讨论 2.1 蒲公英提取液浓度对纳米银粒径的影响见表 1。
由表 1可知蒲公英提取液浓度不宜过高,综合粒径和PDI数据采用0.01g/ml浓度的蒲公英提取液。
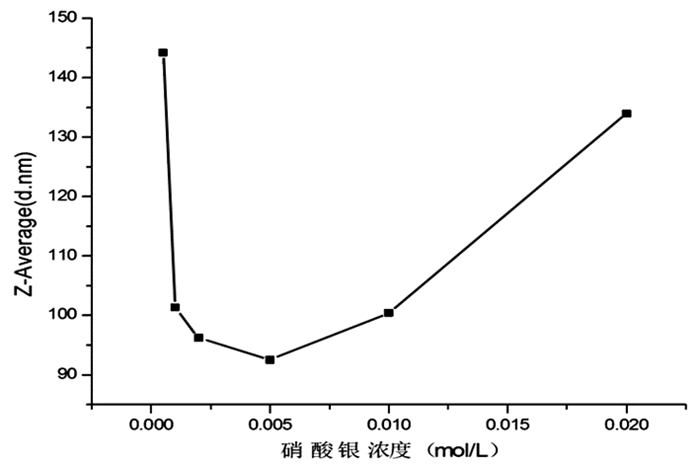
2.2 硝酸银浓度对纳米银粒径的影响固定蒲公英提取液浓度为0.01g/ml; 85℃下加热,pH值为6条件下合成纳米银,将所得纳米银混悬液用超纯水洗涤、离心后重新分散,测定其粒径及PDI值。考察硝酸银浓度对纳米银粒径的影响。见图 1。
|
图 1 硝酸银浓度对纳米银粒径的影响 注:洗涤后的纳米银粒径值 |
由图 1可见,硝酸银浓度在0.005~0.010mol/L范围内合成出的纳米银粒径较理想。由图 1数据与表 1数据比较可见,经过离心洗涤后的纳米银粒径较未洗涤前明显增加,说明经过洗涤后,吸附于纳米银表面的蒲公英中部分活性成分被洗脱,从而对纳米银的保护作用降低,导致部分银粒子发生聚集,从而使其粒度及PDI值增加。
2.3 温度对纳米银粒径的影响固定蒲公英提取液浓度为0.01g/ml; AgNO3浓度为0.001mol/L; 水浴震荡2h,pH值为6,考察不同温度下硝酸银粒径大小、粒度分布及紫外吸收。见表 2。
由表 2可见,当温度比较低时,所得纳米银粒径较大,随温度升高粒径减小。当温度处于60℃~80℃之间时粒径及PDI值基本不随温度的变化而变化。但当温度为85℃时,平均粒径明显减小。随着温度的升高,反应体系颜色的变化越快,粒径越来越小。而紫外光谱的最大吸收波长先增大后减小,基本稳定在425.00nm,分散系数、电位变化不大,比较稳定。
2.4 反应时间对纳米银粒径的影响固定蒲公英提取液浓度0.01g/ml; AgNO3 0.001mol/L; 85℃下加热震荡,考察反应时间不同对纳米银粒子及PDI值的影响。结果见表 3。
| 表 3 反应时间对纳米银性质的影响 |
由表 3可见,在0.5~5h时间范围内,纳米银粒子粒径及PDI值无明显变化,说明反应时间对纳米银的性质影响不大,而且也说明在该反应条件下纳米银粒子未发生自聚。
2.5 pH值对纳米银粒径的影响固定蒲公英提取液浓度为0.005g/ml; AgNO3浓度为0.001mol/L; 85℃下加热震荡2h;用氨水和乙酸调节pH值,考察提取液pH值对纳米银粒径及其分布的影响,结果见表 4。
| 表 4 pH对纳米银粒径的影响 |
用氨水和醋酸调pH,发现在85℃的恒温水浴振荡器中反应2h的条件下,pH增大,纳米银粒径会减小。加醋酸或加氨水都会使分散系数增大。原因可能是醋酸与提取液中的多元醇发生反应生成酯类,减小了多元醇对Ag+的还原促进和保护作用;氨水与其中的酸反应,生成了酰胺,酰胺能增强Ag+的还原有促进和保护。而通过分析数据可以得出,随着粒径的增加,紫外光谱的最大吸收波长会发生蓝移。
2.6 纳米银的理化性质表征 2.6.1 纳米银粒度、电位及形态表征利用纳米粒度激光分析仪测定纳米银粒径、电位,利用TEM表征其粒径大小及形态。结果见图 2~4。
|
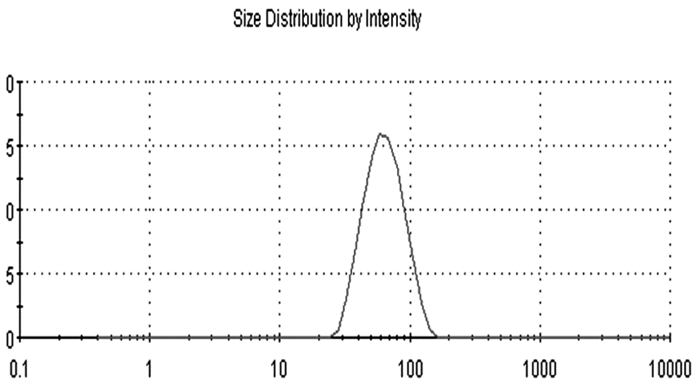
图 2 纳米银粒度分布图 |
|
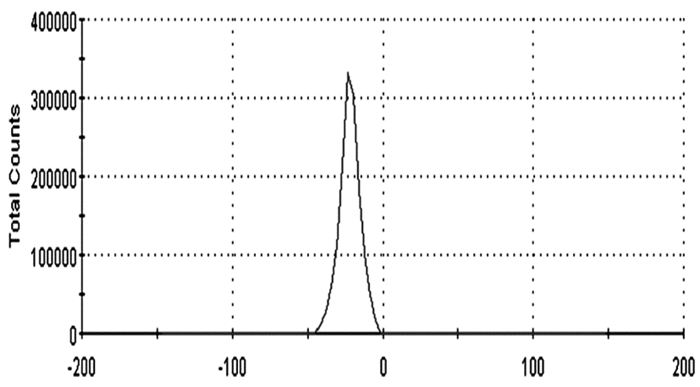
图 3 纳米银zeta电位图 |
|
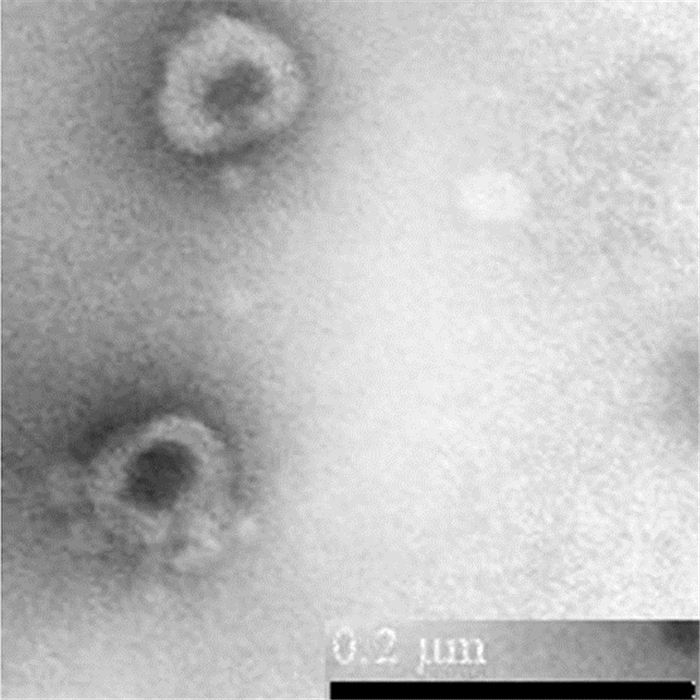
图 4 纳米银TEM图片 |
由图 2~3可见,体系中纳米银粒子分布较为均匀,且其分布呈正态分布,PDI值较小,其电位值-20 mV左右。由图 4 TEM图片可见,所得纳米银为球形粒子。
2.6.2 纳米银紫外吸收光谱利用UV-2450紫外分光光度计测纳米银紫外吸收光谱,结果见图 5。
|
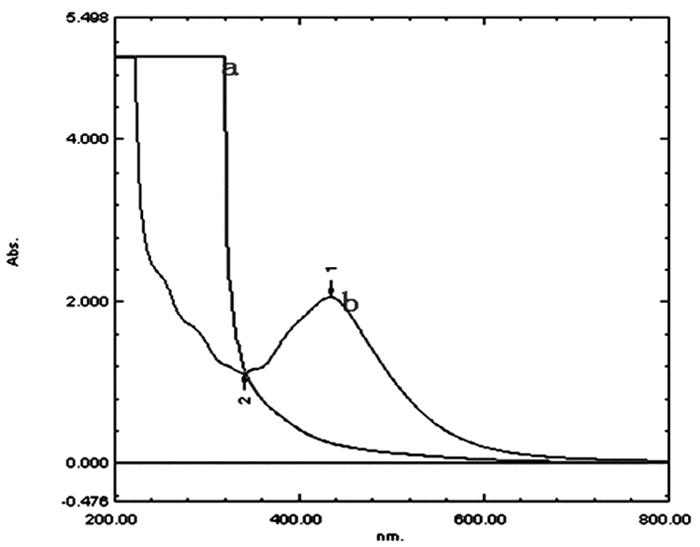
图 5 纳米银的紫外吸收光谱图 注:a.蒲公英提取液; b.蒲公英提取液制备的纳米银 |
由图 5可知,纳米银紫外光谱的最大最大吸收波长在432±20nm范围。文献[12]报道,纳米银的特征吸收峰主要在410nm附近,与本文所得结果基本一致。而蒲公英提取液在此范围内则没有吸收,由此也证明了该生物合成方法所得到的纳米银。
2.6.3 纳米银红外吸收光谱利用FTIR测纳米银生物还原前后的典型的官能团变化,以识别提取液中发挥作用的官能团,其红外光谱图见图 6。
|
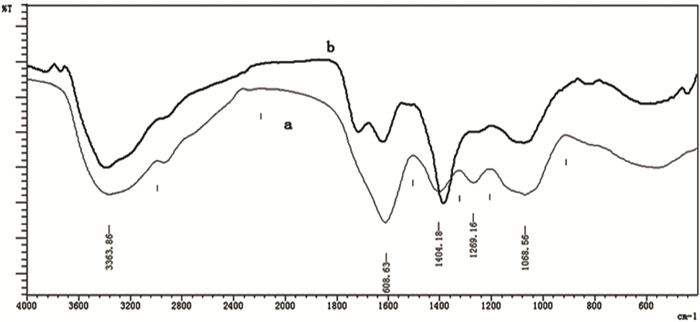
图 6 纳米银的FTIR光谱图 注:a.蒲公英提取液;b.纳米银溶液 |
图 6中a,蒲公英提取液的3363.86cm-1可能是νO-H或νN-H, 1269.16cm-1可能是νC-O或νC-0-C,1404.18cm-1可能是βO-H,1608.63cm-1可能是νC=C或βN-H。所以提取液中的νO-H, νC-O, βO-H有醇类,νO-H, νC-O, νC-0-C, νC=C表示含有水溶性的黄酮、酚类等物质。b,纳米银溶液中相比提取液在1705cm-1出现了新峰可能是νC=O,1608.63cm-1处的峰减弱,说明其中含有酰胺类物质,而原液中未出现可能是被1608.63cm-1处的强峰遮盖;在1269.16cm-1处的峰强有轻微减弱,在1404.18cm-1处的峰强有所增强,峰的位置也轻微的移动,这说明了蒲公英提取液中含有的醇类、酰胺类、黄酮、酚类物质在Ag+还原的过程中可能发挥还原和保护作用。
2.6.4 纳米银X射线衍射分析见图 7。
|
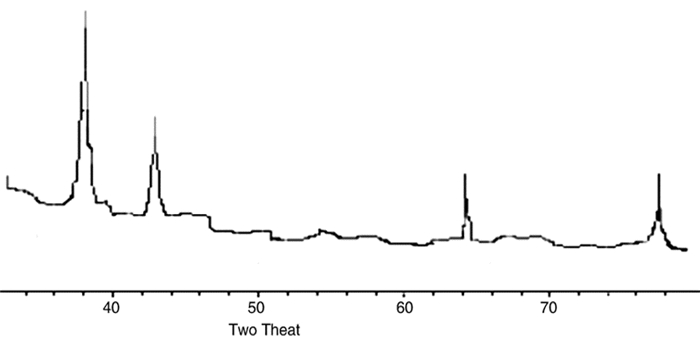
图 7 纳米银离子XRD衍射图谱 |
银的标准XRD图谱数据(20为38.096度、44.257度、64.406度、77.452度)。本文所得XRD图谱在相应位置均出现了相关衍射峰,说明了纳米银的形成。
2.7 纳米银的抗菌实验取同样量的纳米银混悬液及阿莫西林分散片配制溶液,考察其对大肠杆菌及葡萄球菌的杀菌作用。见图 8。
|
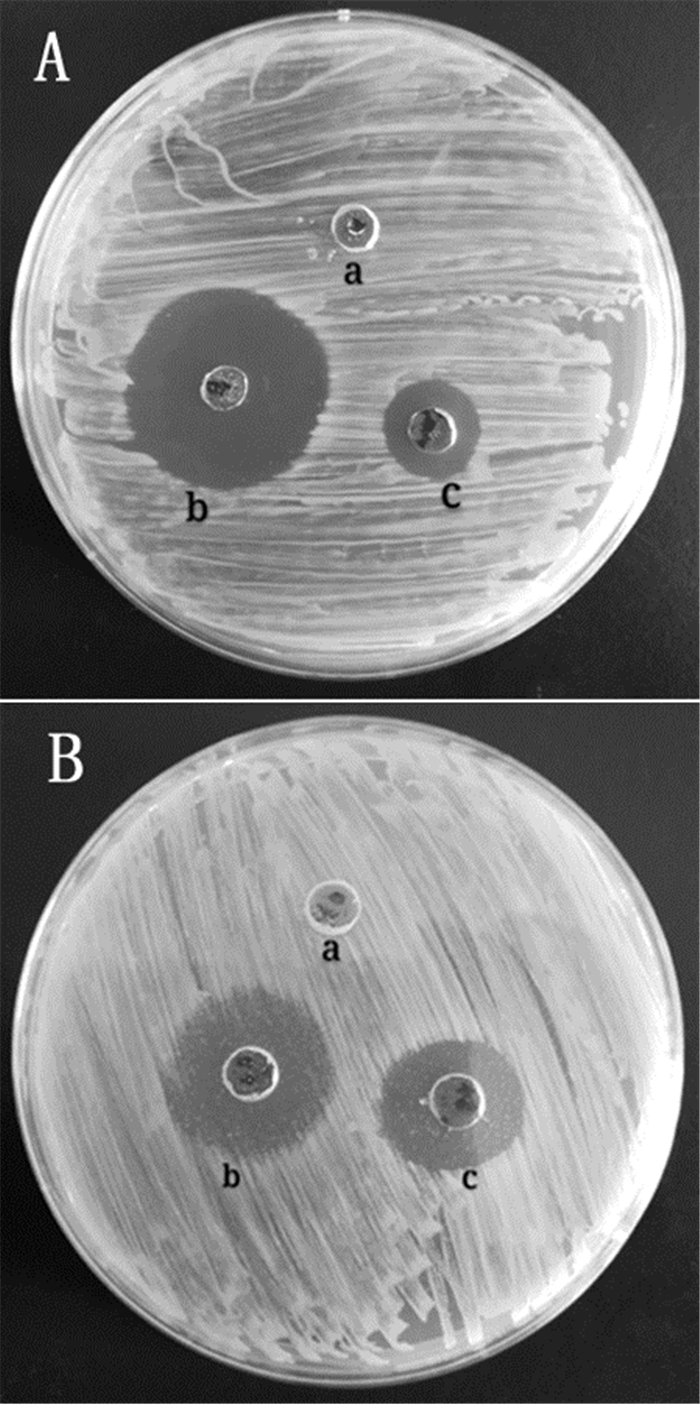
图 8 纳米银对大肠杆菌的抑菌试验 注:a.蒲公英原液;b.阿莫西林溶液;c.纳米银溶液A.大肠杆菌B.金黄色葡萄球菌 |
由图 8可见,纳米银对革兰氏阳性菌及革兰氏阴性菌均具有一定的抑制效应,而且加入同样量的纳米银,对葡萄球菌的抑菌圈明显大于同等条件下大肠杆菌的抑菌圈,说明纳米银对革兰氏阳性菌的抑菌效果明显优于革兰氏阴性菌。
3 结论在蒲公英提取液制备纳米银的过程中,最佳工艺条件为:提取液浓度0.01g/ml、反应温度85℃、硝酸银浓度0.005mg/ml、pH 6、时间2h。
利用生物合成法所得纳米银对革兰氏阳性菌较革兰氏阴性菌具有更强的杀菌效果
利用蒲公英提取液制备纳米银方案可行,且合成路线绿色环保,成本低、效率高,该方法为纳米银及其他贵金属的绿色生物合成提供了依据。
| [1] | 吴宗山, 胡海洋, 任艺, 等. 纳米银的抗菌机理研究进展[J]. 化工进展, 2015, 34(5): 1349–1356, 1370. DOI:10.16085/j.issn.1000-6613.2015.05.028 |
| [2] | Sun RW, Chen R, Chung NP, et al. Silver nanoparticles fabricated in Hepes buffer exhibit cytoprotective activities toward HIV-1 infected cells[J]. Chem Commun (Camb), 2005(40): 5059–5061. DOI:10.1039/b510984a |
| [3] | 林丽, 仇佩虹. 纳米银胶标记的DNA电化学传感器制备及应用[J]. 温州医学院学报, 2008, 38(2): 170–171. DOI:10.3969/j.issn.1000-2138.2008.02.024 |
| [4] | Joy Prabu H, Johnson I. Plant-mediated biosynthesis and characterization of silver nanoparticles by leaf extracts of Tragia involucrata, Cymbopogon citronella, Solanum verbascifolium and Tylophora ovata[J]. Karbala International Journal of Modern Science, 2015, 1(4): 237–246. DOI:10.1016/j.kijoms.2015.12.003 |
| [5] | Ghoreishi SM, Behpour M, Khayatkashani M. Green synthesis of silver and gold nanoparticles using Rosa damascena and its primary application in electrochemistry[J]. Physica E:Low-dimensional Systems and Nanostructures, 2011(1): 97–104. DOI:10.1016/j.physe.2011.07.008 |
| [6] | Shankar SS, Ahmad A, Sastry M. Geranium Leaf Assisted Biosynthesis of Silver Nanoparticles[J]. Biotechnology Progress, 2003, 19(6): 1627–1631. DOI:10.1021/bp034070w |
| [7] | Begum NA, Mondal S, Basu S, et al. Biogenic synthesis of Au and Ag nanoparticles using aqueous solutions of Black Tea leaf extracts[J]. Colloids Surf B Biointerfaces, 2009, 71(1): 113–118. DOI:10.1016/j.colsurfb.2009.01.012 |
| [8] | Patil RS, Kokate MR, Kolekar SS. Bioinspired synthesis of highly stabilized silver nanoparticles using Ocimum tenuiflorum leaf extract and their antibacterial activity[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2012, 91: 234–238. DOI:10.1016/j.saa.2012.02.009 |
| [9] | Kasthuri J, Veerapandian S, Rajendiran N. Biological synthesis of silver and gold nanoparticles using apiin as reducing agent[J]. Colloids Surf B Biointerfaces, 2009, 68(1): 55–60. DOI:10.1016/j.colsurfb.2008.09.021 |
| [10] | Ghoreishi SM, Behpour M, Khayatkashani M. Green synthesis of silver and gold nanoparticles using Rosa damascena and its primary application in electrochemistry[J]. Physica E:Low-dimensional Systems and Nanostructures, 2011(1): 97–104. DOI:10.1016/j.physe.2011.07.008 |
| [11] | Vijay Kumar PPN, Pammi SVN, Kollu P, et al. Green synthesis and characterization of silver nanoparticles using Boerhaavia diffusa plant extract and their anti bacterial activity[J]. Industrial Crops and Products, 2014, 52: 562–566. DOI:10.1016/j.indcrop.2013.10.050 |
| [12] | Li ZZ, Chen JF, Liu F, et al. Study of UV-shielding properties of novel porous hollow silica nanoparticle carriers for avermectin[J]. Pest Manag Sci, 2007, 63(3): 241–246. DOI:10.1002/ps.1301 |


 王慧云, 女, 博士, 教授, 硕士生导师, 全国优秀教师、济宁市有突出贡献中青年专家。主持承担了国家"十一五"科技支撑项目、山东省科技攻关项目等9项科研课题, 主持《药剂学》省级精品课程、药物制剂省级特色专业以及山东省高水平应用型专业群的建设。发表学术论文50余篇, 其中第一作者及通讯作者30余篇, SCI/EI收录15篇, 授权国家发明专利3项, 主编和参编教材4部, 获得科研奖励9项, 指导学生获得全国大学生课外科技学术作品挑战杯大赛三等奖等。学术兼职:全国药学教育研究会理事、山东省药学类本科教育教学指导委员会委员、济宁市药学会副理事长、济宁医学院重点实验室"药物化学与药物制剂研究所"所长
王慧云, 女, 博士, 教授, 硕士生导师, 全国优秀教师、济宁市有突出贡献中青年专家。主持承担了国家"十一五"科技支撑项目、山东省科技攻关项目等9项科研课题, 主持《药剂学》省级精品课程、药物制剂省级特色专业以及山东省高水平应用型专业群的建设。发表学术论文50余篇, 其中第一作者及通讯作者30余篇, SCI/EI收录15篇, 授权国家发明专利3项, 主编和参编教材4部, 获得科研奖励9项, 指导学生获得全国大学生课外科技学术作品挑战杯大赛三等奖等。学术兼职:全国药学教育研究会理事、山东省药学类本科教育教学指导委员会委员、济宁市药学会副理事长、济宁医学院重点实验室"药物化学与药物制剂研究所"所长