2. 济宁医学院公共卫生学院, 济宁 272067
2. School of Public Health, Jining Medical University, Jining 272067, China
饮酒后驾驶是导致交通事故的重要危险因素。目前,在司法案件中全血中乙醇含量的测定是判定饮酒后驾车和醉酒后驾车的依据,是建立在化学定量分析的结果基础上[1]。根据相关规定,血液中乙醇浓度为20.00、80.00 mg/100ml是车辆驾驶人员饮酒后驾驶和醉酒后驾驶的两个临界值[2]。定量分析结果的准确性直接关系到司法判定的正确性,尤其当检测结果为上述2个临界值附近时,对检测结果的准确性和可靠性进行不确定度评估是尤为重要的。
不确定度是用来直观反映检测工作中测定结果如何的。不确定度越小,说明测定结果与真值越接近,它可以表明检测的水平,反映实验室能力。自2004年开始,国家实验室认可委员会已将测量不确定度作为检测实验室通过认可评审的要求之一[3]。在法医毒物分析工作中,也正受到越来越大的压力要求其证明结果的质量,尤其是通过度量结果的可信度来证明结果的适宜性,而度量该项内容的一个有用的方法就是测量不确定度。因此,测量不确定度的评定在法医毒物分析工作中亦受到越来越多的重视。
本文根据司法鉴定技术规范《血液中乙醇的测定顶空气相色谱法》(SF/Z JD0107001-2016),采用顶空气相色谱(HS-GC)内标校准曲线法测定血液检材中乙醇的含量,依据中国合格评定委员会(CNAS)的要求和不确定度评定的指导性文件[4-6],从测定程序分析测量不确定的来源,找出影响不确定度的主要因素,对各个主要因素进行量化评定,计算出血液中乙醇测定结果的相对合成标准不确定度和扩展不确定度,特别针对处于2个临界值附近的检材进行检测及不确定度评估,以期为酒驾检测案件提供参考。
1 材料与方法 1.1 试剂乙醇(99.9%,批号:41222 04/2021,Dr.Ehrenstorfer GmbH),叔丁醇(≥99.5%,天津市科密欧),纯水由超纯水仪(Merck Millipore Elix Essential 3.5.10.15) 制备。
1.2 溶液配制乙醇对照品溶液:精密量取乙醇3.20ml于50ml容量瓶中,添加纯水至刻度,混匀,得50.00mg/ml乙醇储备溶液。用纯水稀释成1.00mg/ml乙醇工作液。
叔丁醇内标溶液:精密量取叔丁醇0.32ml于50ml容量瓶中,添加纯水至刻度,混匀,得5.00mg/ml叔丁醇储备液;用纯水稀释成4.00mg/100ml叔丁醇内标工作液。
1.3 仪器与实验条件 1.3.1 仪器Agilent顶空气相色谱仪(7697A-7890B),可调移液器(BIO-DL,100~1000 μl,10~100 μl)由山东省计量科学研究院检定,分度吸管(2、5、10 ml)、容量瓶(50、100 ml)由济宁市计量测试所检定。
1.3.2 顶空气相色谱仪实验条件气相色谱仪条件:色谱柱:DB-ALC2 (30.00m×0.32mm×1.20μm)石英毛细管柱;柱温:40℃,保持3min;检测器:火焰离子化检测器(FID);检测器温度:250℃;进样口温度:150℃;载气(N2):8ml/min;燃气(H2):30ml/min;空气:400ml/min。
顶空自动进样器条件:加热箱温度:65℃;定量环温度:105℃;传输线温度:110℃;气相循环时间:3.50min;样品瓶加热平衡时间:10.00min;样品瓶加压时间:0.10min;定量环充满时间:0.10min;定量环平衡时间:0.05min;进样时间:1.00min。
1.4 制样及分析 1.4.1 校准曲线的绘制取空白全血配制成含乙醇质量浓度为10.00mg/100ml、20.00mg/100ml、50.00mg/100ml、80.00mg/100ml、100.00mg/100ml、200.00mg/100ml及300.00mg/100ml的系列样品,各取0.10 ml两份分别加入顶空瓶中,再添加0.50ml浓度为4.00mg/100ml的叔醇内标工作液,密封,混匀,置于顶空进样器—气相色谱仪中分析,建立乙醇内标校准曲线的回归方程。
1.4.2 数学模型的建立根据乙醇内标校准曲线的回归方程,得血液检材中乙醇浓度测定公式:
| $ C{\rm{ = }}\frac{{Y{\rm{-}}b}}{a}{C_{内标}} $ | (1) |
式中:Y——待测血液检材中乙醇的峰面积与内标物的峰面积之比;
b——截距;
a——斜率;
C内标——叔丁醇内标工作液浓度;
C——待测血液检材中乙醇浓度。
1.4.3 血液检材检测血液检材1和血液检材2各取2份0.10 ml分别于样品瓶内,添加0.50 ml浓度为4.00 mg/100ml的叔丁醇内标工作液,密封,混匀,置于顶空自动进样器中,加热,进样测定,同一个检材的2份样品测定结果的相对标准偏差≤5%。
另随机选取不同浓度10组血液检材,同上操作,进行A类不确定度评定。
2 结果与讨论 2.1 乙醇内标法校准曲线的回归方程所得校准曲线回归方程为:Y=0.0425641X-0.0397095,相关系数r=0.99989;Y为乙醇与叔丁醇的峰面积比值,X为样品中乙醇与内标叔丁醇的含量比。
2.2 血液检材测定数据检材1和检材2测定结果见表 1。
| 表 1 待测血液检材的测定结果 |
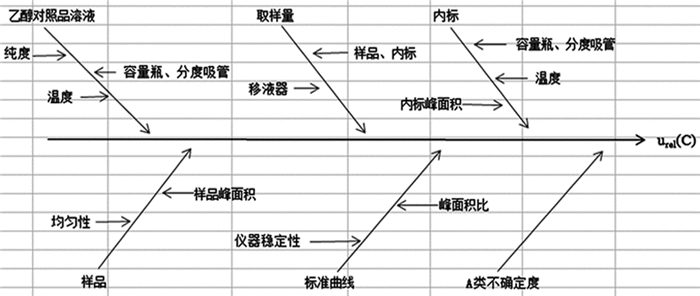
评估不确定度时,尽可能密切观察产生不确定度的所有可能来源,得图 1。
|
图 1 HS-GC法测定血液中乙醇含量的测量不确定度来源因果图 |
不确定度分量分为A类和B类。
2.4.1 A类不确定度随机检测10个血液检材进行A类不确定度评定。见表 2。
| 表 2 10个血液检材测定浓度及平均值、残差平方值 |
单次测量的标准偏差:
平均值的标准偏差:
uc(Ai)=S(A)=S/
检材1的相对标准不确定度为:
urel(A1)= uc(A)/C1=0.03402
检材2的相对不确定度为:
urel(A2)= uc(A)/C2=0.008436
2.4.2 B类不确定度1) 乙醇及内标物叔丁醇对照品引入的相对标准不确定度urel(P)
纯度是潜在的附加不确定度来源。
乙醇对照品的纯度P为99.9%,标注的不确定度为0.5%;其相对标准不确定度(矩形分布)urel(P1)=0.5%/
叔丁醇对照品的纯度P为≥99.5%,即叔丁醇的纯度可表示为(0.995±0.005),其相对标准不确定度(矩形分布)urel(P2)=0.005/(0.995)=0.002901。
2) 容量瓶校准引入的urel(V)。配制乙醇及叔丁醇工作液时使用到50及100 ml容量瓶稀释定容,则定容引入的相对标准不确定度由容量瓶校准检定可得,见表 3。
| 表 3 容量瓶的校准数据 |
即50ml容量瓶的相对标准不确定度为:
urel(V1)= uc(Vi)/50=0.001155
100 ml容量瓶的相对标准不确定度为:
urel(V2)= uc(Vi)/100=0.001155
3) 分度吸管校准引入的相对标准不确定度。在配制乙醇及叔丁醇工作液时使用到2、5、10 ml的分度吸管进行溶液的移取、稀释,则工作液配制中对照品取量引入的相对标准不确定度由分度吸管的校准检定可得。见表 4。
| 表 4 分度吸管的校准数据 |
2ml分度吸管的urel(V3)= 0.003464;
5ml分度吸管的urel(V4)= 0.002887;
10ml分度吸管的urel(V5)= 0.002887。
4) 温度影响引起的uc(T)。实验温控在(20±4)℃,乙醇的膨胀系数为0.00109/℃,叔丁醇的膨胀系数为0.00133℃。
乙醇产生的体积变化为V50=±(Vi×4×膨胀系数)=±0.2180 ml;设为矩形分布,则uc(T1)= V50/
叔丁醇产生的体积变化为V500=±(Vi×4×膨胀系数)=±2.660 ml;设为矩形分布,则uc(T2)= V500/
5) 取样量引入的标准不确定度。本实验中血液检材取样量为0.10 ml,内标叔丁醇溶液取样量为0.50 ml,而此过程的不确定度主要由移液器引入,移液器的校准数据见表 5。
| 表 5 移液器的校准数据 |
由表 5可知,吸取100 μl样品时不确定度为0.58 μl,标准不确定度为0.29 μl,相对标准不确定度urel(V6)=0.0029;
吸取500 μl内标叔丁醇溶液时不确定度为0.33μl,标准不确定度为0.16μl,相对标准不确定度urel(V7) =0.00033。
6) 气相色谱仪引入的相对标准不确定度
气相色谱仪(仪器出厂编号:CN15113150),其检定重复性RSD(GC)=0.18%,K=2,则urel(GC)= RSD/K=0.0090。
7) 标准曲线引入的相对标准不确定度
校准曲线产生的不确定度来源于校准曲线残差的标准偏差,残差为测定值与校准曲线拟合值之差的绝对值|Y-Ŷ|,残差计算见表 6。
| 表 6 标准曲线残差计算表 |
残差的标准偏差为:
标准溶液含量比残差的平方和为:
标准曲线引入的标准不确定度为:
uc(Xi)=
uc(X1)==0.4416
uc(X2)==0.4100
即对应的相对标准不确定度为:
urel(X1)= uc(X1)/C1=0.02286
urel(X2)= uc(X2)/C2=0.005264
8) 待测样品峰面积与内标峰面积之比引入的标准不确定度
样品及内标的峰面积自动积分,最后1位数字估算带来的误差对于不确定度的贡献非常小,可以忽略不计。
2.4.3 合成标准不确定度的计算因各分量相互独立,则合成相对标准不确定度
| $ \begin{array}{l} {{\rm{u}}_{{\rm{rel}}}}\left( {\rm{C}} \right) = \\ \;\;\sqrt {{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{A}}_{\rm{i}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{P}}_{\rm{1}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{P}}_{\rm{2}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{V}}_{\rm{1}}}{{\rm{)}}^{\rm{2}}}{\rm{, \ldots, }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{V}}_{\rm{7}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{T}}_{\rm{1}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{T}}_{\rm{2}}}{{\rm{)}}^{\rm{2}}}{\rm{ + }}{{\rm{u}}_{{\rm{rel}}}}{\rm{(}}{{\rm{X}}_{\rm{i}}}{{\rm{)}}^{\rm{2}}}} \end{array} $ |
转化成合成标准不确定度为:
uc(C1)=urel(C1) ×C1=0.8270 mg/100ml
uc(C2)=urel(C2) ×C2=1.237 mg/100ml
2.5 扩展不确定度的计算扩展不确定度表示为U=k·uc(C),取置信水平P=95%,包含因子k=2。
检材1的扩展不确定度U1=1.65 mg/100ml;
检材2的扩展不确定度U2=2.47 mg/100ml。
2.6 报告检材1的乙醇含量为(19.32±1.65) mg/100ml,k = 2;
检材2的乙醇含量为(77.88±2.47) mg/100ml,k = 2。
3 结论检测结果的不确定度是定量说明检测结果质量的一个重要参数。血液中乙醇检测不确定度的影响因素主要来自于样品的检测误差、检测仪器的精密度、标准物质和内标物质的纯度、容量器皿的不确定度、标准曲线引入的不确定度等。据评定结果可知,样品测定引起的标准不确定度分量最大、其次是标准曲线,而对照品纯度、温度以及气相色谱仪等引入的不确定度分量相对较小。也就表明合成不确定度的数值主要取决于A类与标准曲线引入的不确定度分量。即在检测过程中,实验人员熟练操作标准及内标溶液的配制稀释,熟练掌握移液器吸取黏稠血液检材的方法,定期对仪器进行校准,严格按照规程操作,对于降低对实验结果产生的不确定度影响是较为重要的。此外,除了严格按照检测规程进行操作外,也应保证标准对照品的质量,加强标准溶液购买和使用的监控,减少标准溶液带来的不确定度。
本方法可用于日常检案工作中HS-GC法检测血液中乙醇含量的检测结果的不确定度评定,且当更改了新的标准系列或者样品测量,而其他的实验条件没有改变,通过相对应分量数据的更改,即可快速获得检测结果的扩展不确定度,方便在实际工作中评估不同情况的乙醇含量测定的不确定度。此外,本文特别给出了当检测的乙醇浓度在我国规定的酒驾和醉驾临界值(20.00mg/100ml和80.00mg/100ml)附近时的不确定度完整检测报告,为法医鉴定工作提供参考信息与基础数据。
| [1] | 中国实验室国家认可委员会. CNAS-GL06:2006.化学分析中不确定度的评估指南[M]. 北京: 中国计量出版社, 2006: 4-18. |
| [2] | 中华人民共和国国家质量监督检验检疫总局. 国家标准GB/T 19522-2010. 车辆驾驶人员血液、呼气酒精含量阈值与检验[S]. 北京: 国家标准化管理委员会办公室, 2017. |
| [3] | 卓先义, 马栋, 卜俊, 等. 顶空气相色谱法测定血液中乙醇不确定度的评估[J]. 中国司法鉴定, 2004(3): 12–15. DOI:10.3969/j.issn.1671-2072.2004.03.003 |
| [4] | 中国计量科学研究院. JJF1059-1999测量不确定度评定与表示[S]. 北京: 中国计量出版社, 1999. |
| [5] | 中国合格评定国家认可委员会. CNAS-GL05: 测量不确定度要求的实施指南[S]. 北京: 中网计量出版社, 2006. |
| [6] | 中国合格评定国家认可委员会. CNAS-GL07: 测量不确定度评估和报告通用要求[S]. 北京: 中网计量出版社, 2006. |

