2. 济宁医学院附属医院, 济宁 272029;
3. 济宁医学院基础医学院, 济宁 272067
2. Affiliated Hospital of Jining Medical University, Jining 272067, China;
3. School of Basic Medicine Sciences, Jining Medical University, Jining 272067, China
蛋白质是生物体内具有重要生理功能的大分子,是构成细胞的基本有机物,如血清白蛋白是血浆中含量最丰富的蛋白质,对于进入体内的药物小分子的储存、输运、受体部位药理作用的发挥等具有多方面的作用[1-2];血清蛋白质还有着广泛的结合能力,能与内源性及外源性物质相结合,也能与溶于水和难溶于水的一些物质相结合。牛血清白蛋白 (bovine serum albumin, BSA) 是生命体液的一种重要成分,能提供血液渗透压并且具有参与生物系统质量运输的功能。由于它的理化性能具有良好的特点,所以它被广泛应用于分子生物学和细胞生物学领域。它以一种大球形蛋白质的形式自然存在于牛血液和牛奶中,并且它也能增加疏水性药物在血浆中的表观溶解度[3-4]。
纳米银粒子 (silver nanoparticles) 自问世以来一直深受人们的关注,这不仅是由于其具有独特的电子特性、光学特性,还因为其具有良好的抗菌性和生物兼容性等优点[5-6]。因此,纳米银粒子是一种非常有用的纳米材料。纳米银材料的功能在一定程度上决定于它的形状、大小、构造以及结晶度[7]。相对于一维、二维银纳米,三维银纳米具有其稳定的空间结构,更容易使药物到达病变部位,与受体结合发挥药效。其包括球形、正四面体、三棱锥等形状。由于球形纳米银颗粒 (spherical silver nanoparticles, SAgNPs) 具有特殊的表面等离子体光学特性,其在生物医学领域的应用研究越来越深入[8],比如,探讨球形银纳米和BSA之间的相互作用机理对理解纳米银的药理作用非常重要。
本文利用化学还原法合成了结构和性质稳定的球形纳米银溶液,并对其进行形貌表征和粒径分析,然后,利用光谱学方法研究纳米银和BSA之间的相互作用,得到了相应的光谱学和热力学数据,为纳米银在医学领域的广泛应用提供了理论依据。
1 实验部分 1.1 试剂和仪器硝酸银 (AgNO3)、二水合柠檬酸三钠 (Na3C6H5O7) 均购自国药集团化学试剂有限公司; 聚乙烯吡咯烷酮 (PVP), Mw=29.0 kg/mol,天津科密欧化学试剂有限公司; 硼氢化钠 (NaBH4),纯度98%,购自Alfa; BSA (纯度99%,Mw=66.0 kg/mol,北京欣科中晶生物科技有限公司);三羟甲基氨基甲烷 (Tris), 购自Alfa。
岛津UV-2501 PC紫外分光光度计 (日本);岛津RF-5301 PC荧光分光光度计 (日本);EL 204电子天平 (梅特勒-托利多仪器有限公司,上海);DF-Ⅱ型集热式磁力加热搅拌器,德国艾本德可调移液器,扫描电子显微镜 (Zeiss,德国)。
1.2 球形纳米银的制备与表征利用化学还原法合成球形纳米银,具体操作为[9]:将AgNO3溶液 (2mM, 12.5ml) 与Na3C6H5O7溶液 (4mM, 12.5ml) 在烧杯中混合,快速磁力搅拌5min,加入PVP溶液 (0.02g/ml, 25ml),继续搅拌10min,然后加入NaBH4溶液 (10mM, 1ml) 搅拌5min,于40℃水浴中再反应5min。取出冷却,离心,洗涤。
利用紫外分光光度计对合成的纳米银溶液进行初步测定,再利用扫描电子显微镜对纳米银粒子的形貌进行分析检测。
1.3 紫外光谱测定利用紫外分光光度计,以1200 nm/min的速度对波长范围在200 nm到900 nm处的紫外吸收光谱进行了测量。用Tris-HCl缓冲溶液 (pH=7.40) 配制BSA标准溶液;比色皿中BSA的浓度固定为0.80μM。
1.4 荧光光谱测定为了进一步了解纳米银与BSA的相互作用,利用荧光分光光度计对纳米银与牛血清白蛋白相互作用的荧光强度进行了检测。激发波长设定在280 nm,并且相应的扫描波段是280~450 nm,激发和发射狭缝宽度分别为5 nm和3 nm。比色皿中BSA的浓度固定为0.80μM。将所得荧光数据处理绘制Stern-Volmer图像,求出结合体系的热力学参数。
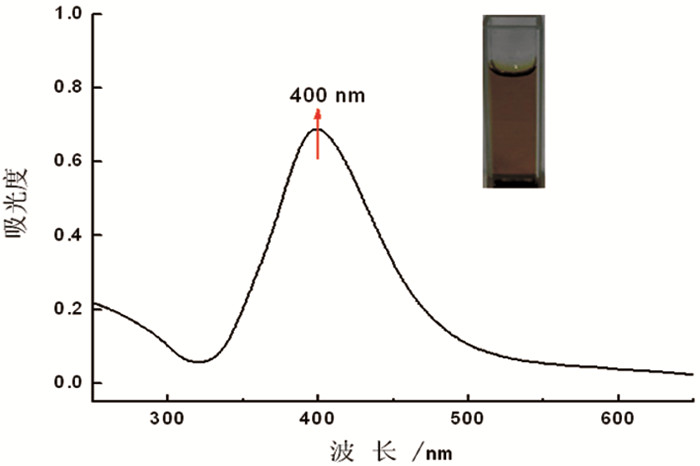
2 结果与讨论 2.1 球形纳米银的表征图 1是纳米银溶液的紫外可见吸收光谱图,由图 1可知,此溶液在400 nm处有一紫外吸收峰,此吸收峰是球形纳米银的特征吸收峰;而且,由插入图可知纳米银溶液的颜色为黄色,与文献报道的结果相一致[10];由此实验结果可知合成的纳米银的形状为球形。
|
图 1 球形纳米银的紫外吸收光谱图 注:插入图为球形纳米银的分散液 |
另外,本文还利用扫描电子显微镜对纳米银进行了形貌表征 (见图 2A),由图可知,纳米银颗粒为球形,且此颗粒尺度分布均匀,由粒径分析软件可得到其平均粒径约为25 nm (结果见图 2B)。

|
图 2 球形纳米银的形貌表征 注:(A) 扫描式电子显微镜 (SEM) 图像,(B) 粒径分布图 |
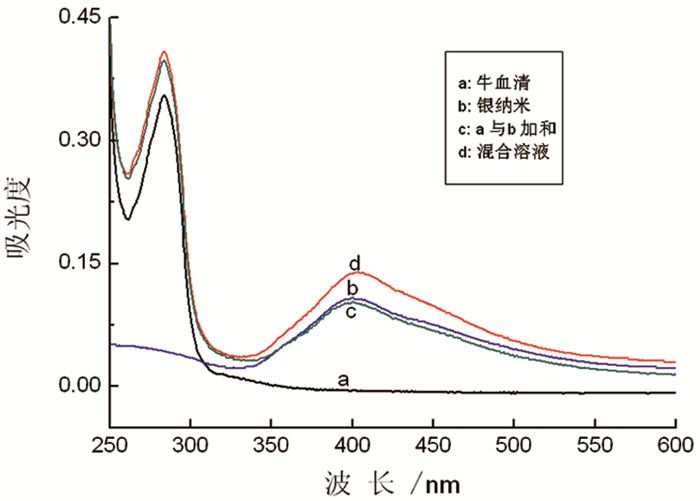
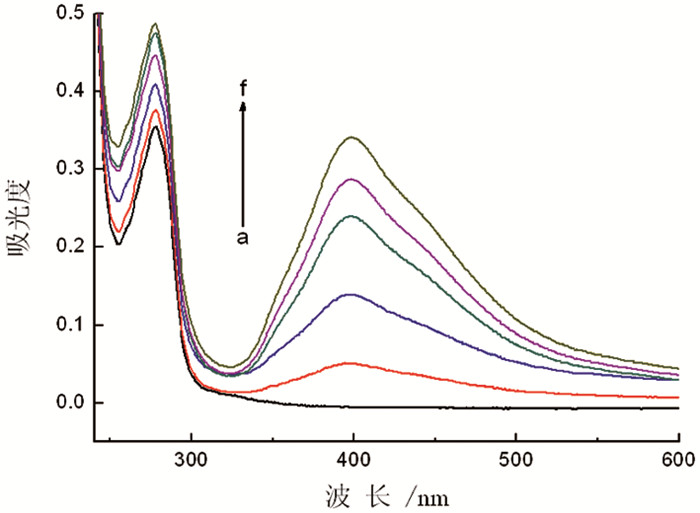
紫外吸收光谱测定法是研究纳米银与蛋白质之间相互作用的一种重要方法。图 3是球形纳米银与BSA在缓冲溶液 (pH=7.40) 中相互作用的紫外吸收光谱图。由图 3可知,BSA溶液和球形纳米银溶液的特征吸收峰分别在280nm和400nm处,而纳米银与BSA混合溶液的特征吸收峰约在280nm和404nm处,此结果表明混合溶液的吸收峰不是纳米银和BSA特征吸收峰的简单加和。混合溶液在400 nm处的吸收峰发生了红移现象,且吸收峰强度有所变化,此现象表明球形纳米银与BSA之间发生了相互作用,形成了纳米银与BSA的复合物。另外,由实验结果可知只有400 nm处的特征吸收峰有轻微红移到404 nm处,而能量较高的280 nm处的特征峰没有位移,说明这种复合物是通过无化学键改组的弱相互作用形成。另外,由图 4可知,随着纳米银浓度的增加,混合溶液的紫外吸光度也随着增强。与空白BSA溶液的光谱图相比较,纳米银对BSA溶液的紫外吸收峰的强度产生了显著的影响,此结果也说明球形纳米银与BSA在溶液中发生了相互作用,且形成了复合物。

|
图 3 球形纳米银与牛血清白蛋白 (BSA) 相互作用的紫外吸收光谱图 注:牛血清白蛋白 (BSA) 的浓度固定为0.80μM |
|
图 4 不同量的球形纳米银与牛血清白蛋白 (BSA) 相互作用的紫外吸收光谱图 注:a到f纳米银溶液的浓度分别为0, 3.0, 3.8, 6.5, 13.0, 15.6μM |
由于纳米银溶液几乎没有荧光信号,而BSA溶液的荧光信号较强,所以,可以采用荧光光谱实验来测定纳米银与BSA相互作用的情况。由图 5可知,BSA溶液的荧光光谱强度随着球形纳米银溶液浓度的增加而不断下降,即发生了荧光猝灭现象,BSA溶液的荧光猝灭程度随着纳米银浓度的增加而明显增强,这说明该纳米银溶液和蛋白质在溶液中发生了相互作用。
|
图 5 不同量的球形纳米银与牛血清白蛋白相互作用的荧光光谱图 注:a到h纳米银溶液的浓度为0, 3.0, 3.8, 6.5, 13.0, 15.6, 18.2, 21.0μM;插入图为Stern-Volmer方程 |
荧光猝灭机理通常有动态和静态猝灭,这2种类型的猝灭机理的差异可以通过分析双分子猝灭过程的速率常数 (Kq) 来区分。如果Kq值大于生物大分子的扩散速率常数 (kd 2.0×1010 M-1S-1)[11-12],则静态猝灭为主要机理,反之,则为动态猝灭。猝灭机理遵循Stern-Volmer方程:
| $ {{F}_{0}}/F=1+{{K}_{\text{sv}}}\left[Q \right]=1+{{K}_{\text{q}}}\tau 0\left[Q \right] $ | (1) |
式中:F0和F分别是为加入和加入猝灭剂 (球形纳米银) 后的荧光强度;[Q]为猝灭剂浓度mol/L; Kq为双分子猝灭过程的速率常数;Ksv为Stern-Volmer猝灭常数M-1;τ0为无猝灭剂存在下大分子的平均寿命,对于BSA, τ0约为10-8 s[13]。由图 5插入图可知,SAgNPs-BSA体系的Kq为3.18×1012M-1S-1,大于扩散速率常数 (kd 2.0×1010 M-1S-1),由此可以,球形纳米银对BSA的荧光猝灭以静态猝灭为主。
为了更好地理解球形纳米银与BSA相互作用的机理,还分析了荧光强度与猝灭剂之间的关系。即应用公式 (1)[11]:
| $ \text{log}({{\text{F}}_{0}}-\text{F})/\text{F}=\text{logK}+\text{ nlog}\left[Q \right] $ | (2) |
(2) 式中F0和F分别为BSA水溶液中无和有球形纳米银存在时的荧光强度,[Q]为球形纳米银的浓度。以log (F0-F)/F对log[Q]作图,由图 6中直线斜率和截距可求出球形纳米银与BSA分子的结合位点数 (n) 和平衡常数 (K),其数值分别为1.09和4.91×104 M-1。根据公式 (3),由结合常数K可以计算标准吉布斯自由能变ΔG°。

|
图 6 log[纳米银]对log[荧光强度差/荧光强度]作图 |
| $ \Delta {{\text{G}}^{\circ }}=-2.303\text{RT logK} $ | (3) |
从 (2) 式中得到ΔG°=-28.02 kJ/mol < 0。较大正值的平衡常数和较大负值的标准吉布斯自由能变都表明纳米银和BSA的结合过程能够自发进行,并且可以在溶液中形成复合物。
3 结论本文利用化学还原法合成了粒径均匀的球形纳米银溶液,并利用紫外可见吸收光谱和扫描电子显微镜等方法对其形貌和粒径进行了分析;同时还利用紫外和荧光光谱法研究了其与BSA在缓冲溶液中的相互作用。光谱实验结果表明随着纳米银溶液浓度的增加,混合溶液的紫外强度有所增强;而荧光光谱却发生了显著的猝灭现象。由此结果可知纳米银与BSA在溶液中发生了相互作用,形成了相应的复合物,并且此结合过程是自发进行的。
| [1] | Gao PF, Zhang S, Li HW, et al. A two-step binding process of Eu-containing polyoxometalates to bovine serum albumin[J]. Langmuir, 2015, 31(39): 10888–10896. DOI:10.1021/acs.langmuir.5b02868 |
| [2] | Li JC, Li N, Wu QH, et al. Study on the interaction between clozapine and bovine serum albumin[J]. J Mol Struct, 2007, 833(1): 184–188. DOI:10.1016/j.molstruc.2006.09.019 |
| [3] | Ghosh S, Dey J. Binding of fatty acid amide amphiphiles to bovine serum albumin:role of amide hydrogen bonding[J]. J Phys Chem B, 2015, 119(25): 7804–7815. DOI:10.1021/acs.jpcb.5b00965 |
| [4] | Alam S, Mukhopadhyay A. Conjugation of gold nanorods with bovine serum albumin protein[J]. J Phys Chem C, 2014, 118(47): 27459–27464. DOI:10.1021/jp5093465 |
| [5] | Tai JT, Lai CS, Ho HC, et al. Protein-silver nanoparticle interactions to colloidal stability in acidic environments[J]. Langmuir, 2014, 30(43): 12755–12764. DOI:10.1021/la5033465 |
| [6] | Shao W, Liu X, Min H, et al. Preparation, characterization, and antibacterial activity of silver nanoparticle-decorated graphene oxide nanocomposite[J]. ACS Appl Mater Interfaces, 2015, 7(12): 6966–6973. DOI:10.1021/acsami.5b00937 |
| [7] | Wang Y, Zheng Y, Huang CZ, et al. Synthesis of Ag nanocubes 18-32 nm in edge length:the effects of polyol on reduction kinetics, size control, and reproducibility[J]. J Am Chem Soc, 2013, 135(5): 1941–1951. DOI:10.1021/ja311503q |
| [8] | 徐香玉, 王浩, 杜中玉, 等. 球形纳米银与人血清白蛋白相互作用的研究[J]. 化学通报, 2016, 79(3): 279–282. |
| [9] | Steinigeweg D, Schlücker S. Monodispersity and size control in the synthesis of 20-100nm quasi-spherical silver nanoparticles by citrate and ascorbic acid reduction in glycerol-water mixtures[J]. Chem Commun, 2012, 48(69): 8682–8684. DOI:10.1039/c2cc33850e |
| [10] | Ravindran A, Singh A, Raichur AM, et al. Studies on interaction of colloidal Ag nanoparticles with bovine serum albumin (BSA)[J]. Colloid Surface B Biointerfaces, 2010, 76(1): 32–37. DOI:10.1016/j.colsurfb.2009.10.005 |
| [11] | Ali MS, Al-Lohedan HA, Atta AM, et al. Interaction of human serum albumin with silver nanoparticles functionalized with polyvinylthiol[J]. J Mol Liq, 2015, 204: 248–254. DOI:10.1016/j.molliq.2015.01.032 |
| [12] | Zhao X, Liu R, Teng Y, et al. The interaction between Ag+ and bovine serum albumin:a spectroscopic investigation[J]. Sci Total Environ, 2011, 409(5): 892–897. DOI:10.1016/j.scitotenv.2010.11.004 |
| [13] | Zhao L, Liu R, Zhao X, et al. New strategy for the evaluation of CdTe quantum dot toxicity targeted to bovine serum albumin[J]. Sci Total Environ, 2009, 407(18): 5019–5023. DOI:10.1016/j.scitotenv.2009.05.052 |


 徐香玉, 女, 汉族, 1982年12月出生于山东省济宁市。2013年毕业于北京师范大学化学学院分析化学专业, 获得理学博士学位。主要研究领域包括化学热力学、电分析化学。2013年8月到济宁医学院生物纳米技术与医学工程研究所工作, 主要从事电分析化学以及纳米材料的合成和应用研究, 同时还主要讲授《医用化学》、《医学化学实验》等课程。目前以第一作者在SCI期刊上发表论文8篇, 分别发表在《Journal of Mass Spectrometry》、《Journal of Molecular Liquids》、《Ther mochimica Acta》和《Medicinal Chemistry Research》, 累计影响因子为14.7
徐香玉, 女, 汉族, 1982年12月出生于山东省济宁市。2013年毕业于北京师范大学化学学院分析化学专业, 获得理学博士学位。主要研究领域包括化学热力学、电分析化学。2013年8月到济宁医学院生物纳米技术与医学工程研究所工作, 主要从事电分析化学以及纳米材料的合成和应用研究, 同时还主要讲授《医用化学》、《医学化学实验》等课程。目前以第一作者在SCI期刊上发表论文8篇, 分别发表在《Journal of Mass Spectrometry》、《Journal of Molecular Liquids》、《Ther mochimica Acta》和《Medicinal Chemistry Research》, 累计影响因子为14.7